Перейти к:
Прогнозирование поражения ствола левой коронарной артерии у больных стабильной ишемической болезнью сердца с использованием технологии искусственного интеллекта
https://doi.org/10.20996/1819-6446-2026-3232
EDN: KDRPWZ
Аннотация
Цель. Разработать программный комплекс, прогнозирующий наличие значимого стеноза ствола левой коронарной артерии (ЛКА) у больных стабильной ишемической болезнью сердца (ИБС) на основе клинико-инструментальных признаков при помощи методов машинного обучения.
Материал и методы. В исследование включены 208 пациентов со стабильной ИБС, госпитализированных для плановой коронарной ангиографии. По результатам инвазивной коронароангиографии были выделены две группы больных: основная группа — 104 пациента с гемодинамически значимым стенозом ствола ЛКА и группа контроля — 104 пациента без обструктивного поражения коронарных артерий. Значимым считали стеноз ствола ЛКА >50%. На основе изучения историй болезни была создана база данных Excel, содержащая информацию о 107 клинико-инструментальных признаках всех больных. На основании экспертной оценки до начала построения моделей осуществлен отбор 63 из них, которые регистрируются в медицинской карте пациента в реальной практике при стандартной стратегии диагностики ИБС согласно клиническим рекомендациям. Проведен поиск коллинеарных признаков, что позволило исключить 4 признака с низким порогом корреляции. С учетом характера рассматриваемых данных и предположения о наличии в них нелинейных взаимосвязей в качестве алгоритма машинного обучения был выбран градиентный бустинг. Разработанные в ходе исследования программы написаны на языке программирования Python в интегрированной среде программирования PyCharm.
Результаты. На основе наиболее информативных признаков были построены модели прогнозирования поражения ствола ЛКА у больных ИБС. В качестве оптимального алгоритма машинного обучения был определен градиентный бустинг. Рассмотрены три его реализации: LightGBM (Light Gradient Boosting Machine), XGBoost (Extreme Gradient Boosting) и CatBoost (Categorical Boosting). Наиболее эффективной для классифицирования представленных объектов оказалась модель CatBoost. Программный комплекс с использованием модели CatBoost продемонстрировал точность прогноза классификатора 86,2% на тестовом наборе данных при чувствительности 77% и специфичности 76,9%, соответственно. По данным построенных кривых обучения установлено, что дальнейшее расширение объема обучающих данных улучшит качество модели.
Заключение. Разработанный программный комплекс выявления гемодинамически значимого стеноза ствола ЛКА у больных ИБС имеет хорошую точность прогноза с перспективой дальнейшего обучения. Полученное решение может быть интегрировано в диагностический процесс в составе приложения для персонального компьютера либо веб-интерфейса с целью обеспечения поддержки принятия врачебных решений.
Ключевые слова
Для цитирования:
Кудаев Ю.А., Лоховинина Н.Л., Абесадзе И.Т., Алугишвили М.З., Калиниченко А.Н., Смирнова А.П., Панов А.В. Прогнозирование поражения ствола левой коронарной артерии у больных стабильной ишемической болезнью сердца с использованием технологии искусственного интеллекта. Рациональная Фармакотерапия в Кардиологии. 2026;22(1):22-29. https://doi.org/10.20996/1819-6446-2026-3232. EDN: KDRPWZ
For citation:
Kudaev Yu.A., Lokhovinina N.L., Abesadze I.T., Alugishvili M.Z., Kalinichenko A.N., Smirnova A.P., Panov A.V. Prediction of left main coronary artery lesion in patients with stable coronary artery disease using artificial intelligence technology. Rational Pharmacotherapy in Cardiology. 2026;22(1):22-29. (In Russ.) https://doi.org/10.20996/1819-6446-2026-3232. EDN: KDRPWZ
Введение
Ишемическая болезнь сердца (ИБС) занимает ведущее место в структуре заболеваемости и смертности в мире [1]. При этом пациенты с поражением левой коронарной артерии (ЛКА), которая обеспечивает кровоснабжение большей части миокарда левого желудочка (ЛЖ), составляют подгруппу с экстремально высоким риском неблагоприятных сердечно-сосудистых событий [2].
Распространенность стеноза ствола ЛКА среди больных ИБС по данным коронарной ангиографии (КАГ) составляет 5-7%, а клинические проявления могут варьировать от бессимптомного течения до внезапной смерти [3]. Традиционными факторами риска поражения ЛКА, как и системного атеросклероза, считают курение, ожирение, артериальную гипертензию, дислипидемию, сахарный диабет (СД) [4]. По данным многоцентрового исследования ISCHEMIA более высокая вероятность стеноза ствола ЛКА ассоциирована с мужским полом и возрастом старше 65 лет [5]. Отмечено, что поражение ЛКА обладает высоким уровнем наследуемости [6]. Кроме того, результаты исследований указывают на взаимосвязь генетических полиморфизмов с риском развития атеросклероза ствола ЛКА [7].
Диагностика поражения ЛКА основана на стандартах верификации ИБС, а именно, оценке предтестовой вероятности обструктивных изменений в коронарных артериях (КА), проведении электрокардиографии (ЭКГ), эхокардиографии (ЭхоКГ), нагрузочного тестирования, компьютерно-томографической коронарной ангиографии (КТ-КГ) и КАГ [8]. У ряда пациентов на ЭКГ могут наблюдаться изменения сегмента ST и/или аномалии зубца T, отражающие реакцию миокарда на хроническую ишемию [9]. Выполнение ЭхоКГ предоставляет информацию о систолической функции ЛЖ и наличии зон нарушения локальной сократимости, а функциональное тестирование позволяет верифицировать преходящую ишемию миокарда. Единственным неинвазивным методом визуализации анатомии КА и локализации стенотического поражения является КТ-КГ [10]. «Золотым стандартом» диагностики ИБС остается инвазивная КАГ, по данным которой гемодинамически значимым считается стеноз ствола ЛКА >50% [11]. Однако по результатам КАГ лишь в половине случаев подтверждается наличие обструктивной ИБС, что приводит к росту необоснованных инвазивных исследований и медицинских расходов [12].
Стандартизированные алгоритмы прогнозирования поражения ЛКА в настоящее время не представлены. При этом авторами все чаще в качестве вспомогательного диагностического инструмента для идентификации ИБС используются алгоритмы машинного обучения (МО) [13][14]. Хорошее качество прогнозирования трёхсосудистого поражения КА у больных стабильной ИБС демонстрируют модели с использованием логистической регрессии и нейронных сетей [15][16]. На сегодняшний день для оценки вероятности ИБС используют и другие методы МО: деревья решений, наивный байесовский классификатор, метод опорных векторов, k-ближайших соседей и глубокое обучение [17].
Учитывая, что поражение ЛКА ассоциировано с ростом летальности среди пациентов с ИБС, его своевременное выявление следует рассматривать как важную задачу практического здравоохранения, решение которой возможно путем модернизации диагностических подходов к верификации ишемии миокарда с применением технологий искусственного интеллекта, в частности методов МО.
Цель исследования — разработать программный комплекс, позволяющий на основе клинико-инструментальных признаков прогнозировать наличие гемодинамически значимого поражения ствола ЛКА у больных стабильной ИБС.
Материал и методы
В открытое ретроспективное исследование включались пациенты со стабильной ИБС, госпитализированные в ФГБУ «НМИЦ им. В.А. Алмазова» с января 2024 по февраль 2025 гг. для плановой КАГ. Отобраны 104 больных с гемодинамически значимым стенозом ствола ЛКА и 104 — без обструктивного поражения КА. Мужчины составили 61%, женщины — 39%. Медиана возраста пациентов — 67 лет (диапазон 62-70).
Протокол исследования был одобрен локальным этическим комитетом ФГБУ «Национальный медицинский исследовательский центр им. В. А. Алмазова" Минздрава России. Все участники подписывали информированное согласие. Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice).
Критериями исключения были: возраст младше 18 лет, острый инфаркт миокарда (ИМ), нестабильная стенокардия, активное онкологическое заболевание любой локализации.
Для решения задачи была использована база данных Exсel, содержащая информацию о 208 больных, сформированная на основе изучения историй болезни. В исследовании проанализированы данные анамнеза, объективного осмотра, лабораторных и инструментальных обследований, включая общий и биохимический анализы крови, ЭКГ, ЭхоКГ, стресс ЭхоКГ, дуплексное сканирование брахиоцефальных артерий и сосудов нижних конечностей, КАГ. Клинический и биохимический анализы крови проводились на автоматическом анализаторе с применением реактивов и контрольных материалов фирмы Roche (Швейцария). При неинвазивных исследованиях использовано оборудование General Electric (США). Селективная КАГ проводилась по стандартной методике лучевым или бедренным доступом на ангиографическом комплексе «Angioscop-3D» (Siemens, Германия). Ангиографическая оценка степени стенозов в КА осуществлялась в соответствии с рекомендациями Американского колледжа кардиологов, согласно которым значимым считали стеноз ствола ЛКА >50% [18].
Исходно база данных включала набор из 107 клинико-инструментальных признаков. На основании экспертной оценки до начала построения моделей осуществлен отбор 63 из них, которые регистрируются в медицинской карте больного в реальной практике и отражают результаты стандартного подхода диагностики ИБС согласно клиническим рекомендациям Российского кардиологического общества [19]. Из отобранных прогностических признаков было 32 бинарных, 27 числовых и 4 категориальных.
Для выделения наименее коррелированных признаков, наиболее важных и подходящих для предсказания модели, выполнено построение матрицы корреляций. В дальнейшем проведен эксперимент по постепенному исключению коррелированных признаков из обучения модели. Пары признаков с пороговым значением корреляции 0,75 были объединены в кластеры, сформированные из признаков с пересекающимися корреляциями, после чего методом RFE (recursive feature elimination — рекурсивным исключением признаков), внутри которого использовались случайные леса, были исключены наименее важные (табл. 1).
Таблица 1. Пример матрицы корреляции с маской значимости

Объединение в кластеры признаков с корреляцией выше порога позволило выбрать наиболее значимые признаки среди групп. Данный подход использовался в качестве альтернативы методу VIF (variance inflation factor — коэффициент увеличения дисперсии), предполагающему линейные взаимосвязи между признаками.
Выбор градиентного бустинга среди классических методов МО обусловлен предположением о наличии нелинейных взаимосвязей в данных. Кроме того, градиентный бустинг менее чувствителен к масштабированию признаков. На первом этапе для итоговой оценки модели была выделена тестовая выборка, которая составила 20% от исходной и не использовалась в дальнейшем на этапах валидации и подбора гиперпараметров. Базовые модели LightGBM, XGBoost и CatBoost валидировались на оставшихся данных с помощью повторной 5-фолдовой страцифицированной кросс-валидации, в рамках которой рассчитывались средние значения и доверительные интервалы метрик. Для наиболее перспективной модели CatBoost с помощью вложенной кросс-валидации с внешним и внутренним разбиением, состоящим из 4 фолдов, осуществлен подбор гиперпараметров. Учитывая отсутствие значимого улучшения метрик по сравнению с моделью с параметрами по умолчанию, для дальнейшего обучения была использована базовая конфигурация. На этом этапе доверительные интервалы не рассчитывались. Все разработанные в ходе исследования программы написаны на языке программирования Python в интегрированной среде программирования PyCharm. Для загрузки данных и работы с таблицами использовалась библиотека pandas. Сравнение эффективности моделей проводилось с использованием таких метрик, как точность, полнота, F-мера, специфичность и площадь под кривой ROC-AUC (receiver operating characteristic area under curve)1.
Точность (precision) отражает вероятность наличия патологии при её обнаружении моделью, которая вычисляется по формуле: precision = 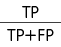 , где TP (True Positive) — истинный положительный результат, а FP (False Positive) — ложный положительный результат. Полнота (recall) показывает вероятность выявления пациентов с патологией. Этот показатель также называют чувствительностью и определяют по формуле: recall =
, где TP (True Positive) — истинный положительный результат, а FP (False Positive) — ложный положительный результат. Полнота (recall) показывает вероятность выявления пациентов с патологией. Этот показатель также называют чувствительностью и определяют по формуле: recall =  , где FN (False Negative) — ложный отрицательный результат. В качестве интегрального показателя для бинарной классификации использовали F-меру, которая представляет собой среднее гармоническое между точностью и полнотой и достигает максимума при их значениях равных единице.
, где FN (False Negative) — ложный отрицательный результат. В качестве интегрального показателя для бинарной классификации использовали F-меру, которая представляет собой среднее гармоническое между точностью и полнотой и достигает максимума при их значениях равных единице.
Специфичность (specificity) интерпретируется как вероятность того, что пациенты без патологии будут определены как здоровые. Рассчитывается по формуле: specificity = 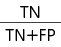 , где TN (True Negative) — истинный отрицательный результат.
, где TN (True Negative) — истинный отрицательный результат.
Результаты моделей — показатели эффективности моделей, выраженные площадью под кривой ROC-AUC, которая эквивалентна вероятности, что классификатор присвоит больший вес случайно выбранной положительной сущности, чем случайно выбранной отрицательной. Сравнение результатов моделей по целевой метрике ROC-AUC осуществлялось с помощью t-теста Стьюдента для связанных выборок. Корреляционный анализ проведен с применением коэффициента ранговой корреляции Спирмена. Уровень значимости (p) при проверке статистических гипотез в исследовании принимался <0,05.
Результаты
На основе трех реализаций алгоритма градиентного бустинга, используя 63 отобранных признака, были построены модели: LightGBM, XGBoost и CatBoost. Целевой переменной в представленном наборе данных являлся признак «стеноз ствола ЛКА». Значение «1» означало наличие гемодинамически значимого стеноза, а значение «0» — его отсутствие. Оставшиеся признаки рассматривались как независимые переменные.
Результаты тестирования трех разработанных базовых моделей классификаторов LightGBM, XGBoost и CatBoost с помощью указанных метрик, принятых в задачах классификации, приведены в табл. 2.
Таблица 2. Значения метрик качества для базовых моделей (63 признака)
|
Метрика |
LightGBM |
XGBoost |
CatBoost |
|
Точность (precision) |
0,792 (0,731-0,853) |
0,757 (0,670-0,844) |
0,753 (0,685-0,821) |
|
Полнота (recall) |
0,684 (0,506-0,862) |
0,703 (0,536-0,870) |
0,751 (0,568-0,934) |
|
F-мера |
0,726 (0,626-0,827) |
0,726 (0,602-0,851) |
0,749 (0,624-0,875) |
|
Специфичность (specificity) |
0,817 (0,736-0,897) |
0,779 (0,713-0,845) |
0,760 (0,717-0,802) |
|
ROC-AUC |
0,825 (0,730-0,920) |
0,841 (0,767-0,916) |
0,861 (0,783-0,940) |
|
Данные представлены в виде средних значений (95% доверительный интервал) |
|||
Требованиям ГОСТ Р 59921.5-2022, согласно которым значение ROC-AUC должно быть не менее 0,8, удовлетворяли все представленные модели. Таким образом, методы продемонстрировали схожие результаты, но наиболее перспективной себя показала модель CatBoost.
По данным кривых обучения, построенных для оценки эффективности дальнейшего обучения установлено, что повышение количества обучающих данных улучшает качество модели (рис. 1). Такое поведение кривых обучения свидетельствует о переобучении. Однако кривая обучения, построенная на тестовом множестве, еще не вышла на плато, и для достижения меньших значений ошибки необходимо увеличить тренировочное множество.

Рисунок 1. Кривые обучения (внизу) и валидации (вверху) модели CatBoost.
Для модели CatBoost осуществлен отбор и исключение коллинеарных признаков, что позволило отбросить 4 признака с порогом корреляции в 0,75 и оптимизировать результаты при кросс-валидации (табл. 3). По средним значениям и доверительным интервалам видно, что разброс метрик качества, за исключением точности и специфичности, стал меньше. Также наблюдалась тенденция к росту средних значений метрик, в связи с чем для дальнейшей оптимизации выбрана модель CatBoost, обученная на 59 признаках. В табл. 4 приведены результаты итогового тестирования модели CatBoost после окончательного обучения на кросс-валидационном датасете.
Таблица 3. Значения метрик качества моделей CatBoost, обученных на 63 и 59 признаках
|
Метрика |
CatBoost (63 признака) |
CatBoost (59 признаков) |
|
Точность (precision) |
0,753 (0,685-0,821) |
0,765 (0,679-0,852) |
|
Полнота (recall) |
0,751 (0,568-0,934) |
0,778 (0,691-0,865) |
|
F-мера |
0,749 (0,624-0,875) |
0,768 (0,717-0,820) |
|
Специфичность (specificity) |
0,760 (0,717-0,802) |
0,765 (0,649-0,880) |
|
ROC-AUC |
0,861 (0,783-0,940) |
0,855 (0,793-0,917) |
|
Данные представлены в виде средних значений (95% доверительный интервал) |
||
Таблица 4. Итоговые значения метрик качества для модели CatBoost
|
Метрика |
CatBoost (59 признаков) |
|
Точность (precision) |
0,767 |
|
Полнота (recall) |
0,770 |
|
F-мера |
0,765 |
|
Специфичность (specificity) |
0,769 |
|
ROC-AUC |
0,862 |
Кроме того, встроенными инструментами CatBoost удалось идентифицировать наиболее информативные и прогностически значимые признаки. К их числу отнесены пол, индекс массы тела, риск смерти от сердечно-сосудистых заболеваний в течение ближайших 10 лет по шкале SCORE (Systematic COronary Risk Evaluation), функциональный класс стенокардии, ИМ в анамнезе, хроническая сердечная недостаточность, уровень эритроцитов, лейкоцитов, калия, холестерин липопротеинов высокой плотности, холестерин липопротеинов низкой плотности и триглицеридов в плазме крови (рис. 2).

Рисунок 2. Значимые признаки, определенные встроенными инструментами CatBoost.
Обсуждение
Увеличение продолжительности и улучшение качества жизни являются основными целями медикаментозного и хирургического лечения ИБС. При этом на сегодняшний день в крупных рандомизированных исследованиях COURAGE и ISCHEMIA показано, что рутинная коронарная реваскуляризация не сопровождается снижением неблагоприятных сердечно-сосудистых событий [20][21]. Исключение составляют только пациенты со стенозом ствола ЛКА >50%, поражение которого служит абсолютным показанием к реваскуляризации миокарда, в том числе у лиц перед выполнением внесердечных хирургических вмешательств, представляющих единственную ангиографическую подгруппу с преимуществом в выживаемости от предоперационного коронарного вмешательства [22]. Это обусловлено тем, что стеноз ствола ЛКА является независимым предиктором крайне высокой летальности среди больных ИБС [23]. Так, у пациентов со стволовым поражением смертность в течение 3 лет после установления диагноза достигает 50% [24]. Стоит отметить, что по мере роста числа КАГ в связи с ИМ стали чаще выявляться значимые стенозы ЛКА без предшествующих клинических проявлений [25]. Представленные сведения свидетельствуют о чрезвычайной актуальности проблемы своевременной верификации стеноза ЛКА, а предложенный нами на основе технологий искусственного интеллекта алгоритм определяет перспективы решения задачи ранней диагностики поражения ствола ЛКА и снижения смертности в этой когорте пациентов.
В проведенном исследовании алгоритм градиентного бустинга продемонстрировал точность прогноза классификатора 86,2% на тестовом наборе данных при чувствительности и специфичности 77% и 76,9%, соответственно. В работе Р. Nuchanat и соавт. [15], посвященной прогнозированию трёхсосудистого поражения КА и стеноза ствола ЛКА, модель логистической регрессии обучалась на данных 162 пациентов с хроническим коронарным синдромом. Предварительно отобранными прогностическими признаками считали наличие СН, систолической дисфункции ЛЖ, подъема сегмента ST в отведениях aVR и V1, а также депрессию сегмента ST. Чувствительность и специфичность представленной модели составили 71,26% и 86,67%, соответственно, а значение ROC-AUC 0,855 [15]. Стоит отметить, что логистическая регрессия предполагает наличие только линейных связей внутри предикторов и между предикторами и исходами, что может повлиять на качество прогнозов [26]. Выбор алгоритма градиентного бустинга в нашем исследовании обусловлен тем, что, во-первых, он устойчив к выбросам, корреляции, пропускам, во-вторых, он не требует нормализации и стандартизации, может обрабатывать разные типы данных, чувствителен к нелинейным связям и, в-третьих, он хорошо интерпретируем [27].
В исследовании по применению нейронных сетей при выявлении ИБС, включавшем 120 пациентов, для обучения использовались 23 параметра, включая изображения ЭКГ. Модель продемонстрировала следующую эффективность: точность — 80%, чувствительность — 63%, полнота — 55%, ROC-AUC — 0,74 [16]. Таким образом, модель CatBoost не только не уступает предложенным для идентификации ИБС алгоритмам с применением логистической регрессии и нейронных сетей, а даже превосходит их по чувствительности и ROC-AUC [15][16]. Разработанный на ее основе программный комплекс определяет возможности применения метода в клинической практике для эффективной поддержки принятия врачебных решений.
Кроме того, совершенствование алгоритмов за счет набора новых данных, используемых для дальнейшего обучения модели, способно повысить статистическую значимость получаемых ответов [17]. В проведенном исследовании при построении кривых обучений наглядно показано, что расширение объема обучающих данных улучшит качество представленной модели. Также в перспективе возможно выполнить настройку порога классификации по ROC-AUC и осуществлять информирование врача об уровне вероятности принадлежности случая к определенному классу. Таким образом, специалистам будет известно о том, насколько сильно машина уверена в своих предположениях и стоит ли опираться на ее прогноз.
Использование алгоритмов МО в дополнение к общеизвестным факторам неблагоприятного течения атеросклероза, таким как курение, ожирение, гиперхолестеринемия, артериальная гипертензия и СД, позволяет выявить дополнительные неблагоприятные прогностические признаки, такие как хроническая сердечная недостаточность, снижение фракции выброса ЛЖ [5][15]. В настоящем исследовании прогностическими признаками стволового поражения ЛКА, идентифицированными моделью CatBoost, оказались пол, индекс массы тела, ХСН, уровень эритроцитов, лейкоцитов, калия, холестерин липопротеинов высокой и низкой плотности и триглицериды в плазме крови. Главными преимуществами МО, которые способствуют ранней верификации болезней системы кровообращения, являются упрощение анализа большого количества признаков и выявление важных и неочевидных взаимосвязей. При этом кластеризация признаков и изучение их совокупного влияния на процессы атерогенеза будут способствовать разработке персонифицированных лечебно-диагностических стратегий не только у пациентов со стволовым поражением ЛКА, но и для больных с атеросклерозом смежных артериальных бассейнов.
Ограничения исследования
Исследование является одноцентровым с ограниченным количеством включенных пациентов, поэтому для подтверждения отсутствия смещения результатов и возможности применения предложенной модели в клинической практике необходимо проведение многоцентровых исследований, способствующих увеличению объема обучающих данных.
Заключение
Модель выявления гемодинамически значимого стеноза ствола ЛКА у больных ИБС на основе алгоритма градиентного бустинга демонстрирует хорошую точность прогноза. Ценность представленного программного комплекса заключается в разработке универсальных функций, которые обеспечивают дальнейшее обучение модели с повышением диагностической ценности. Полученное решение может быть интегрировано в диагностический процесс в составе приложения для персонального компьютера либо веб-интерфейса, автоматически анализирующего значимые для программы признаки из электронных медицинских карт пациентов, и служить дополнительным диагностическим инструментом, обеспечивающим поддержку принятия врачебных решений и повышение качества оказываемой медицинской помощи.
Отношения и Деятельность. Исследование проведено при поддержке Национального медицинского исследовательского центра им. В. А. Алмазова.
Relationships and Activities. The study was performed with the support of the Almazov National Medical Research Center.
1. Национальный стандарт Российской Федерации ГОСТ Р 59921.5-2022 «Системы искусственного интеллекта в клинической медицине. Часть 5. Требования к структуре и порядку применения набора данных для обучения и тестирования алгоритмов» от 01.06.2022. Доступен на: https://docs.cntd.ru/document/1200183858.
Список литературы
1. GBD 2021 Causes of Death Collaborators. Global burden of 288 causes of death and life expectancy decomposition in 204 countries and territories and 811 subnational locations, 1990-2021: a systematic analysis for the Global Burden of Disease Study 2021. Lancet. 2024;403(10440):2100-2132. DOI:10.1016/S0140-6736(24)00367-2.
2. Vrints C, Andreotti F, Koskinas KC, et al. 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J. 2024;45(36):3415-3537. DOI:10.1093/eurheartj/ehae177.
3. Davidson LJ, Cleveland JC, Welt FG, et al. A Practical Approach to Left Main Coronary Artery Disease: JACC State-of-the-Art Review. J Am Coll Cardiol. 2022;80(22):2119-2134. DOI:10.1016/j.jacc.2022.09.034.
4. Virani SS, Newby LK, Arnold SV, et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA Guideline for the Management of Patients With Chronic Coronary Disease: A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2023;148(9):e9-e119. DOI:10.1161/CIR.0000000000001168.
5. Senior R, Reynolds HR, Min JK, et al. Predictors of Left Main Coronary Artery Disease in the ISCHEMIA Trial. J Am Coll Cardiol. 2022;79(7):651-661. DOI:10.1016/j.jacc.2021.11.052.
6. Liu H, Xu Z, Sun C, et al. A Variant in COX-2 Gene Is Associated with Left Main Coronary Artery Disease and Clinical Outcomes of Coronary Artery Bypass Grafting. Biomed Res Int. 2017;2017:2924731. DOI:10.1155/2017/2924731.
7. Liu R, Liu H, Gu H, et al. A Polymorphism in Hepatocyte Nuclear Factor 1 Alpha, rs7310409, Is Associated with Left Main Coronary Artery Disease. Biochem Res Int. 2014;2014:924105. DOI:10.1155/2014/924105.
8. Knuuti J, Wijns W, Saraste A, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41(3):407-477. DOI:10.1093/eurheartj/ehz425.
9. Lee GK, Hsieh YP, Hsu SW, et al. Value of ST-segment change in lead aVR in diagnosing left main disease in Non-ST-elevation acute coronary syndrome-A meta-analysis. Ann Noninvasive Electrocardiol. 2019;24(6):e12692. DOI:10.1111/anec.12692.
10. Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR Guideline for the Evaluation and Diagnosis of Chest Pain: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2021;144(22):e368-e454. DOI:10.1161/CIR.0000000000001029.
11. Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40(2):87-165. DOI:10.1093/eurheartj/ehy394.
12. Сумин А.Н. Место клинической оценки в выявлении обструктивных поражений коронарных артерий при стабильной ишемической болезни сердца. Часть I. Российский кардиологический журнал. 2019;(5):95-100. DOI:10.15829/1560-4071-2019-5-95-100.
13. Циванюк М.М., Гельцер Б.И., Шахгельдян К.И. и др. Электрокардиографические, эхокардиографические и липидные показатели в прогнозировании обструктивного поражения коронарных артерий у больных с острым коронарным синдромом без подъема сегмента ST. Российский кардиологический журнал. 2022;27(6):5036. DOI:10.15829/1560-4071-2022-5036.
14. Oise GP, Oyedotun SA, Nwabuokei OC, et al. Enhanced prediction of coronary artery disease using logistic regression. FUDMA Journal of Sciences. 2025;9(3):201-208. DOI:10.33003/fjs-2025-0903-3263.
15. Nuchanat P, Methavigul K. Predictive model for left main coronary artery or triple vessel disease in patients with chronic coronary syndromes. Asian Biomed (Res Rev News). 2024;18(4):180-185. DOI:10.2478/abm-2024-0024.
16. Абдуалимов Т.П., Обрезан А.Г. Выявление поражения коронарных артерий при помощи алгоритмов глубокого обучения. Кардиология: новости, мнения, обучение. 2021;9(2):9-13. DOI:10.33029/2309-1908-2021-9-2-9-13.
17. Garavand A, Behmanesh A, Aslani N, et al. Towards Diagnostic Aided Systems in Coronary Artery Disease Detection: A Comprehensive Multiview Survey of the State of the Art. International Journal of Intelligent Systems. 2023;4:1-19. DOI:10.1155/2023/6442756.
18. Patel MR, Calhoon JH, Dehmer GJ, et al. ACC/AATS/AHA/ASE/ASNC/SCAI/SCCT/STS 2017 Appropriate Use Criteria for Coronary Revascularization in Patients With Stable Ischemic Heart Disease: A Report of the American College of Cardiology Appropriate Use Criteria Task Force, American Association for Thoracic Surgery, American Heart Association, American Society of Echocardiography, American Society of Nuclear Cardiology, Society for Cardiovascular Angiography and Interventions, Society of Cardiovascular Computed Tomography, and Society of Thoracic Surgeons. J Am Coll Cardiol. 2017;69(17):2212-2241. DOI:10.1016/j.jacc.2017.02.001.
19. Национальный стандарт Российской Федерации ГОСТ Р 59921.5-2022 «Системы искусственного интеллекта в клинической медицине. Часть 5. Требования к структуре и порядку применения набора данных для обучения и тестирования алгоритмов» от 01.06.2022. Доступен на: https://docs.cntd.ru/document/1200183858.
20. Maron DJ, Mancini GBJ, Hartigan PM, et al. Healthy Behavior, Risk Factor Control, and Survival in the COURAGE Trial. J Am Coll Cardiol. 2018;72(19):2297-2305. DOI:10.1016/j.jacc.2018.08.2163.
21. Maron DJ, Hochman JS, Reynolds HR, et al. Initial Invasive or Conservative Strategy for Stable Coronary Disease. N Engl J Med. 2020;382(15):1395-1407. DOI:10.1056/NEJMoa1915922.
22. Thompson A, Fleischmann KE, Smilowitz NR, et al. 2024 AHA/ACC/ACS/ASNC/HRS/SCA/SCCT/SCMR/SVM Guideline for Perioperative Cardiovascular Management for Noncardiac Surgery: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2024;84(19):1869-1969. DOI:10.1016/j.jacc.2024.06.013.
23. Khawaja M, Britt M, Khan MA, et al. Left Main Coronary Artery Disease: A Contemporary Review of Diagnosis and Management. Rev Cardiovasc Med. 2024;25(2):66. DOI:10.31083/j.rcm2502066.
24. Fajadet J, Chieffo A. Current management of left main coronary artery disease. Eur Heart J. 2012;33(1):36-50b. DOI:10.1093/eurheartj/ehr426.
25. Algamal AM, Salem MA, Bedier AI, et al. Clinical and angiographic profile of left main coronary artery disease in patients with chronic coronary syndrome: a retrospective study. Egypt Heart J. 2025;77(1):17. DOI:10.1186/s43044-025-00615-5.
26. Гельцер Б.И., Циванюк М.М., Шахгельдян К.И., Рублев В.Ю. Методы машинного обучения как инструмент диагностических и прогностических исследований при ишемической болезни сердца. Российский кардиологический журнал. 2020;25(12):3999. DOI:10.15829/1560-4071-2020-3999.
27. Natekin A, Knoll A. Gradient boosting machines, a tutorial. Front Neurorobot. 2013;7:21. DOI:10.3389/fnbot.2013.00021.
Об авторах
Ю. А. КудаевРоссия
Кудаев Юрий Анатольевич
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
Н. Л. Лоховинина
Россия
Лоховинина Наталья Львовна
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
И. Т. Абесадзе
Россия
Абесадзе Инга Тенгизовна
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
М. З. Алугишвили
Россия
Алугишвили Марианна Захариевна
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
А. Н. Калиниченко
Россия
Калиниченко Александр Николаевич
Инструментальная ул., д. 2, Санкт-Петербург
А. П. Смирнова
Россия
Смирнова Анастасия Павловна
Инструментальная ул., д. 2, Санкт-Петербург
А. В. Панов
Россия
Панов Алексей Владимирович
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
Рецензия
Для цитирования:
Кудаев Ю.А., Лоховинина Н.Л., Абесадзе И.Т., Алугишвили М.З., Калиниченко А.Н., Смирнова А.П., Панов А.В. Прогнозирование поражения ствола левой коронарной артерии у больных стабильной ишемической болезнью сердца с использованием технологии искусственного интеллекта. Рациональная Фармакотерапия в Кардиологии. 2026;22(1):22-29. https://doi.org/10.20996/1819-6446-2026-3232. EDN: KDRPWZ
For citation:
Kudaev Yu.A., Lokhovinina N.L., Abesadze I.T., Alugishvili M.Z., Kalinichenko A.N., Smirnova A.P., Panov A.V. Prediction of left main coronary artery lesion in patients with stable coronary artery disease using artificial intelligence technology. Rational Pharmacotherapy in Cardiology. 2026;22(1):22-29. (In Russ.) https://doi.org/10.20996/1819-6446-2026-3232. EDN: KDRPWZ
JATS XML













































.jpg)

