Перейти к:
Легочная гипертензия в результате хронической сердечной недостаточности ишемического генеза: клинические фенотипы с учетом правожелудочково-артериального сопряжения
https://doi.org/10.20996/1819-6446-2026-3235
EDN: OPDJNM
Аннотация
Цель. Изучить клинические фенотипы с учетом правожелудочково-артериального сопряжения (ПЖАС) и прогностические факторы у пациентов с легочной гипертензией, ассоциированной с хронической сердечной недостаточностью ишемического происхождения (ЛГ-иХСН).
Материал и методы. Обследовано 69 больных с ЛГ-иХСН и разными фракциями выброса левого желудочка (ФВ ЛЖ). ЛГ считалось повышение систолического давления в легочной артерии (СДЛА) более 30 мм рт. ст. по данным трансторакальной эхокардиографии. Проводилось сопоставление вероятности ЛГ с количеством подтвержденных случаев. Произведен расчет встречаемости ЛГ-иХСН среди больных с ХСН. Оценена корреляционная связь между ПЖАС и ФВ ЛЖ. Клинические фенотипы формировались на основании значения ПЖАС, как соотношение TAPSE (амплитуда систолического движения кольца трикуспидального клапана) к СДЛА. Проанализированы неблагоприятные исходы в виде смертности от всех причин и госпитализаций в связи с декомпенсацией ХСН за 13,2±0,9 мес. наблюдения.
Результаты. В 3,3% случаев ХСН встречалась ЛГ-иХСН. Повышению СДЛА >30 мм рт.ст. соответствовало 34,8% больных с высокой вероятностью ЛГ. Увеличение ФВ ЛЖ на 10% соответствовало увеличению ПЖАС на 0,096 мм/мм рт.ст. Сформировано 3 клинических фенотипа с тяжёлым (<0,28 мм/мм рт.ст), умеренным (≥0,28 и ≤0,47 мм/мм рт.ст.) и лёгким (>0,47 мм/мм рт.ст.) разобщением ПЖАС. Тяжелое разобщение ПЖАС чаще характеризовалось выраженными клиническими проявлениями (отеки нижних конечностей 53%, асцит 21% случаев), наихудшим функциональным состоянием больных (функциональный класс ЛГ III в 79% случаев), низкой толерантностью к физической нагрузке (расстояние теста шестиминутной ходьбы 267,2±107,4 м), а также наиболее продолжительным стационарным лечением (9,9±4,9 койко-дней). Тяжелое разобщение ПЖАС в 67% случаев соответствовало высокой вероятности ЛГ. Между клиническими фенотипами отсутствовало различие во времени наступления неблагоприятных исходов. ПЖАС ≤0,47 и ≤0,28 мм/мм рт.ст., СДЛА ≥40 мм рт.ст., TAPSE ≤18 мм, площадь правого предсердия ≥18 см2 и поперечный размер правого желудочка ≥3,5 см являлись предикторами неблагоприятного прогноза при ЛГ-иХСН.
Заключение. ПЖАС может быть использован как клинико-функциональный предиктор течения заболевания и неблагоприятных исходов у пациентов с ЛГ-иХСН.
Ключевые слова
Для цитирования:
Мареева В.А., Клименко А.А. Легочная гипертензия в результате хронической сердечной недостаточности ишемического генеза: клинические фенотипы с учетом правожелудочково-артериального сопряжения. Рациональная Фармакотерапия в Кардиологии. 2026;22(1):37-44. https://doi.org/10.20996/1819-6446-2026-3235. EDN: OPDJNM
For citation:
Mareyeva V.A., Klimenko A.A. Pulmonary hypertension due to chronic heart failure of ischemic genesis: clinical phenotypes determined by the right ventricular-pulmonary artery coupling. Rational Pharmacotherapy in Cardiology. 2026;22(1):37-44. (In Russ.) https://doi.org/10.20996/1819-6446-2026-3235. EDN: OPDJNM
Введение
Легочная гипертензия (ЛГ) является распространенным следствием длительной гемодинамической перегрузки левых отделов сердца при хронической сердечной недостаточности (ХСН) различной этиологии. Перегрузка левых отделов сердца при систолической и/или диастолической дисфункции ЛЖ запускает каскад анатомических и функциональных изменений легочного русла, что в конечном итоге приводит к дисфункции правого желудочка (ПЖ) и его недостаточности, а это, в свою очередь, повышает риски госпитализаций и смертности у больных с ХСН [1][2]. По последним данным, во всем мире 64,3 миллиона людей страдают сердечной недостаточностью [3], при этом в развитых странах ее частота встречаемости составляет 1-2% от общей численности взрослого населения [4]. В связи с прогрессирующим неблагоприятным течением одного из распространенных сердечно-сосудистых заболеваний мира, ЛГ сформировавшаяся на фоне ХСН, в настоящий момент является одной из актуальных тем современных исследований. В то же время, такие работы, как правило, посвящены различным формам ХСН, где оцениваются группы со сниженной фракцией выброса (ФВ) левого желудочка (ЛЖ) против сохраненной [5]. Изучение правожелудочково-артериального сопряжения (ПЖАС), системы, отражающей состояние баланса между ПЖ и легочной артерией (ЛА) [6], у больных с ЛГ и ХСН, часто проводят с помощью инвазивных методов исследования [7].
Однако работы по неинвазивной оценке ПЖАС в группе ЛГ, ассоциированной с ХСН ишемического генеза (ЛГ-иХСН) с различной ФВ ЛЖ не встречаются. Цель исследования — изучить клинико-функциональное состояние больных, провести сравнительный анализ клинических фенотипов на основании ПЖАС, а также изучить прогноз пациентов с ЛГ-иХСН.
Материал и методы
В течение трех лет из 2110 больных ХСН различной этиологии с разной ФВ ЛЖ в возрасте от 45 лет, поступивших в кардиологическое и терапевтическое отделения, было проанализировано и отобрано 80 пациентов (3,8%) с ЛГ. Из них в исследование было включено 69 больных (86,3%) с ЛГ-иХСН. За наличие ЛГ было принято повышение систолического давления в легочной артерии (СДЛА) >30 мм рт.ст. по данным трансторакальной эхокардиографии (ЭхоКГ). После отбора данные ЭхоКГ пациентов были сопоставлены критериям вероятности ЛГ, на основании пиковой скорости трикуспидальной регургитации и дополнительных ЭхоКГ признаков перегрузки правых отделов сердца [8]. ХСН была диагностирована исходя из клинической картины, жалоб, систолической (ФВ ЛЖ) и/или диастолической дисфункции ЛЖ (E/A и E/e’, где E — фаза быстрого раннего наполнения левого желудочка, A — фаза сокращения предсердий, е’ — ранняя диастолическая волна) в сочетании с повышением уровня N-концевого промозгового натрийуретического пептида (NT-proBNP) >125 пг/мл. Ишемическому генезу ХСН соответствовали перенесенный >3 мес. назад инфаркт миокарда, или поражение как минимум одной коронарной артерии >70% согласно данным коронароангиографии, или проведенная ранее реваскуляризация. Стадия ХСН устанавливалась с помощью классификации Н. Д. Стражеско, В. Х. Василенко (1935 г.) на момент актуальных клинических рекомендаций по ХСН от 2020 г. [9]. Критерии невключения: ЛГ вследствие бронхолегочной патологии, клапанных пороков сердца, эпизодов перенесенной тромбоэмболии ЛА, системных заболеваний соединительной ткани, неишемическое поражение сердца, острое нарушение мозгового кровообращения и перенесенный инфаркт миокарда давностью <3 мес., лечение по поводу онкологического заболевания, анемия средней и тяжелой степени, цирроз печени класса В и С по Чайлд-Пью, хроническая болезнь почек стадии 4-5 стадии.
Протокол исследования был одобрен этическим комитетом ФГАОУ ВО РНИМУ им. Н. И. Пирогова Минздрава России. Все пациенты подписали добровольное информированное согласие. Исследование проведено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации.
Больным было проведено стандартное комплексное обследование (физикальный осмотр, лабораторное обследование, включая NT-proBNP (44 пациента), электрокардиография, рентгенография или компьютерная томография органов грудной клетки, спирометрия) после стабилизации состояния через 1 мес. после выписки из стационара. Всем пациентам на аппаратах GE Healthcare Vivid E95 или Philips EPIQ 7 проводилась ЭхоКГ экспертного уровня с дополнительной оценкой ПЖАС в виде индекса систолической функции правого желудочка TAPSE (tricuspid annular plane systolic excursion)/СДЛА (мм/мм рт.ст.).
Прогностическая оценка проводилась путем анализа наступления комбинированной конечной точки (повторная госпитализация по причине декомпенсации ХСН или смерти от любых причин) у больных с ЛГ-иХСН в течение 13,2±0,9 мес. наблюдения.
Статистический анализ выполнялся с помощью программы Statistica 12. Проверка нормальности осуществлялась по критерию Шапиро-Уилка. Группы сравнивали дисперсионным анализом с тестом Тьюки (при нормальном распределении), либо H-критерием Краскела-Уоллиса с Z-тестом Данна (при ненормальном распределении). Оценка различий в таблицах сопряженности проводилась с применением критериев χ² Пирсона и точного критерия Фишера. Корреляционная связь определялась коэффициентом Спирмена (rs). Кластерный метод k-средних использован для формирования клинических фенотипов ЛГ-иХСН. Анализ выживаемости проводился с помощью построения кривых Каплана-Мейера и попарного сравнительного лог-рангового анализа. Параметры риска неблагоприятных исходов выявлены посредством ROC-анализа. Различия считали статистически значимыми при p<0,05.
Результаты
В исследование включено 69 больных с ЛГ-иХСН, среди которых было 44 мужчины и 25 женщин (средний возраст 70±10 лет, индекс массы тела 27,6±5 кг/м²). У 94,2% пациентов фоновым заболеванием была артериальная гипертензия, в то время как фибрилляция предсердий встречалась в 59,4% случаев (рис. 1а). С помощью спирометрии у обследованных больных были исключены обструктивные нарушения. Медикаментозная терапия пациентов (рис. 1b) основывалась на действующих клинических рекомендациях по ХСН на период с 2021 по 2023 гг., что определяло низкий процент применения препаратов группы ингибиторов натрий-глюкозного котранспортера 2-го типа (иSGLT2). При сопоставлении пациентов с СДЛА >30 мм рт. ст. с вероятностными шкалами оценки риска ЛГ, только 34,8% больных соответствовало наличию высокой ее вероятности.

Рисунок 1a. Сопутствующие заболевания у пациентов с ЛГ-иХСН (n=69)
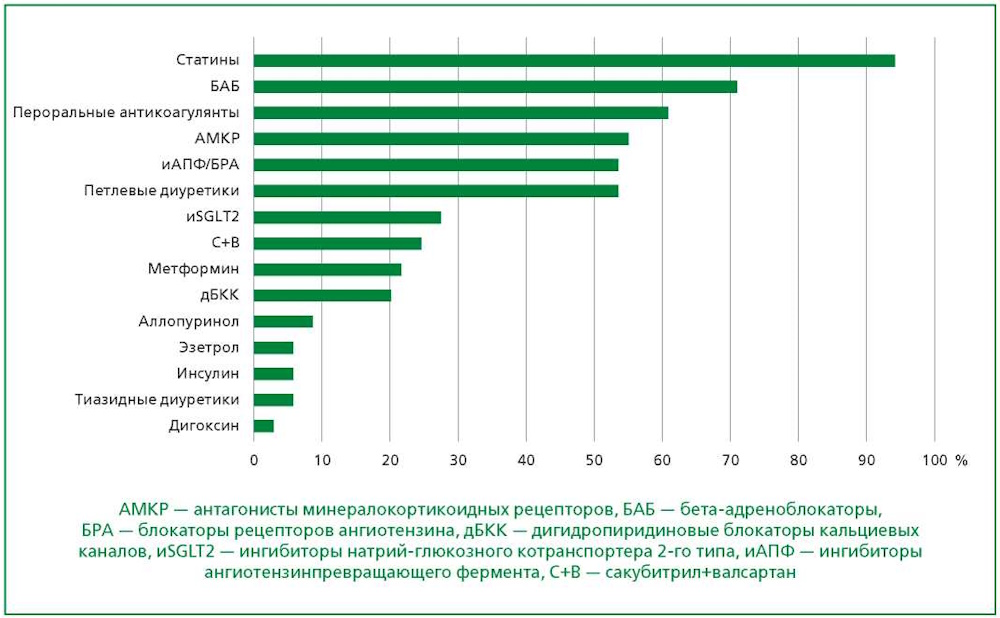
Рисунок 1b. Медикаментозная терапия пациентов с ЛГ-иХСН (n=69)
При ЛГ-иХСН, между ФВ ЛЖ и ПЖАС была обнаружена положительная корреляционная связь (rs=0,31; p=0,01) (рис. 2). По данным линейного регрессионного анализа увеличение ФВ ЛЖ на 10% соответствовало увеличению ПЖАС в среднем на 0,096 мм/мм рт. ст. (среднее значение ± стандартная ошибка (B±SE) = 0,0096±0,0006; p<0,001; R²=78,5%).

Рисунок 2. Корреляция фракции выброса левого желудочка и правожелудочково-артериального сопряжения
На основании степени разобщения системы ПЖ-ЛА кластерным анализом методом k-средних были сформированы 3 клинических фенотипа ЛГ-иХСН с: тяжелым (<0,28 мм/ мм рт.ст), умеренным (≥0,28 и ≤0,47 мм/ мм рт.ст.) и легким разобщением ПЖАС (>0,47 мм/мм рт.ст.). Результаты сравнительного анализа клинических фенотипов представлены в табл. 1.
Таблица 1. Сравнительный анализ клинических фенотипов пациентов с ЛГ-иХСН в зависимости от правожелудочково-артериального сопряжения
|
Показатель |
Легкое разобщение (ПЖАС >0,47 мм/мм рт.ст.)¹ n=19 |
Умеренное разобщение (ПЖАС ≥0,28 и ≤0,47 мм/мм рт.ст.)² n=28 |
Тяжелое разобщение (ПЖАС <0,28 мм/мм рт.ст.)³ n=22 |
P |
|
Стадия ХСН I стадии, n (%) |
3 (14) |
0 |
0 |
0,31¹-² |
|
Стадия ХСН IIA стадии, n (%) |
13 (59) |
9 (32) |
3 (16) |
|
|
Стадия ХСН IIБ стадии, n (%) |
6 (27) |
19 (68) |
16 (84) |
|
|
Одышка, n (%) |
21 (95) |
26 (93) |
18 (95) |
1¹-² |
|
Отеки нижних конечностей, n (%) |
4 (18) |
19 (68) |
10 (53) |
0,365¹-² |
|
Асцит, n (%) |
0 |
1 (4) |
4 (21) |
0,142¹-² |
|
ФК ЛГ I, n (%) |
3 (14) |
1 (4) |
0 |
0,214¹-² |
|
ФК ЛГ II, n (%) |
16 (73) |
11 (39) |
4 (21) |
|
|
ФК ЛГ III, n (%) |
3 (14) |
16 (57) |
15 (79) |
|
|
ФВ ЛЖ, % |
49,4±11,4 |
41,2±11,6 |
39,1±11,4 |
0,842¹-² |
|
ПЖАС, мм/мм рт.ст. |
0,674±0,249 |
0,381±0,05 |
0,218±0,034 |
<0,001¹-² |
|
СДЛА, мм рт.ст. |
32,3±7,6 |
45,8±6,9 |
64,7±9,5 |
<0,001¹-² |
|
TAPSE, мм |
20,1±2,2 |
17,2±2 |
13,9±1,7 |
<0,001¹-² |
|
Площадь ПП, см² |
17,5±4,7 |
21,2±5 |
25±8 |
0,578¹-² |
|
Поперечный размер ПЖ, см |
2,95±0,5 |
3,39±0,59 |
4,08±0,88 |
0,005¹-² |
|
НПВ, см |
1,65±0,29 |
1,88±0,3 |
2,36±0,5 |
<0,001¹-² |
|
1 степень МР |
15 (68%) |
7 (25%) |
6 (32%) |
0,219¹-² |
|
1-2 степень МР |
4 (18%) |
11 (39%) |
4 (21%) |
|
|
2-3 степень МР |
1 (5%) |
0 |
3 (16%) |
|
|
NT-proBNP, пг/мл |
552±732 |
9752±12688 |
4678±3195 |
1¹-² |
|
Расстояние Т6МХ, м |
368,1±117,9 |
288,3±113,4 |
267±107,4 |
1¹-² 0,018¹-³ 0,058²-³ |
|
Койко-дни |
7,6±1,7 |
7,1±2,3 |
9,9±4,9 |
0,013¹-² 0,373¹-³ 0,598²-³ |
|
МР — митральная регургитация, НПВ — нижняя полая вена, ПЖ — правый желудочек, ПЖАС — правожелудочково-артериальное сопряжение, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, Т6МХ — тест шестиминутной ходьбы, ФВ ЛЖ — фракция выброса левого желудочка, ФК — функциональный класс, ХСН — хроническая сердечная недостаточность, NT-proBNP — N-концевой промозговой натрийуретический пептид, TAPSE — амплитуда систолического движения кольца трикуспидального клапана |
||||
Определено, что легкое разобщение ПЖАС соответствовало низкой вероятности ЛГ (64%, p=0,028), умеренное разобщение — средней (65%, p<0,001), а тяжелое — высокой вероятности ЛГ (67%, p<0,001).
Фенотип с тяжелым разобщением ПЖАС демонстрировал наиболее выраженные клинические проявления, низкую толерантностью к физическим нагрузкам, наименьшее пройденное расстояние теста шестиминутной ходьбы, тяжелую перегрузку правых отелов сердца со значимым приростом NT-proBNP, наихудшую систолическую функцию ЛЖ с тяжелой степенью митральной регургитации, а также продолжительное пребывание на стационарном лечении (p<0,05). При умеренном разобщении ПЖАС, концентрация NT-proBNP была наибольшей (8696±10493 пг/мл при наличии хронической болезни почек vs 3228±7144 пг/мл при ее отсутствии; p=0,011), что было обусловлено более частым наличием в анамнезе хронической болезни почек (скорость клубочковой фильтрации при умеренном разобщении ПЖАС 61,2±17,6 vs 71,5±19,2 и 62,7±16,2 мл/мин/1,73 м² при легком и умеренном разобщении, соответственно).
Оценка долгосрочных исходов проводилась на основе анализа полученных данных 50 больных, которые продолжили участие в исследовании. За период наблюдения (13,2±0,9 мес.) комбинированная конечная точка наблюдалась у 22 пациентов: 2 летальных исхода (тромбоэмболия ЛА и внезапная сердечная смерть) и 20 случаев декомпенсации ХСН. По данным сравнительного анализа выживаемости с построением кривых Каплана-Мейера, время наступления неблагоприятных исходов между клиническими фенотипами за весь период наблюдения не различалось (p>0,05). С помощью ROC-анализа были определены пороговые значения СДЛА ≥40 мм рт.ст. (площадь под кривой (AUC)=0,722, 95% доверительный интервал (ДИ): 0,581-0,863; p=0,002), TAPSE ≤18 мм (AUC=0,702, 95% ДИ: 0,559-0,845; p=0,006), площади правого предсердия ≥18 см² (AUC = 0,7, 95% ДИ: 0,553-0,847; p=0,008) и поперечного размера ПЖ ≥3,5 см (AUC=0,8, 95% ДИ: 0,673-0,927; p <0,001), прогнозирующих неблагоприятный исход в течение всего периода наблюдения. Две точки отсечения ПЖАС ≤0,47 и ≤0,28 мм/мм рт.ст. (AUC=0,728, 95% ДИ: 0,589-0,867; p=0,001) также имели прогностическую значимость у больных с ЛГ-иХСН. С помощью анализа отношения шансов по наступлению комбинированной конечной точки в течение 13,2±0,9 мес. наблюдения, установлено, что, среди прочих ЭхоКГ параметров, снижение TAPSE ≤18 мм повышало риск развития неблагоприятных событий в 11,54 раза (p<0,05), внося наиболее значимый вклад в определение негативных исходов у пациентов с ЛГ-иХСН (табл. 2).
Таблица 2. ЭхоКГ предикторы развития неблагоприятных исходов у больных с ЛГ-иХСН
|
Параметр |
Наличие исхода, n (%) |
Отсутствие исхода, n (%) |
P |
OR [CI] |
|
|
ПЖ, см |
<3,5 |
7 (32) |
23 (82) |
<0,001 |
9,86 [ 2,64; 36,87] |
|
≥3,5 |
15 (68) |
5 (18) |
|||
|
ПЖАС, мм/мм рт.ст. |
>0,28 |
13 (59) |
24 (86) |
0,033 |
4,15 [ 1,07; 16,14] |
|
≤0,28 |
9 (41) |
4 (14) |
|||
|
ПЖАС, мм/мм рт.ст. |
>0,47 |
3 (14) |
13 (46) |
0,017 |
5,49 [ 1,32; 22,85] |
|
≤0,47 |
19 (86) |
15 (54) |
|||
|
ПП, см² |
<18 |
3 (14) |
15 (54) |
0,007 |
7,31 [ 1,76; 30,42] |
|
≥18 |
19 (86) |
13 (46) |
|||
|
СДЛА, мм рт.ст. |
<40 |
3 (14) |
16 (57) |
0,003 |
8,44 [ 2,02; 35,26] |
|
≥40 |
19 (86) |
12 (43) |
|||
|
TAPSE, мм |
>18 |
2 (9) |
15 (54) |
0,001 |
11,54 [ 2,26; 59,03] |
|
≤18 |
20 (91) |
13 (46) |
|||
|
ПЖ — правый желудочек, ПЖАС — правожелудочково-артериальное сопряжение, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, OR [CI] — odds ratio и confidence interval, TAPSE — амплитуда систолического движения кольца трикуспидального клапана |
|||||
Обсуждение
В литературе продемонстрировано, как вне зависимости от уровня ФВ ЛЖ, худшее клиническое течение и прогноз наблюдались у пациентов с более выраженной дисфункцией ПЖ [10], и меньшим значением ПЖАС [11][12]. В то же время, по данным других исследований, уровень ПЖАС взаимосвязан со значением ФВ ЛЖ так, что дисфункция ЛЖ сопровождалась угнетением работы ПЖ с разобщением ПЖ-ЛА. Так, например, при острой сердечной недостаточности, больные с ПЖАС менее 0,49 мм/мм рт.ст. имеют значительно большие объемы ЛЖ, а также худшую систолическую и диастолическую функцию ЛЖ по сравнению с теми, у кого ПЖАС больше [12]. Значительное повышение СДЛА у больных с ЛГ-иХСН вероятно обусловлено тяжелым течением ХСН. Так, по нашим данным именно у фенотипа с выраженным разобщением ПЖАС и наиболее высокими показателями СДЛА, отмечалась наихудшая систолическая функция ЛЖ. Ранее было доказано существование бивентрикулярного взаимодействия, поддерживающего адекватную адаптационную насосную функцию сердца [13].
В поддержку ценности формирования клинических фенотипов при ЛГ-иХСН, результатами различных исследований продемонстрировано, как низкий уровень ПЖАС характеризуется худшим клиническим, гемодинамическим состоянием больного, тяжелыми функциональными нарушениями не только правых [14], но и левых отделов сердца. В работе V. Anastasiou и соавт. разобщение ПЖАС сопровождалось двухкратным повышением риска неблагоприятных исходов [16]. В то же время нет общепринятой точки отсечения, отражающей точное начало разобщения системы ПЖ-ЛА при разных формах ЛГ. Так, ПЖАС <0,55 мм/мм рт.ст. используется как дополнительный критерий определения вероятности наличия ЛГ [8]. Для легочной артериальной гипертензии и хронической тромбоэмболической ЛГ, снижение ПЖАС <0,31 мм/мм рт.ст., сопровождалось повышением риска неблагоприятного прогноза [7]. В работе C. Falletta и соавт., при изучении больных ХСН было выявлено, как риск смерти снижался в 3 раза при значениях ПЖАС ≥0,36 мм/мм рт.ст. [17]. ПЖАС <0,62 мм/мм рт.ст., R. Badagliacca и соавт., использовали в качестве индикатора ЛГ у пациентов с ХСН и сохраненной ФВ ЛЖ [18].
При включении пациентов с повышенным значением СДЛА, лишь часть соответствовала критериям высокой вероятности наличия ЛГ, что может свидетельствовать об ограничении и возможных неточностях вероятностных шкал, а также о недостатках неинвазивной диагностики установления диагноза ЛГ. Однако исследование ПЖАС расширяет диагностические возможности ЭхоКГ, поскольку нарушения в кардиопульмональной системе могут развиваться задолго до формирования ЛГ даже при ХСН с сохраненной ФВ ЛЖ, что было продемонстрировано в экспериментальном исследовании G. Hubesch и соавт. в 2024 г. [19].
Полученные в проведенном исследовании прогностические пороговые значения для TAPSE (18 мм) и площади правого предсердия (18 см²) включены в актуальные клинические рекомендации по ЛГ и ассоциированы с высоким риском смертности и неблагоприятных исходов при снижении TAPSE ниже и увеличении площади ПП выше указанного уровня [20]. Увеличение поперечного размера ПЖ или его дилатация [21] и нарастание СДЛА [22], также связаны с увеличением вероятности неблагоприятных исходов у больных ХСН. По данным литературы, значение ПЖАС определяет время наступления неблагоприятных событий при ЛГ [23][24], однако в настоящей работе такая связь не выявлена, вероятно, вследствие непродолжительного срока наблюдения. Так, в исследовании M. Ono и соавт., получение статистически значимых результатов стало возможным при наблюдении больных более 3 лет [25].
Таким образом, необходимы дальнейшие масштабные клинические исследования пациентов с различными формами ЛГ для установления точного порогового уровня разобщения ПЖАС, а долгосрочный проспективный анализ будет способствовать разработке многомерной модели прогнозирования неблагоприятных исходов.
Ограничения исследования: малая выборка больных и срок наблюдения для оценки анализа выживаемости.
Заключение
Определение клинического фенотипа у пациентов с ЛГ-иХСН на основании ПЖАС дает более углубленное представление о клинико-функциональном статусе больного. Изучение фенотипов в перспективе может позволить определить течение заболевания, прогнозировать переносимость физических нагрузок и возможные неблагоприятные исходы, а также адаптировать терапевтические стратегии в зависимости от степени разобщения ПЖАС.
Отношения и Деятельность. Исследование проведено при поддержке ФГАОУ ВО РНИМУ им. Н. И. Пирогова Минздрава России.
Relationships and Activities. The study was conducted with the support of the Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation.
Список литературы
1. Ghio S, Guazzi M, Scardovi AB, et al.; all investigators. Different correlates but similar prognostic implications for right ventricular dysfunction in heart failure patients with reduced or preserved ejection fraction. Eur J Heart Fail. 2016;19(7):873-9. DOI:10.1002/ejhf.664.
2. Gorter TM, Hoendermis ES, van Veldhuisen DJ, et al. Right ventricular dysfunction in heart failure with preserved ejection fraction: a systematic review and meta-analysis. Eur J Heart Fail. 2016;18(12):1472-87. DOI:10.1002/ejhf.630.
3. GBD 2017 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2018;392(10159):1789-858. DOI:10.1016/S0140-6736(18)32279-7. Erratum in: Lancet. 2019;393(10190):e44. DOI:10.1016/S0140-6736(19)31047-5.
4. Smeets M, Vaes B, Mamouris P, et al. Burden of heart failure in Flemish general practices: a registry-based study in the Intego database. BMJ Open. 2019;9(1):e022972. DOI:10.1136/bmjopen-2018-022972.
5. Deaconu S, Deaconu A, Scarlatescu A, et al. Right ventricular-arterial coupling — A new perspective for right ventricle evaluation in heart failure patients undergoing cardiac resynchronization therapy. Echocardiography. 2021;38(7):1157-64. DOI:10.1111/echo.15096.
6. Мареева В.А., Клименко А.А., Шостак Н.А. Хроническая сердечная недостаточность и легочная гипертензия: трудности оценки прогноза и возможные решения. Рациональная Фармакотерапия в Кардиологии 2023;19(1):71-6. DOI:10.20996/1819-6446-2023-01-01.
7. Tello K, Wan J, Dalmer A, et al. Validation of the Tricuspid Annular Plane Systolic Excursion/Systolic Pulmonary Artery Pressure Ratio for the Assessment of Right Ventricular-Arterial Coupling in Severe Pulmonary Hypertension. Circ Cardiovasc Imaging. 2019;12(9):e009047. DOI:10.1161/CIRCIMAGING.119.009047.
8. Humbert M, Kovacs G, Hoeper MM, et al.; ESC/ERS Scientific Document Group. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Respir J. 2023;61(1):2200879. DOI:10.1183/13993003.00879-2022.
9. Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(11):4083. DOI:10.15829/1560-4071-2020-4083
10. Чучалин А.Г. Правожелудочковая сердечная недостаточность. Пульмонология. 2019;29(2):135-47. DOI:10.18093/0869-0189-2019-29-2-135-147.
11. Palazzuoli A, Cartocci A, Pirrotta F, et al. Different right ventricular dysfunction and pulmonary coupling in acute heart failure according to the left ventricular ejection fraction. Prog Cardiovasc Dis. 2023;81:89-97. DOI:10.1016/j.pcad.2023.07.008.
12. Anastasiou V, Papazoglou AS, Moysidis DV, et al. The prognostic impact of right ventricular-pulmonary arterial coupling in heart failure: a systematic review and meta-analysis. Heart Fail Rev. 2024;29(1):13-26. DOI:10.1007/s10741-023-10341-2.
13. Guazzi M, Pepi M, Maltagliati A, et al. How the two sides of the heart adapt to graded impedance to venous return with head-up tilting. J Am Coll Cardiol. 1995;26(7):1732-40. DOI:10.1016/0735-1097(95)00370-3.
14. Исламова М.Р., Лазарев П.В., Сафарова А.Ф., Кобалава Ж.Д. Эхокардиографические возможности оценки функции правого желудочка и правожелудочково-артериального сопряжения при хронической сердечной недостаточности. Кардиология: Новости, Мнения, Обучение. 2018;6(3):51-8. DOI:10.24411/2309-1908-2018-13004.
15. Pestelli G, Fiorencis A, Trevisan F, et al. New measures of right ventricle-pulmonary artery coupling in heart failure: An all-cause mortality echocardiographic study. Int J Cardiol. 2021;329:234-41. DOI:10.1016/j.ijcard.2020.12.057.
16. Anastasiou V, Daios S, Moysidis DV, et al. Right ventricular-pulmonary arterial coupling in patients with first acute myocardial infarction: an emerging post-revascularization triage tool. Hellenic J Cardiol. 2024:S1109-9666(24)00139-8. DOI:10.1016/j.hjc.2024.07.002.
17. Falletta C, Clemenza F, Klersy C, et al. Additive Value of Biomarkers and Echocardiography to Stratify the Risk of Death in Heart Failure Patients with Reduced Ejection Fraction. Cardiol Res Pract. 2019;2019:1824816. DOI:10.1155/2019/1824816.
18. Badagliacca R, Ghio S, Manzi G, Vizza CD. Right Ventricular/Pulmonary Artery Coupling in Patients With Heart Failure With Preserved Ejection Fraction: A Clue for Pulmonary Hypertension? J Am Heart Assoc. 2024;13(1):e032639. DOI:10.1161/JAHA.123.032639.
19. Hubesch G, Dewachter C, Chomette L, et al. Early Alteration of Right VentriclePulmonary Artery Coupling in Experimental Heart Failure With Preserved Ejection Fraction. J Am Heart Assoc. 2024;13(11):e032201. DOI:10.1161/JAHA.123.032201.
20. Авдеев С. Н., Барбараш О. Л., Валиева З. С. и др. Легочная гипертензия, в том числе хроническая тромбоэмболическая легочная гипертензия. Клинические рекомендации 2024. Российский кардиологический журнал. 2024;29(11):6161. DOI:10.15829/1560-4071-2024-6161
21. Galloo X, Stassen J, Hirasawa K, et al. Prognostic Implications of Right Ventricular Size and Function in Patients Undergoing Cardiac Resynchronization Therapy. Circ Arrhythm Electrophysiol. 2023;16(2):e011676. DOI:10.1161/CIRCEP.122.011676.
22. Ушакова Н.С., Ершов Е.С., Щербакова С.Д. и др. Легочная гипертензия у пожилых пациентов с хронической сердечной недостаточностью. Медицинский Алфавит. Современная Поликлиника. 2020;(2):60.
23. Tello K, Axmann J, Ghofrani HA, et al. Relevance of the TAPSE/PASP ratio in pulmonary arterial hypertension. Int J Cardiol. 2018;266:229-35. DOI:10.1016/j.ijcard.2018.01.053.
24. Wang N, Rueter P, Ng M, et al. Echocardiographic predictors of cardiovascular outcome in heart failure with preserved ejection fraction. Eur J Heart Fail. 2024;26(8):1778-87. DOI:10.1002/ejhf.3271.
25. Ono M, Suzuki A, Yoshida A, et al. HIJ-HF III study, Prognostic role of right ventricular-pulmonary artery coupling assessed by TAPSE/PASP ratio in patients with heart failure and mildly reduced ejection fraction, Eur Heart J. 2024;45 (Supplement):1, ehae666.858. DOI:10.1093/eurheartj/ehae666.858.
Об авторах
В. А. МарееваРоссия
Мареева Варвара Андреевна
125124, 1-я Ямского Поля ул., 15, строение 4
А. А. Клименко
Россия
Клименко Алеся Александровна Москва, 117513, ул. Островитянова д. 1 Москва, 119049, Ленинский пр-кт, д. 8.
Рецензия
Для цитирования:
Мареева В.А., Клименко А.А. Легочная гипертензия в результате хронической сердечной недостаточности ишемического генеза: клинические фенотипы с учетом правожелудочково-артериального сопряжения. Рациональная Фармакотерапия в Кардиологии. 2026;22(1):37-44. https://doi.org/10.20996/1819-6446-2026-3235. EDN: OPDJNM
For citation:
Mareyeva V.A., Klimenko A.A. Pulmonary hypertension due to chronic heart failure of ischemic genesis: clinical phenotypes determined by the right ventricular-pulmonary artery coupling. Rational Pharmacotherapy in Cardiology. 2026;22(1):37-44. (In Russ.) https://doi.org/10.20996/1819-6446-2026-3235. EDN: OPDJNM
JATS XML













































.jpg)

