Перейти к:
N-ацетилцистеин в профилактике контраст-индуцированного острого почечного повреждения: систематический обзор и мета-анализ рандомизированных контролируемых клинических исследований
https://doi.org/10.20996/1819-6446-2022-08-10
Аннотация
Цель. Провести анализ опубликованных рандомизированных контролируемых клинических исследований для оценки влияния N-ацетилцистеина на частоту развития контраст-индуцированного острого почечного повреждения (КИ-ОПП).
Материал и методы. Мета-анализ выполнен в соответствии с рекомендациями PRISMA на основании поиска существующей литературы в базе данных PubMed/MEDLINE за период с 2015 г. по 16 февраля 2022 г. Ключевые слова включали MeSH термины «acute kidney injury», или «contrast-induced nephropathy», или «AKI», или «CIN» и «contrast media» и «N-acetylcysteine». Для оценки систематической ошибки исследований использовали RoB2 tool.
Результаты. При поиске на основе изначально избранной стратегии отобрано 98 публикаций, часть из них была исключена из анализа в связи с несоответствием критериям включения в данный мета-анализ, в итоге были включены 7 исследований не имеющих критериев исключения, общее количество пациентов в которых составило 10394. Результаты мета-анализа показали, что у пациентов, получавших N-ацетилцистеин, КИ-ОПП развивалось с такой же частотой, как и у пациентов, которые не получали такой терапии в качестве меры профилактики развития данного осложнения (отношение шансов 1,06, 95% доверительный интервал 0,91-1,23; p=0,46).
Заключение. Использование N-ацетилцистеина не дает каких-либо преимуществ в снижении частоты КИ-ОПП по сравнению с введением солевых растворов (натрия гидрокарбонат или натрия хлорид 0,9%) или плацебо.
Ключевые слова
Для цитирования:
Межонов Е.М., Вялкина Ю.А., Шалаев С.В. N-ацетилцистеин в профилактике контраст-индуцированного острого почечного повреждения: систематический обзор и мета-анализ рандомизированных контролируемых клинических исследований. Рациональная Фармакотерапия в Кардиологии. 2022;18(4):455-461. https://doi.org/10.20996/1819-6446-2022-08-10
For citation:
Mezhonov E.M., Vyalkina Yu.A., Shalaev S.V. N-acetylcysteine in the Prevention of Contrast-induced Acute Kidney Injury: a Systematic Review and Meta-analysis of Randomized Controlled Clinical Trials. Rational Pharmacotherapy in Cardiology. 2022;18(4):455-461. (In Russ.) https://doi.org/10.20996/1819-6446-2022-08-10
Введение
Обеспокоенность по поводу того, что йодсодержащие рентгеноконтрастные средства вызывают контраст-индуцированное острое почечное повреждение (КИ-ОПП), является повсеместной, и уже более полувека влияет на принятие клинических решений, связанных с диагностической визуализацией и терапевтическими вмешательствами [1]. Рентгеноконтрастные методы диагностики и лечения широко используются в современной кардиологии; так, чрескожные коронарные вмешательства (ЧКВ) стали методом выбора в лечении как хронической ишемической болезни сердца, так и острого коронарного синдрома. Поскольку у пациентов с КИ-ОПП не существует эффективных терапевтических мер, кроме заместительной почечной терапии, в медицинском сообществе растет понимание необходимости применения профилактических мероприятий у пациентов из группы повышенного риска [2]. КИ-ОПП часто выявляется у пациентов уже с острым заболеванием, и понятно, что в этих случаях проведение первичной профилактики невозможно. Однако ситуации, в которых плановые клинические вмешательства или воздействия подвергают пациентов риску КИОПП, предоставляют возможности для изменения факторов, способствующих развитию и прогрессированию КИ-ОПП [3]. Существуют сценарии, в которых введение рентгеноконтрастных средств неизбежно, к одному из частных случаев данного сценария относится острый коронарный синдром и предполагаемый риск введения рентгеноконтрастных средств вызвал повышенный интерес к мерам профилактики КИ-ОПП. Была создана целая область исследования, направленная на их выявление и оценку. На это направление исследований было выделено огромное количество средств, и очень большое количество пациентов подверглось исследуемым вмешательствам, включая N-ацетилцистеин, бикарбонат натрия, жидкостную нагрузку, статины, витамин С, вазоактивные препараты, теофиллин, прекондиционирующую ишемию и заместительную почечную терапия, но ни один из них не лишен побочных эффектов [4]. Помимо перипроцедурной гидратации, которая, по-видимому, снижает, но не полностью предотвращает риск повреждения почек после введения рентгеноконтрастных средств, результаты применения других препаратов, таких как дофамин, маннит, Nацетилцистеин и каптоприл, аллопуринол неоднозначны [5-7]. В клинических рекомендациях KDIGO по ОПП с целью профилактики КИ-ОПП наряду с внутривенным восполнением объема циркулирующей крови физиологическим раствором натрия хлорида или растворами натрия бикарбоната рекомендуется использовать пероральную терапию N ацетилцистеином в сочетании с внутривенным введением изотонических растворов кристаллоидов [8]. По данным мета-анализа E.P. Navarese и соавт. добавление N-ацетилцистеина к физиологическому раствору натрия дополнительно снижает риск развития КИ-ОПП на 28% [отношение шансов (ОШ) 0,72, 95% доверительный интервал (ДИ) 0,57-0,99] [9]. В более поздних работах эффективность N-ацетилцистеина в профилактике КИ-ОПП подвергалась сомнениям.
Цель систематического обзора и мета-анализа – выполнить подробный анализ опубликованных отчетов о клинических исследованиях для оценки влияния N-ацетилцистеина на частоту развития КИ-ОПП.
Материал и методы
Данный систематический обзор и мета-анализ выполнили в соответствии с рекомендациями «Предпочтительных элементов отчетности для систематических обзоров и руководящих принципов мета-анализа» (the Preferred Reporting Items for Systematic Reviews and Meta-Analyses guidelines – PRISMA) [10]. Проводился поиск существующей литературы в базе данных PubMed/MEDLINE в период с 2015 г. по 16 февраля 2022 г. Ключевые слова включали MeSH термины «acute kidney injury» OR «contrast-induced nephropathy», или «AKI», или «CIN» и «contrast media» и «N-acetylcysteine». Не использовались фильтры по языку, типу исследования. Другие критерии включения: представление в результатах исследования частоты развития контраст-индуцированной нефропатии (КИН) или КИОПП в течение периода наблюдения, возраст пациентов старше 18 лет. Описание отдельных случаев развития КИН или КИ-ОПП в изучаемой популяции, исследования с участием менее 10 пациентов, отсутствие в исследовании группы сравнения, не получающей Nацетилцистеин, обзоры и мнения экспертов, а также исследования, результаты которых опубликованы только в виде тезисов, исключались из анализа. Был проведен ручной поиск ссылок в обнаруженных статьях для выявления дополнительных исследований, которые могут представлять интерес. Два автора независимо друг от друга изучали заголовки и аннотации публикации на предмет соответствия критериям включения, в случае возникновения разногласий публикация анализировалась третьим автором, и разногласия устранялись путем обсуждения в группе авторов обзора. Включенные исследования были подробно рассмотрены для установления клинико-демографических характеристик пациентов, частоты развития КИН или КИ-ОПП. Первичной конечной точкой являлось развитие КИН, определенное как повышение уровня креатинина в сыворотке более чем на 25% или 44,2 мкмоль/л (0,5 мг/дл) от исходного через 48-72 ч после введения рентгеноконтрастного вещества. Для оценки систематической ошибки исследований использовали Кокрейновский инструмент оценки риска RoB2 [11].
Все виды статистического анализа проводили с помощью пакета программ Review Manager 5.4. Статистическую гетерогенность исследовании количественно ̆ оценивали с помощью Chi2 и статистики I2. Для дихотомизированных данных рассчитали ОШ и 95% ДИ. Модель случайных эффектов использовалась в случае p<0,10 или I2> 50%.
Результаты
Общее количество публикаций на основе изначально избранной стратегии поиска составило 98. После изучения названий и аннотаций статей из дальнейшего анализа были исключены 58 статей. Из полнотекстовых статей остальных 40 исследований были удалены 33 статьи: 2 являлись дубликатами статей, 12 – не имели контрольной группы, не использующей N-ацетилцистеин, 5 являлись описанием отдельных случаев развития КИН или КИ-ОПП, в 2-х отсутствовали данные о конечной точке, 12 – обзоры и мнения экспертов. В мета-анализ были включены 7 исследований, соответствующих критериям включения и исключения (рис. 1). Детали включенных исследований представлены в табл. 1.
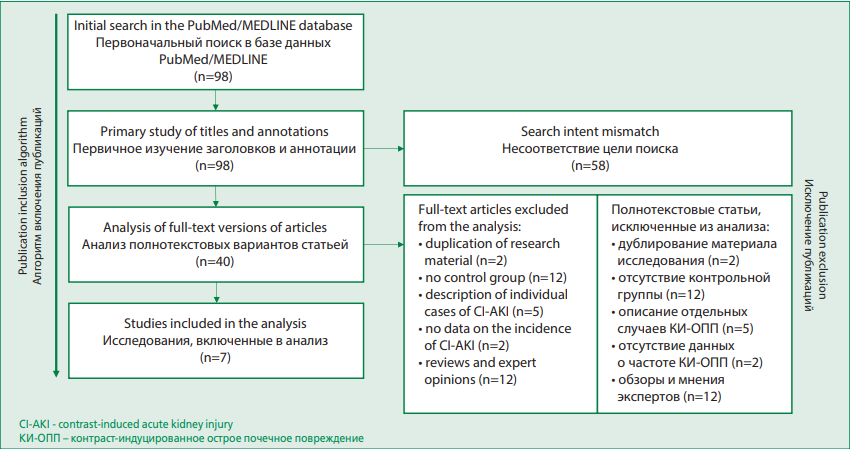
Figure 1. Algorithm for selecting publications.
Рисунок 1. Алгоритм отбора публикаций.
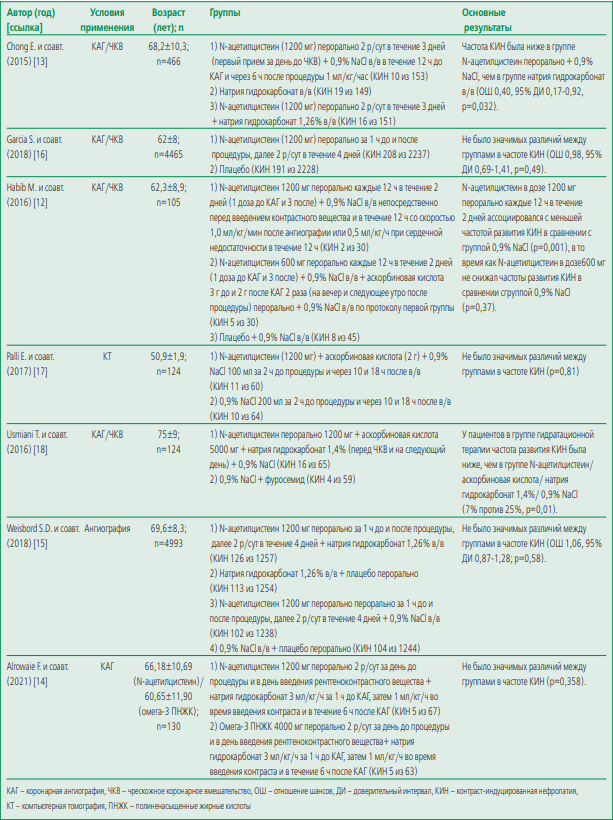
Table 1 Characteristics of the studies included in the meta-analysis
Таблица 1. Характеристика, включенных в мета-анализ исследований
Оценка систематической ошибки исследований с использованием RoB2 tool представлена на рис. 2. Ни одно из 7 исследований не было оценено как имеющее общий высокий риск систематической ошибки, 5 исследований (71%) были оценены как имеющие низкий общий риск, а остальные 2 (29%) – как имеющие некоторые опасения относительно общего риска систематической ошибки. Исследование M. Habib и соавт. являлось одноцентровым рандомизированным плацебо-контролируемым [12], в статье не приведено сравнение исходных клинических характеристик изучаемых групп, что затрудняет оценку процесса рандомизации, определенное протоколом исследования. Назначение препаратов сравнения позволяло исследователям быть осведомленными о группе вмешательства. Исследование CONTRAST, проведенное E. Chong и соавт., было многоцентровым рандомизированным контролируемым, дизайн исследования также позволял исследователям быть осведомленными о группе вмешательства, расчетное количество пациентов, необходимое для демонстрации эффекта исследуемого препарата, не было достигнуто, к тому же имело место исключение части пациентов из анализа по различным причинам [13]. Исследование F. Alrowaie и соавт. являлось одноцентровым рандомизированным контролируемым, и исходные характеристики групп статистически значимо различались по возрасту, частоте приема ингибиторов ангионтензин-превращающего фермента, что не исключает проблем в процессе рандомизации [14]. Исследования S.D. Weisbord и соавт. [15] и S. Garcia и соавт. [16] были многоцентровыми двойными слепыми плацебо-контролируемыми рандомизированными, и не имели рисков систематической ошибки. Исследование E. Palli и соавт. являлось открытым одноцентровым рандомизированным контролируемым, определенное протоколом исследования назначение препаратов сравнения позволяло исследователям быть осведомленными о группе вмешательства [17]. Исследование T. Usmiani и соавт. было одноцентровым рандомизированным контролируемым, так же, как и в предыдущей работе определенное протоколом назначение препаратов сравнения позволяло исследователям быть осведомленными о группе вмешательства [18].
В систематический обзор и мета-анализ были включены 10394 пациентов из 7 работ (5288 пациентов получали N-ацетилцистеин, 5106 – получали инфузию солевых растворов в качестве меры профилактики КИ-ОПП или инфузию солевых растворов и плацебо).
Результаты мета-анализа показали, что у пациентов, получавших N-ацетилцистеин, КИ-ОПП развивалось с такой же частотой, как у пациентов, которые не получали такой терапии в качестве меры профилактики развития данного осложнения (ОШ=1,06, 95% ДИ=0,91–1,23, p=0,46; рис 3. Результаты статических тестов на гетерогенность указывали на отсутствие статистически значимой гетерогенности различий по выраженности эффекта терапии между отдельными исследованиями (Tau2=0,04; Chi2=9,67, df=6 (p=0,14); I2=38%), в связи с чем была использована модель фиксированного эффекта. При оценка публикационного смещения на диаграмме funnel plot (рис. 4) не выявлено смещения публикации в сторону положительного или отрицательного влияния N-ацителцистеина на частоту развития КИ-ОПП.
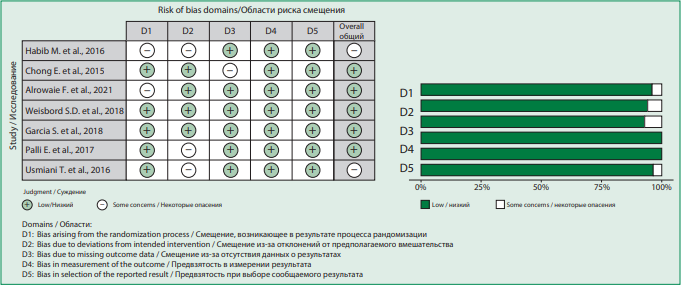
Figure 2. Risk of bias for studies included in the meta-analysis
Рисунок 2. Риск систематической ошибки исследований, включенных в мета-анализ
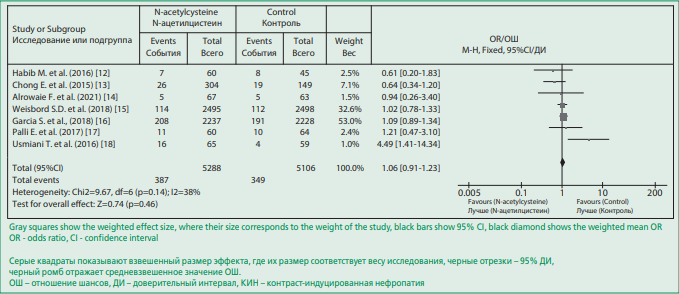
Figure 3. Effect of N-acetylcysteine on the development of contrast-induced nephropathy
Рисунок 3. Эффект N-ацетилцистеина на развитие КИН
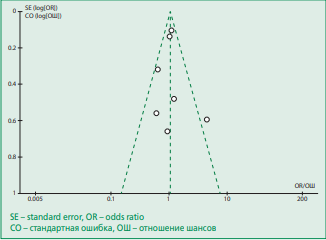
Figure 4. Estimated publication bias
Рисунок 4. Оценка публикационного смещения
Обсуждение
Широкое использование инвазивных диагностических исследований с использованием рентгеноконтрастных препаратов, традиционно входящих в лидирующую тройку причин развития ОПП, в современной кардиологии нашло отражение и в проведенном нами мета-анализе, где 5 из 7 исследований были посвящены возможностям профилактики КИ-ОПП у кардиологических пациентов, которым требовалось проведение коронароангиографии. На сегодняшний день отсутствуют убедительные доказательства эффективности профилактических вмешательств, направленных на снижение риска развития КИ-ОПП.
В наш анализ вошло 7 исследований с участием 10394 пациентов, в которых изучали N-ацетилцистеин по сравнению с плацебо или введением только солевых растворов (натрия гидрокарбонат или натрия хлорид
0,9%). Результаты настоящего мета-анализа показали, что отсутствуют существенные различия между введением солевых растворов (натрия гидрокарбонат или натрия хлорид 0,9%) и приемом N-ацителцистеина для предотвращения КИ-ОПП у пациентов, подвергающихся введению рентгеноконтрастных препаратов. Среди включенных исследований исследования E. Chong и соавт. [13] и M. Habib и соавт. [12] показали, что высокие дозы N-ацителцистеина (1200 мг перорально 2 р/д) снижают частоту КИ-ОПП по сравнению с введением солевых растворов (натрия гидрокарбонат или натрия хлорид 0,9%), что не соответствовало нашим результатам. Однако в исследованиях S. Garcia и соавт. [16] и S.D. Weisbord и соавт. [15], в которых использовалась такая же дозировка N-ацителцистеина, сравнивали эффект данного препарата только с приемом плацебо, либо в сочетании плацебо с введением натрия гидрокарбонат и натрия хлорид 0,9%, соответственно, не было выявлено существенной разницы в предотвращении КИ-ОПП. Учитывая большое количество участников в этих двух исследованиях, вес этих исследований в проведенном мета-анализе составил 85%. В работах E. Palli и соавт. [17] и F. Alrowaie и соавт. [14] также не получено различий в частоте КИОПП в группе пациентов, получавших N-ацителцистеин, и не получавших данного препарата. В исследовании T. Usmiani и соавт. [18] частота КИ-ОПП среди пациентов, получавших N-ацителцистеин, была выше, чем в группе пациентов, получавших только натрия хлорид 0,9%. Эти противоречивые результаты могли быть получены из-за различия в дизайне исследований, включая как число участников, так и процесс рандомизации, позволявший исследователям быть осведомленными о группе вмешательства. Между тем все включенные в мета-анализ исследования были высокого качества. К ограничениям нашего анализа можно отнести некоторые различия в дизайне исследований (время введения препаратов, дозировки и длительность введения солевых растворов, продолжительность приема и пути введения N-ацителцистеина).
Заключение
Проведенный мета-анализ показывает, что использование N-ацителцистеина не дает каких-либо преимуществ в снижении частоты КИ-ОПП по сравнению с введением только солевых растворов (натрия гидрокарбонат или натрия хлорид 0,9%).
Отношения и Деятельность. Нет.
Relationships and Activities. None.
Финансирование: Исследование проведено при поддержке ФГБОУ ВО Тюменский ГМУ Минздрава России.
Funding: The study was performed with the support of the Tyumen State Medical University
Список литературы
1. Ehrmann S, Aronson D, Hinson JS, et al. Contrast-associated acute kidney injury is a myth: Yes. Intensive Care Med. 2018;44(1):104-6. DOI:10.1007/s00134-017-4950-6.
2. Ando G, Cortese B, Russo F et al. Acute Kidney Injury After Radial or Femoral Access for Invasive Acute Coronary Syndrome Management. J Am Coll Cardiol. 2017;69(21):2592-603. DOI:10.1016/j.jacc.2017.02.070.
3. Ostermann M, Zarbock A, Goldstein S, et al. Recommendations on Acute Kidney Injury Biomarkers From the Acute Disease Quality Initiative Consensus Conference. JAMA Netw Open. 2020;3(10):e2019209. DOI:10.1001/jamanetworkopen.2020.19209.
4. Kaltsas E, Chalikias G, Tziakas D. The Incidence and the Prognostic Impact of Acute Kidney Injury in Acute Myocardial Infarction Patients: Current Preventive Strategies. Cardiovasc drugs Ther. 2018;32(1):81-98. DOI:10.1007/s10557-017-6766-6.
5. Kabeer MA, Cross J, Hamilton G, et al. Obesity as a Risk Factor for Radiographic Contrast-Induced Nephropathy. Angiology. 2021;72(3):274-8. DOI:10.1177/0003319720969536.
6. Ma G, Wang G, Xiao D, et al. Meta-analysis on allopurinol preventive intervention on contrast-induced acute kidney injury with random controlled trials: PRISMA. Medicine (Baltimore). 2019;98(25): e15962. DOI:10.1097/MD.0000000000015962.
7. Vandenberghe W, Hoste E. Contrast-associated acute kidney injury: does it really exist, and if so, what to do about it? F1000Res. 2019;8:753. DOI:10.12688/f1000research.16347.1.
8. Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney Int Suppl. 2012;2(1):1-138. DOI:10.1038/kisup.2012.1.
9. Navarese EP, Gurbel PA, Andreotti F, et al. Prevention of contrast-induced acute kidney injury in patients undergoing cardiovascular procedures-a systematic review and network meta-analysis. PLoS One. 2017;12(2):e0168726. DOI:10.1371/journal.pone.0168726.
10. Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71. DOI:10.1136/bmj.n71.
11. Higgins JPT, Altman DG, Gotzsche PC, et al. The Cochrane Collaboration's tool for assessing risk of bias in randomised trials. BMJ. 2011;343(oct18 2):d5928-d5928. DOI:10.1136/bmj.d5928.
12. Habib M, Hillis A, Hammad A. N-acetylcysteine and/or ascorbic acid versus placebo to prevent contrast-induced nephropathy in patients undergoing elective cardiac catheterization: The NAPCIN trial; A single-center, prospective, randomized trial. Saudi J Kidney Dis Transpl. 2016;27(1):55-61. DOI:10.4103/1319-2442.174072.
13. Chong E, Poh KK, Lu Q, et al. Comparison of combination therapy of high-dose oral N-acetylcysteine and intravenous sodium bicarbonate hydration with individual therapies in the reduction of Contrast-induced Nephropathy during Cardiac Catheterisation and Percutaneous Coronary Intervention (CONTRAST): A multi-centre, randomised, controlled trial. Int J Cardiol. 2015;201:237-42. DOI:10.1016/j.ijcard.2015.07.108.
14. Alrowaie F, Almatham K, Alsamadi F, et al. Could Omega 3 fatty acids reduce the risk of contrast-induced nephropathy in patients undergoing coronary angiography? A randomized controlled trial. Saudi J Kidney Dis Transplant. 2021;32(2):328. DOI:10.4103/1319-2442.335443.
15. Weisbord SD, Gallagher M, Jneid H, et al. Outcomes after Angiography with Sodium Bicarbonate and Acetylcysteine. N Engl J Med. 2018;378(7):603-14. DOI:10.1056/NEJMoa1710933.
16. Garcia S, Bhatt DL, Gallagher M, et al. Strategies to Reduce Acute Kidney Injury and Improve Clinical Outcomes Following Percutaneous Coronary Intervention: A Subgroup Analysis of the PRESERVE Trial. JACC Cardiovasc Interv. 2018;11(22):2254-61. DOI:10.1016/j.jcin.2018.07.044.
17. Palli E, Makris D, Papanikolaou J, et al. The impact of N-acetylcysteine and ascorbic acid in contrast-induced nephropathy in critical care patients: An open-label randomized controlled study. Crit Care. 2017;21(1):269. DOI:10.1186/s13054-017-1862-3.
18. Usmiani T, Andreis A, Budano C,et al. AKIGUARD (Acute Kidney Injury GUARding Device) trial. J Cardiovasc Med. 2016;17(7):530-7. DOI:10.2459/JCM.0000000000000348.
Об авторах
Е. М. МежоновРоссия
Межонов Евгений Михайлович.
Тюмень.
eLibrary SPIN 2935-9617
Ю. А. Вялкина
Россия
Вялкина Юлия Александровна.
Тюмень.
eLibrary SPIN 4237-5048
С. В. Шалаев
Россия
Шалаев Сергей Васильевич.
Тюмень.
eLibrary SPIN 5285-0082
Рецензия
Для цитирования:
Межонов Е.М., Вялкина Ю.А., Шалаев С.В. N-ацетилцистеин в профилактике контраст-индуцированного острого почечного повреждения: систематический обзор и мета-анализ рандомизированных контролируемых клинических исследований. Рациональная Фармакотерапия в Кардиологии. 2022;18(4):455-461. https://doi.org/10.20996/1819-6446-2022-08-10
For citation:
Mezhonov E.M., Vyalkina Yu.A., Shalaev S.V. N-acetylcysteine in the Prevention of Contrast-induced Acute Kidney Injury: a Systematic Review and Meta-analysis of Randomized Controlled Clinical Trials. Rational Pharmacotherapy in Cardiology. 2022;18(4):455-461. (In Russ.) https://doi.org/10.20996/1819-6446-2022-08-10

















































