Перейти к:
Случай успешного медикаментозного лечения желудочковой тахикардии у пациента с ишемической болезнью сердца и сердечной недостаточностью
https://doi.org/10.20996/1819-6446-2023-02-05
Аннотация
У пациентов с ишемической болезнью сердца патогенетические механизмы возникновения нарушений ритма, в том числе желудочковых аритмий высоких градаций (вплоть до неустойчивой желудочковой тахикардии), могут существенно различаться. Поэтому характеристики желудочковых нарушений ритма необходимо рассматривать по совокупности данных с учетом всех имеющихся особенностей. В настоящей работе отражена важность персонифицированного подхода к тактике ведения пациента с ишемической болезнью сердца, перенесенным 18,5 лет тому назад обширным инфарктом миокарда с последующими маммаро-коронарным шунтированием, аневризмэктомией и формированием сердечной недостаточности с низкой фракцией выброса, у которого желудочковые аритмии возникли на фоне стабильного течения ишемической болезни, но после эмоционального стресса. Расширенное обследование, а также детальное изучение характера желудочковых нарушений ритма, позволило определить главный провоцирующий их фактор, и подобрать индивидуализированное патогенетическое лечение с хорошим антиаритмическим результатом, сохраняющимся в течение нескольких лет наблюдения. Пациентам с ишемической болезнью сердца и хронической сердечной недостаточностью после исключения ишемического и симпатозависимого характера желудочковой эктопии в качестве дополнительного обследования может быть рекомендовано проведение ментальных проб и психологического анкетирования с целью оценки вклада психоэмоционального фактора в аритмогенез. Считать, что все желудочковые аритмии у больных ишемической болезнью сердца носят ишемический характер некорректно, а в некоторых клинических ситуациях даже ошибочно.
Ключевые слова
Для цитирования:
Рыньгач Е.А., Татаринова А.А., Жабина Е.С., Жданова О.Н., Трешкур Т.В. Случай успешного медикаментозного лечения желудочковой тахикардии у пациента с ишемической болезнью сердца и сердечной недостаточностью. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):89-95. https://doi.org/10.20996/1819-6446-2023-02-05
For citation:
Ryngach E.A., Tatarinova A.A., Zhabina E.S., Zhdanova O.N., Treshkur T.V. A Case of Successful Medical Treatment of Ventricular Tachycardia in a Patient With Ischemic Heart Disease and Heart Failure. Rational Pharmacotherapy in Cardiology. 2023;19(1):89-95. (In Russ.) https://doi.org/10.20996/1819-6446-2023-02-05
Введение
Доказано, что в большинстве случаев внезапной смерти в связи с фатальными аритмиями основным пусковым фактором являются желудочковые эктопические комплексы (ЖЭК) (до 90%) [1-2]. Однако вопрос о том, какие именно желудочковые аритмии (ЖА) у больных ишемической болезнью сердца (ИБС) наиболее опасны и какое лечение аритмии оптимально в каждом конкретном случае, до сих пор является предметом дискуссии [3]. Наиболее уязвимой группой принято считать пациентов с желудочковой тахикардией (ЖТ), перенесенным инфарктом миокарда (ИМ), осложнившимся хронической сердечной недостаточностью с низкой фракцией выброса (СНнФВ) [4]. При определенном сочетании этих факторов риска в качестве первичной профилактики внезапной смерти рекомендуется имплантация кардиовертера-дефибриллятора [5].
Хотя ЖА регистрируются у большинства больных ИБС (до 99%), они очень вариабельны как по количеству, так и по качественным характеристикам, и поэтому их прогностическая значимость неодинакова. По-прежнему наиболее опасными считаются парные и полиморфные ЖЭК, а также ЖА большей комплексности. Вместе с тем, нельзя забывать, что для дифференцированного подхода к ведению больных с аритмией, помимо количественных и качественных её характеристик, важно учитывать и фоновую клиническую ситуацию в момент возникновения ЖА. Так, желудочковые нарушения ритма, ассоциированные с ишемией миокарда в сочетании с сопутствующей гиперсимпатикотонией, что по совокупности снижает порог фибрилляции желудочков, требуют незамедлительного пересмотра антиангинального лечения, включая инвазивные методы. Однако аритмии у больных ИБС могут быть не только ишемического генеза. Накопилось много данных о влиянии психогенных факторов, в частности, как острого, так и хронического стресса, на аритмогенный потенциал миокарда, что в первую очередь связано с влиянием изменения активности вегетативной и центральной нервной системы и, несомненно, может быть провоцирующим фактором в развитии ЖА, вплоть до фатальных [6-8].
В литературе нам не встретились классификации ЖА, учитывающие в полной мере все известные провоцирующие факторы, в том числе физический или эмоциональный стресс и их сочетание.
Многочисленные рекомендации по обследованию пациентов с ИБС и ЖА не всегда оптимальны для выбора последующей персонифицированной терапии, что настоятельно требует пересмотра имеющихся алгоритмов [5].
Цель настоящего сообщения – на примере многолетнего проспективного наблюдения за пациентом с ИБС, перенесенным ИМ и СНнФВ, осложнившимися ЖА высоких градаций, показать значение индивидуализированного подхода к обследованию и выбору лечебной тактики.
Клинический случай
Больной А. 64 лет обратился в Национальный медицинский исследовательский центр им. В.А. Алмазова (в дальнейшем: Центр) в марте 2013 г. с жалобами на плохо переносимые ощущения сердцебиения, перебоев в работе сердца, нарушение сна и повышенную утомляемость, появившиеся 6 мес назад. Во время мониторирования электрокардиограммы (ЭКГ) зарегистрированы следующие ЖА: одиночные ЖЭК, включая полиморфные, парные и эпизоды неустойчивой ЖТ в патологическом количестве, преимущественно в дневное время, что послужило поводом для госпитализации.
Из анамнеза: дебют ИБС в 2003 г. с острого ИМ передней стенки левого желудочка (ЛЖ), осложнившегося полной блокадой левой ножки пучка Гиса (БЛНПГ) и аневризмой ЛЖ. Тогда же были выполнены коронароангиография и вентрикулография, по результатам которых проведены маммаро-коронарное шунтирование передней межжелудочковой артерии и аневризмэктомия ЛЖ с эндовентрикулопластикой. На протяжении последующих 9,5 лет самочувствие пациента было удовлетворительным. Он работал заведующим кафедрой в крупном университете, с нагрузкой – физической и эмоциональной справлялся успешно. Принимал ингибиторы ангиотензинпревращающего фермента, бета-адреноблокаторы, статины, антиагреганты, антагонисты рецепторов ангиотензина II, антагонисты альдостерона, диуретики.
Впервые вышеописанные жалобы появились после эмоционального стресса в октябре 2012 г. По результатам суточного мониторирования ЭКГ зарегистрировано 9430 одиночных полиморфных ЖЭК, 1540 парных ЖЭК, 216 неустойчивых ЖТ с максимальной частотой 120 в 1 мин. Причиной плохого самочувствия пациента сочли зарегистрированные ЖА. Их расценили как осложнение ИБС, и в качестве антиаритмической терапии были назначены бисопролола фумарат (5 мг) и амиодарон (по насыщающей схеме с переходом на поддерживающую дозу 200 мг в течение 3 мес), однако ожидаемый эффект от медикаментозной терапии отсутствовал (количество ЖЭК не изменилось).
Пациенту был выставлен следующий клинический диагноз.
Основное заболевание. ИБС: Постинфарктный кардиосклероз (ИМ в 2003 г.). Маммаро-коронарное шунтирование, аневризмэктомия с эндовентрикулопластикой (2003 г.). Гипертоническая болезнь III стадии, 3 степени, риск 4.
Осложнения. ЖА высоких градаций (частые полиморфные одиночные, парные ЖЭК, неустойчивая ЖТ). Полная БЛНПГ. Хроническая сердечная недостаточность IIA ст., III функционального класса (NYHA).
Сопутствующие заболевания. Атеросклероз брахиоцефальных артерий, без гемодинамически значимого стенозирования. Хронический калькулезный холецистит, вне обострения. Хронический гастрит, вне обострения. Доброкачественная гиперплазия предстательной железы I ст.
Во время госпитализации в Центре: при эхокардиографии выявлены дилатация левого (индекс объема 46 мл/м²) и правого (индекс объема 42 мл/м²) предсердий. Эксцентрическая гипертрофия ЛЖ. Фракция выброса ЛЖ по Симпсон – 37 % за счет акинезии, истончения, уплотнения миокарда верхушки, гипокинезии остальных стенок. Незначительная межжелудочковая диссинхрония, значительная внутрижелудочковая диссинхрония. Псевдонормальный тип диастолической дисфункции ЛЖ. Конечный диастолический размер 78 мм, конечный систолический размер 62 мм, конечный диастолический объем 243 мл, конечный систолический объем 153 мл, ударный объем 90 мл. Значимых патологических изменений со стороны правого желудочка не выявлено.
При суточном мониторировании ЭКГ регистрировался синусовый ритм с полной БЛНПГ со средней ЧСС 67 в 1 мин. Одиночные полиморфные ЖЭК – 13090 в сутки: двух морфологий (7600 – первой и 5490 – второй) с ЭКГ признаками парасистолии. Парные ЖЭК: мономорфные – 1034 (днем – 1018), полиморфные – 793 (днем – 563). Эпизоды неустойчивой ЖТ (до 5 QRS комплексов с ЧСЖ до 120 в 1 мин) с дневным типом распределения: мономорфной – 62, полиморфной – 57.
Стресс-эхокардиография не выполнялась из-за малой информативности – наличие обширных рубцовых полей.
ЭКГ: Р=150 мс, PQ=200 мс, QRS=135 мс, QT=460 мс, QТc=460 мс. Синусовый ритм с ЧСС=60 в 1 мин. Увеличение обоих предсердий, нарушение межпредсердной проводимости. Полная БЛНПГ с выраженным отклонением электрической оси QRS влево: угол ά=-90° (рис. 1).
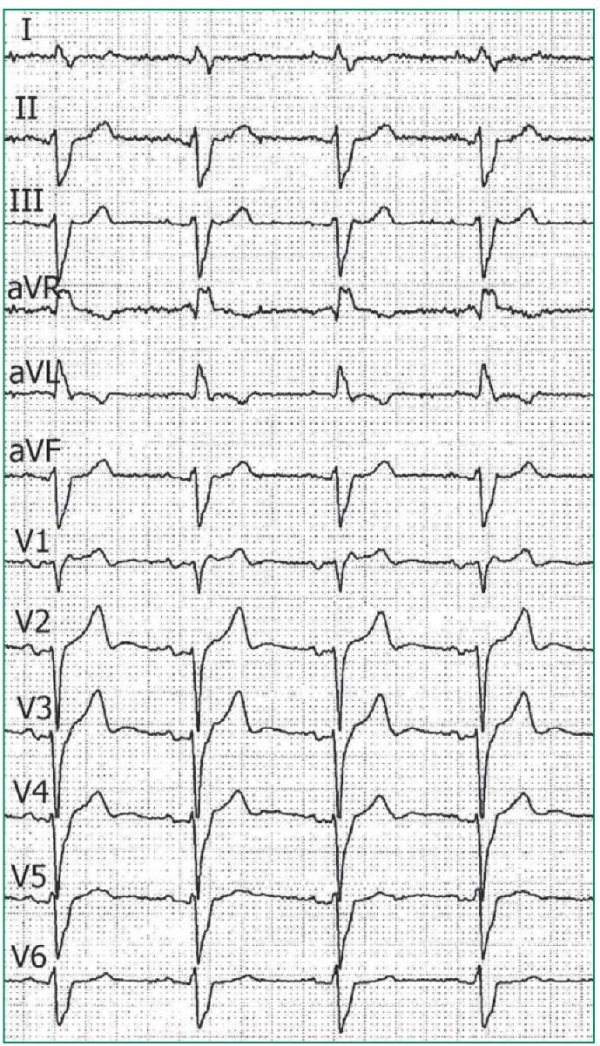
Figure 1. 12-lead ECG of patient A. during hospitalization (25 mm/min, 1 mV=10 mm)
Рисунок 1. ЭКГ в 12 отведениях пациента А. во время госпитализации
Результаты коронароангиошунтографии: периферия передней межжелудочковой артерии удовлетворительная, заполняется по функционирующему маммаро-коронарному шунту. Остальные коронарные артерии без значимого стенозирования.
С учетом дневного типа распределения ЖА для детального анализа «поведения» аритмии на фоне физической нагрузки выполнен тредмил-тест по модифицированному протоколу Bruce.
В претесте только при беседе с больным о его здоровье регистрировались частые одиночные и парные полиморфные ЖЭК, нарастающие по комплексности до неустойчивой нерегулярной ЖТ (рис. 2).
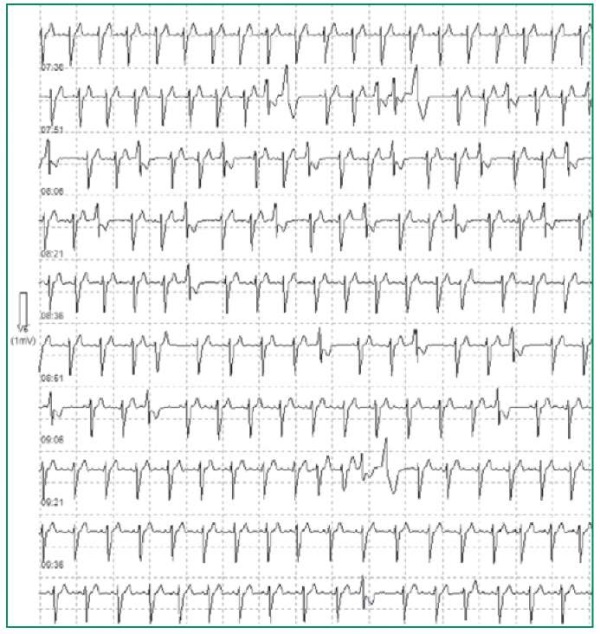
Figure 2. ECG fragment of patient A. (continuous recording in lead V6) in the pretest during a conversation about the disease
Рисунок 2. Фрагмент ЭКГ пациента А. (непрерывная запись в отведении V6) в претесте во время разговора о болезни
На всем протяжении физической нагрузки нарушения ритма не регистрировались, сохранялись признаки полной БЛНПГ со стабильной реполяризацией. Тредмил-тест был прекращен на II ступени в связи с достижением субмаксимальной ЧСС 116 в 1 мин (75%) и усталостью ног. Толерантность к физической нагрузке выше средней (7 МET), превышала повседневную активность пациента. ЖА не возобновились в восстановительном периоде. Анализ пробы с физической нагрузкой исключил ишемический и симпатозависимый характер желудочковой эктопии.
Учитывая полиморфизм ЖЭК на поверхностной ЭКГ, для определения показаний к хирургическому лечению аритмии/установке имплантируемых устройств была проведена топическая диагностика с использованием неинвазивного эндо/эпикардиального электрофизиологического картирования сердца: синхронная регистрация униполярных электрокардиограмм в 224 отведениях с поверхности грудной клетки; магнито-резонансная томография сердца с внутривенным контрастированием и ЭКГ синхронизацией с дальнейшим построением изопараметрических карт на эпи- и эндокардиальной модели сердца с использованием специального программного обеспечения «AMYCARD 01C EP LAB» [9]. Удалось установить, что наличие двух морфологий ЖЭК было обусловлено различным интрамиокардиальным проведением эктопического импульса, и, следовательно, на поверхностной ЭКГ наблюдался «ложный полиморфизм». Единственный аритмогенный очаг был локализован в области выходного тракта правого желудочка.
Анализируя полученные данные, консилиумом врачей, включая кардиолога и кардиохирурга-аритмолога, были определены показания к выполнению электрофизиологического исследования, при проведении которого не индуцировалась неустойчивая и устойчивая ЖТ, регистрировались лишь единичные одиночные полиморфные ЖЭК.
Таким образом, у пациента с СНнФВ ишемического генеза с учетом вышеперечисленных результатов обследований и отсутствия в анамнезе пресинкопе/синкопе не было показаний к имплантации кардиовертера-дефибриллятора. От проведения радиочастной аблации аритмогенного очага решено было воздержаться. Тем не менее, симптомность ЖА и неэффективность антиаритмического лечения послужили основанием продолжить поиск причин ЖА.
Настораживало появление ЖА только при сборе анамнеза у пациента, при разговоре о его болезни, что, по сути, могло быть имитацией ментальной пробы (МП) – «разговор на значимые темы», и указывало на возможный вклад эмоционального напряжения в индукцию ЖА.
Поэтому в дополнение к общепринятым методам с целью моделирования нейрофизиологических процессов при эмоциональном стрессе были использованы МП: тест Струпа, «возврат гнева», разговор на значимую тему/о болезни, арифметический счет; проба Вальсальвы [10]. На рис. 3 продемонстрирован фрагмент ЭКГ во время теста Струпа. До начала его проведения ЖЭК не было. А во время теста отмечалось резкое увеличение ЖЭК (более чем в два раза), появление парных ЖЭК и неустойчивой ЖТ, состоящей из 3 комплексов.
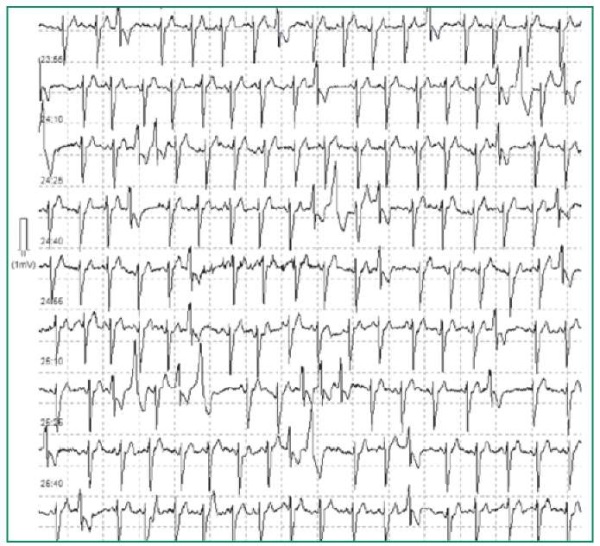
Figure 3. ECG fragment (lead II, continuous recording) during the mental Stroop test in patient A.
Рисунок 3. Фрагмент ЭКГ (отведение II, непрерывная запись) во время ментального теста Струпа больного А.
Кроме того, обращала на себя внимание активная жестикуляция пациента во время теста. Во время релаксации наблюдалось исчезновение аритмии, тест Струпа был расценен как положительный. Аналогичные результаты были получены при тестах «арифметический счет», «разговор на значимые темы» и пробе Вальсальвы. Появление и прогрессирование ЖА наблюдались только в фазы МП, которые соответствовали усилению симпатических влияний.
Психологическое анкетирование включало шкалы: ситуативной тревожности Спилбергера и Ханина, личностных проявлений тревоги Тейлор, нервно-психического напряжения Немчина; методики дифференциальной диагностики депрессивных состояний Зунга; анкеты оценки качества жизни Либис для больных с аритмией.
По результатам анкетирования выявлено повышение ситуативной тревожности при нормальных показателях личностной тревожности и нервно-психического напряжения; данных о наличии депрессии не было. Отмечено снижение качества жизни в связи с аритмией на 21%.
Больной консультирован психологом, поставлен диагноз: Тревожно-невротическое расстройство (ТНР).
Пациенту к основной терапии был присоединен анксиолитик тетраметилтетраазабициклооктандион 1500 мг/сут с рекомендацией последующего контроля через 2 мес [11]. Уже спустя 1 мес лечения он отметил субъективное улучшение: перебои и сердцебиение стали беспокоить значительно меньше, улучшились сон, настроение и работоспособность, что подтвердилось данными психодиагностики – снижением уровня ситуативной тревожности до низкого. Улучшилось качество жизни в 1,7 раз. На контрольном суточном мониторе ЭКГ через 2 мес приема препарата отмечалось: уменьшение одиночных ЖЭК с 12090 до 2902 (на 76%), парных ЖЭК – с 1034 до 93 (на 91%), эпизоды неустойчивой ЖТ не регистрировались. Эффект проведенного лечения был расценен как оптимальный в отношении ЖА.
Прошло 8,5 лет от момента госпитализации в Центр, пациент продолжает работать (в 2021 г. ему исполнилось 73 года). За этот период времени состояние его оставалось стабильным, возобновление аритмии всегда совпадало с периодами психоэмоционального напряжения, с которыми он успешно справлялся курсовым приёмом анксиолитического препарата и психотерапией (по требованию). В 2020 г. он перенес новую коронавирусную инфекцию средней степени тяжести. Следует отметить, что ни на её фоне, ни в период реконвалесценции ЖА не беспокоили и по результатам контрольного мониторирования ЭКГ нарастания желудочковой эктопической активности по количеству и комплексности не отмечалось.
Обсуждение
При поступлении в Центр пациента с ИБС с учетом СНнФВ ЛЖ (37%), патологического количества ЖЭК (15634 – 17,7% от общего количества QRS-комплексов), полиморфизма и высокой комплексности ЖА (парные, неустойчивая ЖТ) обсуждался вопрос о выборе тактики его ведения (включая инвазивные методы).
По результатам обследования очевидной связи дебюта ЖА (спустя 9,5 лет после перенесенного ИМ) с ухудшением течения ИБС, появлением ангинозных болей/эквивалентов стенокардии, снижением толерантности к физической нагрузке или прогрессированием хронической сердечной недостаточности обнаружено не было. Данные обследования позволили констатировать, что ЖА не носит ишемический характер и не провоцируется физической нагрузкой. Более того, очаг желудочковой эктопии расположен не в ЛЖ, что часто бывает после обширного ИМ с развитием аневризмы, а – в правом. Все это поставило под сомнение постинфарктный кардиосклероз как основной аритмогенный субстрат.
Учитывая национальные клинические рекомендации и отсутствие у больного гемодинамически значимых эпизодов ЖТ/фибрилляция желудочков, синкопе, индукции ЖТ при проведении электрофизиологического исследования, от имплантации кардиовертера-дефибриллятора и радиочастотной аблации эктопического очага было решено воздержаться и продолжить обследование для выяснения как характера ЖА, так провоцирующих её факторов.
Симптомность ЖА, беспокойство больного от отсутствия антиаритмического эффекта предшествующей терапии требовали уточнения причин сохранения аритмии и поиска других направлений терапии.
Пациент был полностью адаптирован к тому уровню физической активности, который он позволял себе – ходьба пешком в среднем темпе. Получал оптимальную стандартную терапию, был гемодинамически стабилен.
Обращало на себя внимание, что впервые ЖА возникли на фоне хронической стрессовой ситуации на работе – предстоящим переизбранием по конкурсу и личными опасениями о возможности предложения «ухода с заведования кафедрой». Однако причина ЖА сначала трактовалась исключительно с точки зрения основного диагноза, а появление у него тревожноастенической симптоматики – с фактом обнаружения патологического количества ЖЭК. Отсутствие антиаритмического эффекта на проводимую в течение нескольких месяцев терапию (бисопролол и амиодарон) вызывало у пациента еще большую тревожность. Количество ЖЭК и их комплексность за это время только увеличились, что и послужило причиной госпитализации.
Результаты психологического анкетирования, МП и заключение психолога свидетельствовали, что психогенный фактор играет определяющую роль в индукции аритмии у данного пациента. В качестве сопутствующего диагноза было добавлено ТНР и пересмотрена причинно-следственная связь – впервые ЖА возникла на фоне снижения работоспособности, нарушенного сна, что логично позволяло предположить связь аритмии с эмоциональным статусом.
Однако требовало объяснения несоответствие между данными МП и результатами тредмил-теста, а именно, усиление ЖА при МП наблюдалось при увеличении симпатической активности, в то время как во время физической нагрузки аритмии не было совсем, хотя известно, что физическая нагрузка — естественный активатор симпатического отдела вегетативной нервной системы.
Вместе с тем, при выполнении МП аритмия возникала уже при ЧСС 91 в 1 мин, а во время нагрузочной пробы не индуцировалась при субмаксимальной ЧСС (116 в 1 мин). Факт несоответствия влияния на организм человека физического и психического провоцирующего фактора, как по механизму, так и по силе воздействия, в литературе описан и свидетельствует о сложном генезе возникновения аритмий при психоэмоциональном стрессе, который инициируется в первую очередь нарушениями центральных механизмов регуляции вегетативной нервной системы. Безусловно, это объясняет в какой-то степени расхождение результатов МП и теста с физической нагрузкой.
Необходимо добавить, что проба с физической нагрузкой не была для нашего больного психологическим «стрессом», а, напротив, ходьба в умеренном темпе воспринималась им всегда как позитивный момент – пациент ежедневно ходил пешком, не испытывая при этом никаких отрицательных эмоций. Цель МП как раз обратная – вызывать психоэмоциональное напряжение и спровоцировать негативные эмоции.
Отсутствие ЖА на высоте физической нагрузки еще раз свидетельствовало, что его аритмия не нагрузочная/симпатозависимая. Это объясняет отсутствие антиаритмического эффекта бета-адреноблокатора. Данных по их применению у пациентов с психогенными аритмиями в доступной литературе нам не встретилось.
Учитывая все приведенное выше, стала очевидной необходимость лечения ТНР как наиболее вероятного и может быть основного патогенетического провоцирующего фактора в индукции ЖА у больного. В качестве возможного препарата лечения ТНР выбор пал на тетраметилтетраазабициклооктандион, так как из литературы известно, что помимо четкого анксиолитического эффекта, он, восстанавливая баланс вегетативной нервной системы, способствует уменьшению активности её симпатического отдела [12]. Полагают, что этот анксиолитик в основном влияет именно на катехоламинергическую систему, которая, бесспорно, является одной из ведущих в нейрохимическом реагировании при стрессорных воздействиях и эмоциональных реакциях. Кроме того, данный препарат обладает гармонизирующим действием на баланс активности различных нейромедиаторных систем мозга: активирующим в отношении тормозного медиатора ГАМК и ослабляющим в отношении возбуждающих нейротрансмиттеров – норадреналина и глутамата, а также нормализующим действием на взаимоотношения адрено- и серотонинергических воздействий [13]. Важно отметить, что указанный анксиолитик проявляет четкую центральную адренолитическую активность и не оказывает периферического адренолитического действия. И, по-видимому, именно поэтому при его применении был получен наряду с достаточно выраженным анксиолитическим клиническим эффектом и значимый АА результат.
Кардиальные эффекты Бисопролола основаны на взаимодействии с бета1-адренорецепторами кардиомиоцитов, а антиаритмическое действие его в основном связано с уменьшением симпатических влияний на автоматизм и проводимость сердца.
Многолетнее проспективное наблюдение, включая ретроспективный анализ (18,5 лет), за пациентом А. с учетом совокупности результатов обследования и определения психогенного характера ЖА подтверждает оправданность принятого решения о назначении анксиолитического препарата.
Данное клиническое наблюдение не уникально – мы уверены, что ЖА у больных ИБС могут быть различного происхождения, хотя на страницах печати это редко обсуждается [14]. Поэтому описанная ситуация может представлять интерес как с точки зрения алгоритма обследования больного, так и демонстрации успешной, экономичной и персонифицированной терапии. Выбранный анксиолитический препарат оказался достаточно эффективным средством лечения ТНР и ЖА, появившейся у пациента на фоне хронической стрессовой ситуации.
Пациентам с ИБС и ХСН после исключения ишемического и симпатозависимого характера желудочковой эктопии можно рекомендовать дополнять обследование МП и психологическим анкетированием с целью оценки вклада отрицательных эмоций и психоэмоционального стресса в индукцию аритмий, ибо только после определения причины возможен патогенетический подход к лечению ЖА.
Характеристики желудочковых нарушений ритма следует рассматривать по совокупности данных. У пациентов с, казалось бы, одинаковой клинической ситуацией: ИБС, перенесенный ИМ, СНнФВ патогенетические механизмы возникновения ЖА высоких градаций могут существенно различаться.
Заключение
В представленном клиническом наблюдении отражена важность поиска причины и провоцирующего фактора ЖА у больного ИБС с перенесенным обширным ИМ, СНнФВ, маммаро-коронарным шунтированием и аневризмэктомией. Благодаря комплексному обследованию, включающему проведение нагрузочных и ментальных тестов, психологического анкетирования, а также топической диагностики очага желудочковой парасистолии, удалось подобрать эффективный препарат для лечения ЖА и избежать в данном случае неоправданной инвазивной тактики – имплантации кардиовертера-дефибриллятора и радиочастотной аблации.
Relationships and Activities. None.
Отношения и Деятельность. Нет.
Funding. The study was carried out within the framework of state assignment N 056-00109-21-01.
Финансирование. Работа выполнена в рамках госзадания № 056-00109-21-01.
Список литературы
1. Ulus T, Kudaiberdieva G, Gorenek B. The onset mechanism of ventricular tachycardia Int J Cardiol. 2013;167(3):619-23. DOI:10.1016/j.ijcard.2012.09.034.
2. Gorenek B, Kudaiberdieva G, Birdane A, et al. Initiation of monomorphic ventricular tachycardia: electrophysiological, clinical features, and drug therapy in patients with implantable defibrillators. J Electrocardiol. 2003;36(3):213-8. DOI:10.1016/s0022-0736(03)00051-7.
3. Голухова Е.З., Громова О.И., Булаева Н.И., Бокерия Л.А. Внезапная сердечная смерть у больных ишемическои болезнью сердца: от механизмов к клиническои практике. Кардиология. 2017;57(12):73-81. DOI:10.18087/cardio.2017.12.10069.
4. Knuuti J, Wijns W, Saraste A, et al. ESC Scientific Document Group. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41(3):407-77. DOI:10.1093/eurheartj/ehz425.
5. 2020 Clinical Practice Guidelines of the Ministry of Health of the Russian Federation. Ventricular arrhythmias. Ventricular tachycardia and sudden cardiac death 2020 [cited 2022 Jan 26]. Available from: https://scardio.ru/content/Guidelines/2020/Clinic_rekom_ZHNR.pdf.
6. Levy MN. Sympathetic-parasympathetic interactions in the heart. Circ Res. 1971;29(5):437-45. DOI:10.1161/01.res.29.5.437.
7. Critchley HD, Taggart P, Sutton PM, et al. Mental stress and sudden cardiac death. Brain. 2005;128(1):75–130. DOI:10.1093/brain/awh324.
8. Цуринова Е.А. Острый и хронический психоэмоциональный стресс в генезе желудочковых аритмий. Трансляционная Медицина. 2014;(2):18-25.
9. Чмелевский М.П., Зубарев С.В., Буданова М.А. Неинвазивное электрофизиологическое картирование в диагностике желудочковых аритмий: от научных исследований к клинической практике. Трансляционная Медицина. 2015;(5):91-103.
10. Steptoe A, Vögele D. Methodology of mental stress testing in cardiovascular research. Сirculation. 1991;83(2):14-24.
11. Чутко Л.С., Рожкова Ф.В., Сидоренко В.А. и др. Генерализованное тревожное расстройство: психосоматические аспекты и подходы к лечению. Журнал Неврологии и Психиатрии. 2012;112(1): 40-4.
12. Коваленко В.Н., Несукай Е.Г., Дмитриченко Е.В. Корекція вегетативної дисфункції у хворихна гіпертонічну хворобу та нейроциркуляторну дистонію. Ліки. 2005;(1-2):118-24.
13. Громов Л., Дудко Е. Типичные и атипичные транквилизаторы. Вісник Фармакології та Фармації. 2003;10:7-11.
14. Рыньгач Е.А., Трешкур Т.В., Татаринова А.А., Шляхто Е.В. Алгоритм ведения пациентов со стабильной ишемической болезнью сердца и желудочковыми аритмиями высоких градаций. Терапевтический Архив. 2017;89(1):94-102. DOI:10.17116/terarkh201789194-102.
Об авторах
Е. А. РыньгачРоссия
Рыньгач Елена Александровна.
Cанкт-Петербург
А. А. Татаринова
Россия
Татаринова Анна Андреевна.
Cанкт-Петербург
Е. С. Жабина
Россия
Жабина Екатерина Сергеевна.
Cанкт-Петербург
О. Н. Жданова
Россия
Жданова Ольга Николаевна.
Cанкт-Петербург
Т. В. Трешкур
Россия
Трешкур Татьяна Васильевна.
Cанкт-Петербург
Рецензия
Для цитирования:
Рыньгач Е.А., Татаринова А.А., Жабина Е.С., Жданова О.Н., Трешкур Т.В. Случай успешного медикаментозного лечения желудочковой тахикардии у пациента с ишемической болезнью сердца и сердечной недостаточностью. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):89-95. https://doi.org/10.20996/1819-6446-2023-02-05
For citation:
Ryngach E.A., Tatarinova A.A., Zhabina E.S., Zhdanova O.N., Treshkur T.V. A Case of Successful Medical Treatment of Ventricular Tachycardia in a Patient With Ischemic Heart Disease and Heart Failure. Rational Pharmacotherapy in Cardiology. 2023;19(1):89-95. (In Russ.) https://doi.org/10.20996/1819-6446-2023-02-05

















































