Перейти к:
Частота и выраженность острого повреждения миокарда после торакальных хирургических вмешательств: эффекты никорандила
https://doi.org/10.20996/1819-6446-2023-01-08
Аннотация
Цель. Изучить периоперационную динамику биомаркеров повреждения миокарда высокочувствительного сердечного тропонина I (вч-сТн I), ишемией модифицированного альбумина (ИМА) и растворимого ST2 (sST2) при приеме никорандила у пациентов с раком легкого и сопутствующей ишемической болезнью сердца (ИБС), подвергающихся хирургической резекции легкого.
Материал и методы. В исследование включено 54 пациента (11 женщин и 43 мужчины) с немелкоклеточным раком легкого и сопутствующей стабильной ИБС, которым произведена резекция легкого в объеме лобэктомии или пневмонэктомии. Пациенты были рандомизированы в группу приема никорандила (пероральный прием в дозе 10 мг 2 р/сут в течение 7 дней до операции и 3 дней после нее; n=27) и контрольную группу (n=27). В исследуемых группах сравнивали периоперационную динамику вч-сТн I, ИМА и sST2, определяемых в крови перед операцией и через 24 и 48 ч после нее. Рассчитывали частоту острого повреждения миокарда в группах, диагностируемого в случаях прироста вч-сТн I после вмешательства на величину, большую 99 процентиля верхнего референсного предела. Оценивалии ассоциации приема никорандила и острого повреждения миокарда.
Результаты. Группы были сопоставимы по полу, возрасту, основным клиническим характеристикам, а также исходным уровням биомаркеров повреждения миокарда. После вмешательства в обеих выборках отмечен прирост концентраций вч-сТн I и sST2 и снижение ИМА (все р<0,02 для различий связанных групп). В группе никорандила по сравнению с контролем через 48 ч после операции были ниже уровни вчcТн I [16,7 (11,9;39,7) против 44,3 (15,0;130,7) нг/л; р<0,05] и sST2 [62,8 (43,6;70,1) против 76,5 (50,2;87,1) нг/мл; р<0,05], степень прироста вч-cТн I [14,8 (0,7;42,2) против 32,5 (14,0;125,0) нг/л; р<0,01] и sST2 [24,4 (10,3;42,4) против 47,4 (17,5; 65,3) нг/мл; р<0,05], а также медианы максимальных за весь послеоперационный период концентраций вч-cТн I [30,7 (12,0;53,7) против 79,0 (20,3;203,3) нг/л, р<0,01] и sST2 [99,8 (73,6;162,5) против 147,8 (87,8;207,7) нг/мл; р<0,05]. Содержание ИМА в крови через 24 ч после вмешательства уменьшилось при приеме никорандила в большей степени [-8,0 (-12,6;-2,0) против -2,7 (-6,0;+5,5) нг/мл; р<0,01]. Острое повреждение миокарда диагностировано у 7 человек в группе никорандила (25,9%) и у 15 в контрольной группе (55,6%; рχ2=0,027). Скорректированное отношение шансов развития острого повреждения миокарда при приеме никорандила составило 0,35 (95% доверительный интервал 0,15-0,83; р=0,017).
Заключение. Прием никорандила у пациентов с раком легкого и сопутствующей ИБС, подвергшихся хирургической резекции легкого, ассоциирован с меньшим послеоперационным приростом вч-сТн I и sST2 и снижением риска развития острого повреждения миокарда, что может свидетельствовать о кардиопротективном эффекте никорандила в условиях острого хирургического стресса.
Ключевые слова
Для цитирования:
Протасов К.В., Барахтенко О.А., Батунова Е.В., Распутина Е.A. Частота и выраженность острого повреждения миокарда после торакальных хирургических вмешательств: эффекты никорандила. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):17-25. https://doi.org/10.20996/1819-6446-2023-01-08
For citation:
Protasov K.V., Barahtenko O.A., Batunova E.V., Rasputina E.A. Incidence and Severity of Acute Myocardial Injury after Thoracic Surgery: Effects of Nicorandil. Rational Pharmacotherapy in Cardiology. 2023;19(1):17-25. (In Russ.) https://doi.org/10.20996/1819-6446-2023-01-08
Введение
Ежегодно в мире проводится более 300 млн. внесердечных хирургических операций, из них в России более 10 млн. [1][2]. Крупные внесердечные операции могут сопровождаться бессимптомным повышением уровня сывороточных биомаркеров повреждения миокарда, что встречается в десятки раз чаще, чем явный послеоперационный инфаркт миокарда (ИМ). Для обозначения этого феномена предложен специальный термин – повреждение миокарда после внесердечных операций (ПМВО), что означает повреждение миокарда, вызванное ишемией, которое развивается в первые 30 дней после вмешательства и выявляется по периоперационной динамике сердечного тропонина (сТн) в крови [3]. Частота обнаружения ПМВО при использовании не-высокочувствительного сТн варьируется от 4,6% до 22%, при использовании высокочувствительного сТн (вч-сТн) и после крупных полостных операций возрастает до 53,2% [4-7]. Отмечена тесная взаимосвязь развития ПМВО с ухудшением прогноза пациентов в послеоперационном периоде, даже в случаях бессимптомного изолированного повышения сТн [8]. Диагностическое и прогностическое значение других биомаркеров повреждения миокарда во внесердечной хирургии мало изучено. В немногочисленных исследованиях оценивалась периоперационная динамика и предсказательная ценность натрийуретических пептидов, белка, связывающего жирные кислоты [9][10].
Ишемией модифицированный альбумин (ИМА) – ранний чувствительный маркер ишемии миокарда – образуется при модификации окислительными свободными радикалами третичной молекулярной структуры сывороточного альбумина в условиях острой ишемии [11]. Способен реагировать на ишемию на самых ранних ее стадиях, что обусловливает его диагностическую ценность при остром коронарном синдроме [12]. Периоперационная динамика ИМА при внесердечных хирургических вмешательствах ранее не исследовалась.
Растворимый ST2 (sST2) – изоформа белка ST2 (growth STimulation expressed gene 2, Suppression of Tumorigenicity 2), стимулирующего фактора роста, экспрессируемого геном 2, или IL1RL1 – выделяется кардиомиоцитами, эндотелиальными клетками и фибробластами в условиях миокардиального стресса или повреждения, блокирует защитные эффекты комплекса ST2L/интерлейкин-33, тем самым способствуя ремоделированию миокарда и развитию сердечной недостаточности [13][14]. В настоящее время sST2 рассматривается как новый высокоинформативный предиктор кардиоваскулярных событий [15], неблагоприятных исходов острого ИМ [16]. Оценка диагностической и прогностической значимости sST2 может явиться перспективным направлением биомаркерной концепции оценки сердечно-сосудистого риска после внесердечных хирургических вмешательств.
Профилактика ПМВО практически не разработана. В действующих клинических рекомендациях по ведению пациентов, подвергающихся внесердечным операциям, в качестве средств медикаментозной профилактики сердечно-сосудистых осложнений рассматриваются только статины (IIaC) и бета-адреноблокаторы (IIbC) [17].
Никорандил – антиангинальный препарат с доказанным противоишемическим действием, обладающий эффектом фармакологического ишемического прекондиционирования [18][19]. Под влиянием никорандила снижается риск больших сердечно-сосудистых событий при стабильной ИБС [20][21], осложнений острого ИМ [22], чрескожных коронарных вмешательств [23][24], коронарного шунтирования [25], кардиохирургических вмешательств [26]. Мы предположили, что никорандил, в силу вышеописанных фармакологических эффектов, способен предотвратить или уменьшить выраженность острого повреждения миокарда, вызванного миокардиальным стрессом при внесердечной хирургии.
Цель исследования – изучить периоперационную динамику биомаркеров повреждения миокарда (вч-сТн I, ИМА и sST2) при приеме никорандила у пациентов с раком легкого и сопутствующей ИБС, подвергающихся хирургической резекции легкого.
Материал и методы
Набор пациентов в открытое проспективное рандомизированное исследование в параллельных группах осуществлялся в ГБУЗ «Областной онкологический диспансер» г. Иркутск, лабораторные исследования проводились в ГБУЗ «Областной онкологический диспансер» г. Иркутск и ЦНИЛ ИГМАПО – филиала ФГБОУ ДПО РМАНПО Минздрава России. Работа выполнена в соответствии с принципами Хельсинкской декларации. Протокол исследования одобрен комитетом по этике научных исследований ИГМАПО–филиала ФГБОУ ДПО РМАНПО Минздрава России (протокол №10 от 24.12.2021 г.). Все участники до включения в исследование подписали добровольное информированное согласие.
Критерии включения: пациенты с немелкоклеточным раком легкого I-III стадии, возраст от 50 до 75 лет, планируемое открытое хирургическое вмешательство в объеме пневмонэктомии или лобэктомии, наличие стабильной ИБС в виде стенокардии напряжения I или II функционального класса (ФК) и/или постинфарктного кардиосклероза, подписанное информированное согласие на операцию и участие в исследовании.
Критерии невключения: нестабильная стенокардия, острый ИМ, чрескожное коронарное вмешательство на момент рандомизации и в предшествующие шесть месяцев, систолическое АД >180 мм рт.ст. и/или диастолическое АД>110 мм рт.ст., хроническая сердечная недостаточность III-IV ФК или ее острая декомпенсация на момент рандомизации, операция по экстренным показаниям, прием никорандила, пролонгированных нитратов в предшествующий рандомизации месяц.
Пациенты, соответствующие критериям включения, были рандомизированы методом конвертов в группу вмешательства (n=30) и контрольную группу (n=30). Пациенты из группы вмешательства в течение 7 дней до даты планируемой операции и 3 дней после нее (с момента возобновления энтерального питания) принимали никорандил (Кординик®, компания ПИК-ФАРМА) перорально в дозе 10 мг 2 р/сут. Пациенты обеих групп получали стандартную терапию ИБС (за исключением никорандила в контрольной группе) и, при необходимости, артериальной гипертензии и сердечной недостаточности. Плановое хирургическое вмешательство в намеченные сроки было проведено 54 пациентам (11 женщин и 43 мужчины). Пять пациентов (8,3%) выбыли из исследования вследствие отмены у них операции, один умер во время вмешательства. Таким образом, в последующий анализ были включены по 27 пациентов из каждой группы. Всем пациентам интраоперационно проводилась инвазивная искусственная вентиляция легких (наркозно-дыхательный аппарат Dräger Fabius Plus, Германия).
Диагноз стабильной ИБС устанавливали в соответствии с действующими клиническими рекомендациями. Учитывали данные антропометрии, уровень АД при поступлении, статус курения, наличие коморбидной патологии, фракцию выброса левого желудочка и ФК сердечной недостаточности, исходный уровень креатинина крови, содержание гемоглобина до и после операции, объем и продолжительность хирургического вмешательства, объем кровопотери, длительность госпитализации, получаемую лекарственную терапию.
Рассчитывали риск сердечно-сосудистых осложнений внесердечных операций по скорректированному индексу сердечного риска (RCRI) [27] и шкале ACS-NSQIP [28]. Всем пациентам проводили запись электрокардиограммы (ЭКГ) покоя до операции и на первые, вторые и третьи сутки после нее, эхокардиографию в предоперационном периоде. Осуществляли периоперационный контроль АД и частоты сердечных сокращений. В группе никорандила оценивали переносимость препарата.
У всех пациентов трижды – за один час до операции, через 24 и 48 ч после нее –иммуноферментным методом определяли в крови уровни следующих биомаркеров повреждения миокарда: (1) вч-сТн I (фотометр Mini Vidas, “BioMerieux SA”, Франция; набор реагентов “VIDAS High Sensitive Troponin I (TNHS)”, “BioMerieux SA”, Франция); (2) ИМА (фотометр Stat Fax 4200, “Awarenes Technology”, США; набор реагентов “IMA”, Cloud-Clone Corp., США); (3) sST2 (фотометр Stat Fax 4200, “Awarenes Technology”, США; набор реагентов “Presage ST 2 Assay”, “Critical Diagnostics”, США).
Послеоперационный ИМ или ишемию миокарда по ЭКГ устанавливали в соответствии с 4-м универсальным определением ИМ [29]. Острое повреждение миокарда диагностировали при абсолютном приросте дооперационного уровня вч-сТн I через 24 или 48 ч после операции на величину, большую 99 процентиля верхнего референсного предела, при отсутствии ЭКГпризнаков острой ишемии или повреждения миокарда [17]. Хроническое повреждение миокарда диагностировали в случае стабильного превышения вч-сТн I 99 процентиля верхнего референсного предела как до, так и после операции [17][29].
В изучаемых группах сравнивали периоперационную динамику вышеуказанных биомаркеров повреждения миокарда, частоту послеоперационных острого повреждения миокарда, ИМ и острой ишемии миокарда. Рассчитывали отношение шансов (ОШ) развития острого повреждения миокарда с 95% доверительным интервалом (ДИ). Поскольку распределение признаков в изучаемых выборках отличалось от нормального, использовали непараметрические методы статистики. Данные представлены в виде медианы (Ме) с указанием интерквартильного интервала (25%; 75%). Статистическую значимость различий определяли в независимых выборках по U Манна-Уитни, χ2, точному двустороннему критерию Фишера, в связанных – по критерию Фридмана. Отличие считалось статистически значимым при p<0,05. Применяли пакет прикладных программ Statistica 12.0 (Statsoft Inc., США).
Результаты
Изучаемые группы были сопоставимы по возрасту, полу и всем клиническим показателям, кроме доли курильщиков, длительности вмешательства и фракции выброса левого желудочка (больше в группе никорандила; рис. 1).
Содержание в крови вч-сТн I и sST2 статистически значимо увеличивалось после операции в обеих группах (табл. 2). Концентрация ИМА в обеих группах, напротив, снижалась. Пик концентрации sST2 в обеих группах и вч-сТн I в группе никорандила приходился на первые сутки после операции с последующим снижением. В то же время средние уровни вч-cТн I в группе контроля продолжали нарастать в течение двух суток после операции. При межгрупповом сравнении оказалось, что исходно значения всех изученных биомаркеров в группах не различались. После вмешательства в группе никорандила концентрации вч-cТн I и sST2 через 48 ч, как и максимальные за весь послеоперационный период были существенно ниже, чем в группе контроля.
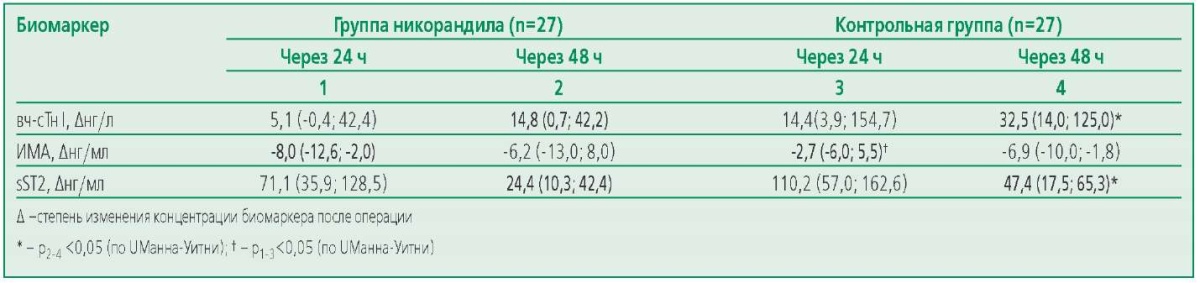
В группе никорандила степень прироста вч-cТн I и sST2 за двое суток послеоперационного периода была статистически значимо меньшей, а уровень ИМА в первые сутки после вмешательства снизился в большей степени, по сравнению с группой контроля (табл. 3).
Table 1. Clinical characteristics of patients in the study groups
Таблица 1. Клиническая характеристика пациентов в исследуемых группах
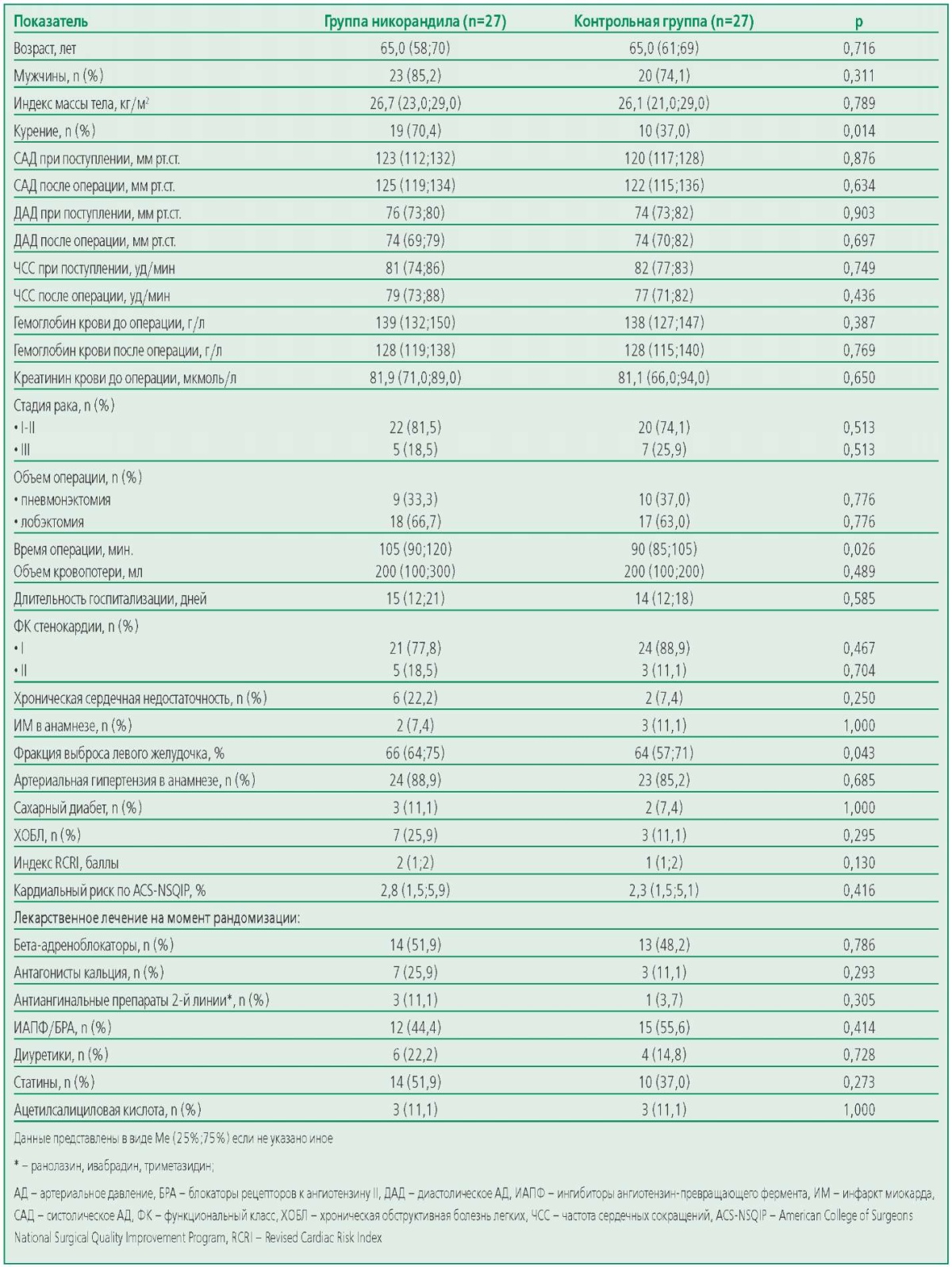
Table 2. Perioperative dynamics of myocardial injury biomarkers
Таблица 2. Периоперационная динамика биомаркеров повреждения миокарда
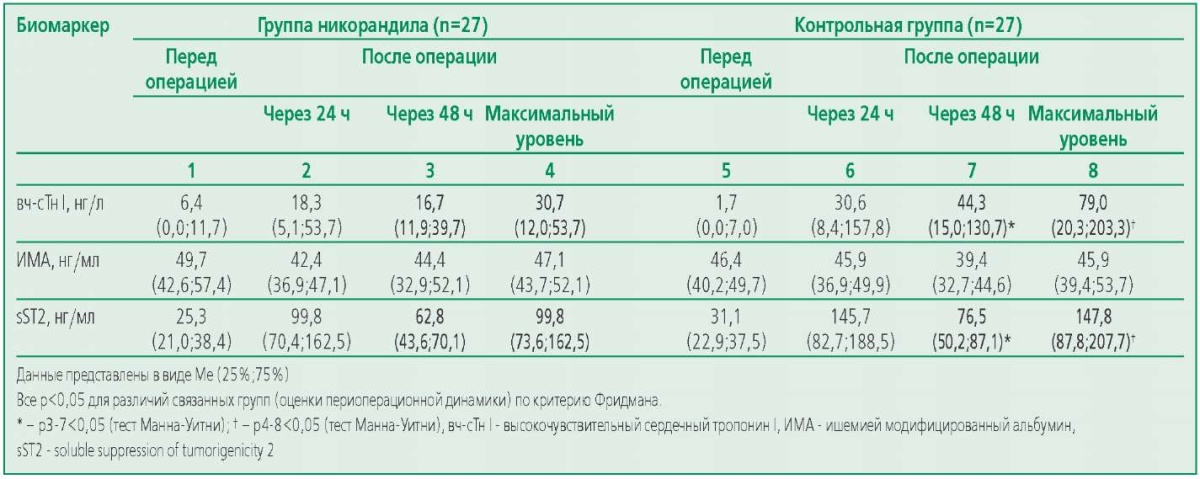
Table 3. Increase in myocardial injury biomarkers after the surgery
Таблица 3. Прирост биомаркеров повреждения миокарда после операции
У пяти пациентов группы никорандила и у трёх из контрольной группы уровни вч-сТн I до и после операции соответствовали критериям хронического повреждения миокарда. Среди 54 пациентов обеих групп острое повреждение миокарда по периоперационной динамике вч-сТн I выявлено у 22 (40,7%). Возможные альтернативные причины повышения вчсТн I (сепсис, тромбоэмболия легочной артерии, инсульт) были исключены, что позволило предположить о наличии ПМВО у данных пациентов. Однако ни у одного из них повышение вч-сТн I не сопровождалось типичными ангинозными болями.
Доля пациентов с острым повреждением миокарда в группе никорандила была статистически значимо меньшей, чем в группе контроля (рис. 1). Отношение шансов развития острого повреждения миокарда при приеме никорандила в однофакторной регрессии составило 0,28 (95% ДИ 0,09-0,88; р=0,03). При включении в регрессионную модель, помимо приема никорандила, возраста, пола, индекса массы тела, а также фракции выброса левого желудочка, статуса курения и длительности операции (показателей, различающихся в группах), обратная взаимосвязь острого приема никорандила и повреждения миокарда сохранила свою значимость (ОШ 0,35; 95% ДИ 0,150,83; р=0,017).
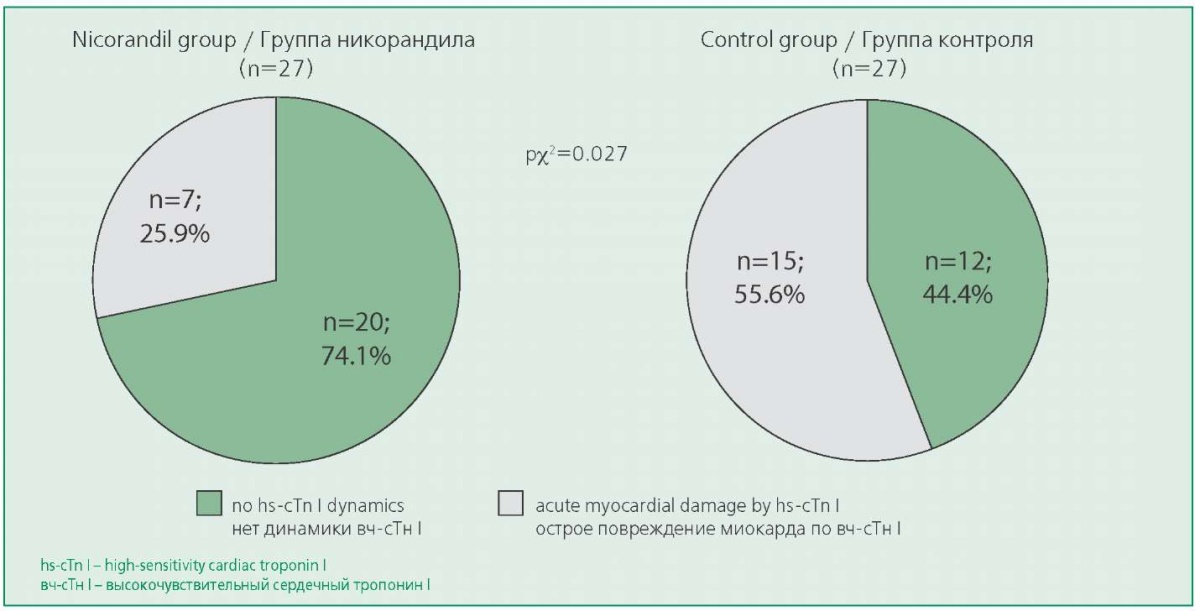
Figure 1. The incidence of acute myocardial injury in the study groups
Рисунок 1. Частота острого повреждения миокарда в изучаемых группах
Среди всех пациентов зарегистрирован один летальный исход от легочной эмболии на третьи сутки после операции (в группе никорандила). Хирургические осложнения в раннем послеоперационном периоде в виде гемофиброторакса и несостоятельности швов культи бронха развились у двух мужчин контрольной группы. Периоперационный ИМ в первые двое суток после операции выявлен у двух пациентов контрольной группы (один – с подъемом сегмента ST ЭКГ, один – без стойкого подъема ST). У 3 пациентов (у 2 из группы никорандила и у 1 из группы контроля) в раннем послеоперационном периоде отмечены ЭКГ-признаки острой ишемии миокарда без закономерной для ИМ динамики вч-сТн I. В группе пациентов, подвергнутых хирургическому лечению рака легкого, частота периоперационного ИМ составила 3,7%, острой ишемии миокарда – 5,6%. Различия по частоте событий в группах отсутствовали. Лишь у одной пациентки ЭКГпризнаки острой ишемии миокарда сопровождались загрудинным дискомфортом. Остальные случаи ИМ и острой ишемии миокарда (4 из 5; 80,0%) протекали бессимптомно.
Обсуждение
С целью поиска новых подходов к медикаментозной профилактике синдрома повреждения миокарда после внесердечных операций нами исследована динамика биомаркеров повреждения миокарда под влиянием никорандила. Результаты исследования показали, что операция в объеме торакотомии в 40,7% случаев сопровождалась острым бессимптомным повреждением миокарда, из которых только 3,7% соответствовали критериям послеоперационного ИМ. Результаты работы подтверждают данные других авторов о высокой частоте ПМВО в экстракардиальной хирургии при использовании вч-сТн, достигающей 50% [4][5]. Механизмы ПМВО окончательно не установлены. Предполагается, что хирургическое вмешательство сопровождается стрессовым ответом организма на повреждение тканей. Происходит выброс нейроэндокринных медиаторов, факторов воспаления. Развиваются анемия вследствие кровопотери, электролитные сдвиги, изменения центральной гемодинамики и нарушения ритма, гипоксия. Все это может приводить к ишемии и ишемическому повреждению миокарда [30].
Нами впервые установлено, что у пациентов с ИБС прием никорандила в предоперационном периоде был ассоциирован с меньшей в два раза, чем в группе контроля, частотой развития ПМВО, меньшим уровнями и степенью прироста вч-сТн I через 48 ч после операции. Прием никорандила был ассоциирован со снижением шанса развития острого повреждения миокарда по вч-сТн I на 65% несмотря на бо́льшую долю курильщиков и длительность вмешательства в группе (что могло увеличить риск осложнений). Высокочувствительный сТн является общепризнанным высокоспецифичным маркером ишемии и ишемического повреждения миокарда. В некардиальной хирургии послеоперационный прирост уровня вч-сТн I явился предиктором неблагоприятных сердечно-сосудистых событий и смертности [31]. Таким образом, меньшая степень прироста вч-сТн I при приеме никорандила может сопровождаться снижением риска кардиальных событий после торакальных хирургических вмешательств.
Нами впервые исследована динамика ИМА – одного из наиболее ранних биомаркеров ишемии/повреждения миокарда – после торакальных внесердечных хирургических операций. В отличие от вч-сТн I, уровень ИМА в послеоперационном периоде снижался в обеих группах, в большей степени в группе никорандила. Ранее серийные измерения концентрации ИМА проводились у пациентов, подвергшихся коронарному шунтированию. Результаты оказались противоречивыми. По данным M. Thielmann и соавт. уровень ИМА резко снижался в первый час после операции, затем в течение суток возвращался к исходному уровню и превышал его через 72 ч после операции, что, в целом, соответствует динамике ИМА в нашей выборке. Однако ИМА не увеличивался у пациентов с ИМ, вызванного коронарным шунтированием [32]. По другим сведениям, пик концентрации ИМА отмечался интраоперационно или сразу после операции с последующим снижением [33-35]. В нашей работе первое послеоперационное измерение ИМА осуществлялось через 24 ч после операции, что, возможно, не позволило зафиксировать ранний пик его концентрации, связанный с интраоперационной ишемией миокарда. При этом было зарегистрировано типичное для ИМА постпиковое его снижение. Итак, полученные данные не позволяют сделать обоснованный вывод о закономерностях динамики ИМА после внесердечных операций, его диагностическом и прогностическом значении. Остается неясным, почему степень снижения ИМА в группе никорандила оказалась более выраженной.
Уровни sST2 в обеих исследуемых группах существенно повысились на вторые сутки после операции, снизились на третьи сутки, не достигнув при этом дооперационного уровня. Аналогичная динамика sST2 (максимальный подъем на вторые сутки в среднем до 155 нг/мл с последующим снижением) отмечена в единственной опубликованной на данную тему работе, в которой уровни биомаркера определялись у 175 пациентов, перенесших внесердечную операцию [36]. При этом повышение sST2 было ассоциировано с увеличением риска больших неблагоприятных сердечно-сосудистых событий в течение 30 дней после вмешательства. В отличие от нашего исследования, в данной работе большинство вмешательств были абдоминальными и нейрохирургическими, а концентрация sST2 не определялась до операции [36]. Сравнительный анализ динамики sST2 показал, что в группе никорандила медианы уровней sST2 на третьи сутки и наибольших за послеоперационный период, а также степень прироста sST2 через 48 ч после вмешательства были ниже, чем в группе контроля. Уменьшение степени прироста sST2 может указывать на повышение под воздействием никорандила устойчивости кардиомиоцитов к перегрузке и ишемическому повреждению при многофакторном воздействии хирургического стресса.
Таким образом, полученные нами данные позволяют предполагать наличие у никорандила кардиопротективной активности у хирургических пациентов с ИБС. S. Kashimoto и соавт. в многоцентровом исследовании выявили снижение частоты ИМ, изменений ST-T на ЭКГ, аритмий, артериальной гипотензии после внесердечных операций под влиянием никорандила, при этом препарат вводился парентерально непосредственно во время операции [37]. Отечественными авторами изучена эффективность никорандила (Кординик®, компания ПИК-ФАРМА) в профилактике перипроцедурных осложнений у пациентов с ИБС, подвергающихся плановому чрескожному коронарному вмешательству. Было показано, что на фоне приема никорандила частота развития инфаркта миокарда 4а типа снижалась с 12% до 3% [24]. Данный феномен авторы объясняют способностью никорандила вызывать эффект фармакологического прекондиционирования, доказанный в экспериментальных исследованиях [19]. Эффективность дистантного ишемического прекондиционирования в профилактике ПМВО при хирургическом лечении переломов бедра была доказана в рандомизированном клиническом исследовании PIXIE [38]. Можно предположить, что этот механизм вносит вклад в кардиопротективное действие никорандила у пациентов, подвергающихся внесердечным хирургическим вмешательствам.
Ограничения исследования. Ограничениями работы может явиться относительная немногочисленность исследуемых групп и отсутствие полной картины послеоперационной динамики ИМА, так как протоколом не было предусмотрено определение уровня ИМА в первые часы после операции. Перспективой дальнейших изысканий по данной проблеме является проведение контролируемого исследования никорандила для оценки его способности снижать риск больших неблагоприятных сердечно-сосудистых событий после внесердечных хирургических вмешательств.
Заключение
Прием никорандила (Кординик®, компания ПИКФАРМА) в предоперационном периоде у пациентов с раком легкого и сопутствующей ИБС, подвергшихся хирургической резекции легкого, ассоциирован с меньшим послеоперационным приростом вч-сТн I и sST2 и снижением риска развития острого повреждения миокарда, что может свидетельствовать кардиопротективном эффекте никорандила в условиях острого хирургического стресса.
Отношения и деятельность. Предоставление ООО «ПИК-ФАРМА» лекарственного препарата и средств для приобретения реактивов организации, где выполнялась работа.
Relationships and Activities. PIK-PHARMA LLC provided a drug and funds for the purchase of reagents for the study.
Финансирование. Исследование проведено при поддержке компании ООО «ПИК-ФАРМА».
Funding. The study was conducted with the support of PIK-PHARMA LLC.
Список литературы
1. Smilowitz NR, Gupta N, Guo Y, et al. Perioperative acute myocardial infarction associated with non-cardiac surgery. Eur Heart J. 2017;38(31):2409-17. DOI:10.1093/eurheartj/ehx313.
2. Здравоохранение в России 2021. М.: Росстат; 2021.
3. Botto F, Alonso-Coello P, Chan MT, et al. Myocardial injury after noncardiac surgery: a large, international, prospective cohort study establishing diagnostic criteria, characteristics, predictors, and 30-day outcomes. Anaesthesiology. 2014;120(3):564-78. DOI:10.1097/ALN.0000000000000113.
4. van Lier F, Wesdorp FHIM, Liem VGB, et al. Association between postoperative mean arterial blood pressure and myocardial injury after noncardiac surgery. Br J Anaesth. 2018;120(1):77-83. DOI:10.1016/j.bja.2017.11.002.
5. Lee SH, Park MS, Song YB, et al. Perioperative myocardial injury in revascularized coronary patients who undergo noncardiac surgery. PLoS One. 2019;14(6):е0219043. DOI:10.1371/journal. pone.0219043.
6. Kim M, Son M, Lee DH, et al. Troponin-I Level After Major Noncardiac Surgery and Its Association With Long-Term Mortality. Int Heart J. 2016;57(3):278-84. DOI:10.1536/ihj.15-352.
7. Biccard BM, Scott DJA, Chan MTV, et al. Myocardial Injury After Noncardiac Surgery (MINS) in Vascular Surgical Patients: A Prospective Observational Cohort Study. Ann Surg. 2018;268(2):357-63. DOI:10.1097/SLA.0000000000002290.
8. Smilowitz NR, Redel-Traub G, Hausvater A, et al. Myocardial Injury after Non-Cardiac Surgery: A Systematic Review and Meta-analysis. Cardiol Rev. 2019;27(6):267-73. DOI:10.1097/CRD.0000000000000254.
9. Большедворская О.А., ПротасовК.В., Батунова Е.В., Семенова Е.Н. Биомаркеры повреждения миокарда при хирургическом лечении рака легкого: периоперационная динамика и прогностическое значение. Комплексные Проблемы Сердечно-сосудистых Заболеваний. 2022;11(2):27-38. DOI:10.17802/2306-1278-2022-11-2-27-38.
10. Rodseth RN, Biccard BM, Le Manach Y, et al. The prognostic value of pre-operative and post-operative B-type natriuretic peptides in patients undergoing noncardiac surgery: B-type natriuretic peptide and N-terminal fragment of pro-B-type natriuretic peptide: a systematic review and individual patient data meta-analysis. J Am Coll Cardiol. 2014;63(2):170-80. DOI:10.1016/j.jacc.2013.08.1630.
11. Чаулин А.М., Дупляков Д.В. Биомаркеры острого инфаркта миокарда: диагностическая и прогностическая ценность. Часть 1. Клиническая Практика. 2020;11(3):75-84. DOI:10.17816/clinpract34284.
12. Shevtsova A, Gordiienko I, Tkachenko V, Ushakova G. Ischemia-Modified Albumin: Origins and Clinical Implications. Dis Markers. 2021;2021:9945424. DOI:10.1155/2021/9945424.
13. Aleksova A, Paldino A, Beltrami AP, et al. Cardiac Biomarkers in the Emergency Department: The Role of Soluble ST2 (sST2) in Acute Heart Failure and Acute Coronary Syndrome-There is Meat on the Bone. J Clin Med. 2019;8(2):270. DOI:10.3390/jcm8020270.
14. Pascual-Figal DA, Januzzi JL. The biology of ST2: the International ST2 Consensus Panel. Am J Cardiol. 2015;115(7 Suppl):3B-7B. DOI:10.1016/j.amjcard.2015.01.034.
15. Dudek M, Kałużna-Oleksy M, Migaj J, Straburzyńska-Migaj E. Clinical value of soluble ST2 in cardiology. Adv Clin Exp Med. 2020;29(10):1205-10. DOI:10.17219/acem/126049.
16. Barbarash O, Gruzdeva O, Uchasova E, et al. Prognostic Value of Soluble ST2 During Hospitalization for ST-Segment Elevation Myocardial Infarction. Ann Lab Med. 2016;36(4):313-9. DOI:10.3343/alm.2016.36.4.313.
17. Halvorsen S, Mehilli J, Cassese S, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J. 2022;43(39):3826-924. DOI:10.1093/eurheartj/ehac270.
18. Лукина Ю.В., Кутишенко Н.П., Марцевич С.Ю. Эффективность, безопасность и отдаленные исходы применения никорандила у больных стабильной ишемической болезнью сердца по данным рандомизированного и наблюдательного исследований. Рациональная Фармакотерапия в Кардиологии. 2019;15(5):641-8. DOI:10.20996/1819-6446-2019-15-5-641-648.
19. Ahmed LA, Salem HA, Attia AS, Agha AM. Pharmacological preconditioning with nicorandil and pioglitazone attenuates myocardial ischemia/reperfusion injury in rats. Eur J Pharmacol. 2011;663(1-3):51-8. DOI:10.1016/j.ejphar.2011.04.038.
20. Horinaka S, Yabe A, Yagi H, Ishimitsu T, et al. Effects of nicorandil on cardiovascular events in patients with coronary artery disease in the Japanese Coronary Artery Disease (JCAD) study. Circ J. 2010;74(3):503-9. DOI:10.1253/circj.cj-09-0649.
21. IONA Study Group. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA) randomised trial. Lancet. 2002;359(9314):1269-75. DOI:10.1016/S0140-6736(02)08265-X.
22. Sakata Y, Nakatani D, Shimizu M, et al. Oral treatment with nicorandil at discharge is associated with reduced mortality after acute myocardial infarction. J Cardiol. 2012;59(1):14-21. DOI:10.1016/j.jjcc.2011.08.001.
23. Lu Y, Hu W, Song Q, Wang Q. The Efficacy and Safety of Nicorandil for Periprocedural Myocardial Injury in Patients Undergoing PCI: A Meta-Analysis. J Interv Cardiol. 2020;2020:3293587. DOI:10.1155/2020/3293587.
24. Соболева Г.Н., Гостищев Р.В., Рогоза А.Н., и др. Влияние фармакологического прекондиционирования никорандилом перед плановым чрескожным коронарным вмешательством на отдаленный прогноз больных стабильной ишемической болезнью сердца. Рациональная Фармакотерапия в Кардиологии. 2020;16(2):191-8. DOI:10.20996/1819-6446-2020-04-05.
25. Saha KK, Kumar A, Deval MM, et al. Nicorandil Infusion During Off-Pump Coronary Artery Bypass Grafting Reduces Incidence of Intra-aortic Balloon Pump Insertion. Innovations (Phila). 2016;11(2):123-7. DOI:10.1097/IMI.0000000000000242.
26. Chinnan NK, Puri GD, Thingnam SK. Myocardial protection by nicorandil during open-heart surgery under cardiopulmonary bypass. Eur J Anaesthesiol. 2007;24(1):26-32. DOI:10.1017/S0265021506000676.
27. Lee TH, Marcantonio ER, Mangione CM, et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery. Circulation. 1999;100(10):1043-9. DOI:10.1161/01.cir.100.10.1043.
28. Bilimoria KY, Liu Y, Paruch JL, et al. Development and evaluation of the universal ACS NSQIP surgical risk calculator: a decision aid and informed consent tool for patients and surgeons. J Am Coll Surg. 2013;217(5):833-42.e1-3. DOI:10.1016/j.jamcollsurg.2013.07.385
29. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019;40(3):237-69. DOI:10.1093/eurheartj/ehy462.
30. Uchoa RB, Caramelli B. Troponin I as a mortality marker after lung resection surgery - a prospective cohort study. BMC Anesthesiol. 2020;20(1):118. DOI:10.1186/s12871-020-01037-3.
31. Zhang Y, Xue J, Zhou L, et al. The predictive value of high-sensitive troponin I for perioperative risk in patients undergoing gastrointestinal tumor surgery. EClinicalMedicine. 2021;40:101128. DOI:10.1016/j.eclinm.2021.101128.
32. Thielmann M, Pasa S, Holst T, et al. Heart-Type Fatty Acid Binding Protein and Ischemia-Modified Albumin for Detection of Myocardial Infarction After Coronary Artery Bypass Graft Surgery. Ann Thorac Surg. 2017;104(1):130-7. DOI:10.1016/j.athoracsur.2016.10.051.
33. Sbarouni E, Georgiadou P, Panagiotakos D, et al. Increased ischaemia modified albumin following coronary artery bypass grafting. Biomarkers. 2009;14(1):38-42. DOI:10.1080/13547500902730706.
34. Kanko M, Yavuz S, Duman C, at al. Ischemia-modified albumin use as a prognostic factor in coronary bypass surgery. J Cardiothorac Surg. 2012;7:3. DOI:10.1186/1749-8090-7-3.
35. Dong SY, Wang XJ, Xiao F, et al. Detection of perioperative myocardial infarction with ischemia-modified albumin. Asian Cardiovascular and Thoracic Annals. 2012;20(3):252-6. DOI:10.1177/0218492311434947.
36. Yang HS, Hur M, Yi A, Kim H, Kim J. Prognostic Role of High-sensitivity Cardiac Troponin I and Soluble Suppression of Tumorigenicity-2 in Surgical Intensive Care Unit Patients Undergoing Non-cardiac Surgery. Ann Lab Med. 2018;38(3):204-11. DOI:10.3343/alm.2018.38.3.204.
37. Kashimoto S, Seki M, Ishiguro T, et al. Nicorandil decreases cardiac events during and after noncardiac surgery. J Clin Anesth. 2007;19(1):44-8. DOI:10.1016/j.jclinane.2006.05.023.
38. Ekeloef S, Homilius M, Stilling M, et al. The effect of remote ischaemic preconditioning on myocardial injury in emergency hip fracture surgery (PIXIE trial): phase II randomised clinical trial. BMJ. 2019;367:l6395. DOI:10.1136/bmj.l6395.
Об авторах
К. В. ПротасовРоссия
Протасов Константин Викторович.
Иркутск
О. А. Барахтенко
Россия
Барахтенко Ольга Александровна.
Иркутск
Е. В. Батунова
Россия
Батунова Елена Владимировна.
Иркутск
Е. A. Распутина
Россия
Распутина Евгения Анатольевна.
Иркутск
Рецензия
Для цитирования:
Протасов К.В., Барахтенко О.А., Батунова Е.В., Распутина Е.A. Частота и выраженность острого повреждения миокарда после торакальных хирургических вмешательств: эффекты никорандила. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):17-25. https://doi.org/10.20996/1819-6446-2023-01-08
For citation:
Protasov K.V., Barahtenko O.A., Batunova E.V., Rasputina E.A. Incidence and Severity of Acute Myocardial Injury after Thoracic Surgery: Effects of Nicorandil. Rational Pharmacotherapy in Cardiology. 2023;19(1):17-25. (In Russ.) https://doi.org/10.20996/1819-6446-2023-01-08

















































