Перейти к:
Анализ применения ингибиторов PCSK9 в клинической практике
https://doi.org/10.20996/1819-6446-2023-02-01
Аннотация
Цель. Проанализировать опыт применения в клинической практике ингибитора PCSK9 (алирокумаба) у пациентов очень высокого сердечно-сосудистого риска по данным наблюдения в условиях дневного стационара многопрофильной клиники.
Материал и методы. В наблюдательном исследовании оценены данные у 31 пациентов (23 мужчин и 8 женщин; средний возраст 59,4±5,8 лет) очень высокого сердечно-сосудистого риска с атерогенной дислипидемией и отсутствием достижения целевых уровней липидов. Алирокумаб вводился в дозе 150 мг подкожно 1 раз в 2 нед в условиях дневного стационара многопрофильной клиники. Критерием оценки эффективности являлись доля пациентов, достигших целевого уровня ХС ЛНП и доля пациентов со снижением исходного уровня ХС ЛНП≥50%. Для оценки безопасности исследовались активность печеночных трансаминаз, уровень креатинина и гликемии, а также нежелательные лекарственные реакции.
Результаты. Применение алирокумаба (в среднем 7,5±2,3 мес) в условиях дневного стационара многопрофильной клиники хорошо переноситься, с отсутствием побочных реакций, и не имеет «синдрома отмены». У 90% пациентов достигнут либо целевой уровень ХС ЛНП <1,4 ммоль/л, либо снижения уровня ХС ЛНП на 50% и более, а у трети – достигнуты оба целевых показателя. В первые месяцы приема алирокумаба можно выделить группу пациентов с хорошим ответом на препарат.
Заключение. Результаты проведенной оценки эффективности применения алирокумаба в дозе 150 мг подкожно 1 раз в 2 нед показали, что для терапии алирокумабом в условиях дневного стационара многопрофильной больницы характерна хорошая переносимость с отсутствием нежелательных реакций и высокая эффективность препарата.
Для цитирования:
Волкова С.Ю., Боярская Л.А., Торопыгин П.Ю., Морозов И.A., Боярская Е.А. Анализ применения ингибиторов PCSK9 в клинической практике. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):43-49. https://doi.org/10.20996/1819-6446-2023-02-01
For citation:
Volkova S.Yu., Boyarskaya L.A., Toropygin P.Yu., Morozov I.A., Boyarskaya E.A. Analysis of The Use of PCSK9 Inhibitors in Clinical Practice. Rational Pharmacotherapy in Cardiology. 2023;19(1):43-49. (In Russ.) https://doi.org/10.20996/1819-6446-2023-02-01
Введение
В 2017 г. в Российской Федерации (РФ) зарегистрирован алирокумаб – представитель нового класса гиполипидемических средств. В настоящее время вопросам применения человеческих моноклональных антител в терапии гиперхолестеринемии в России за последнее 5 лет посвящено около 300 публикаций (в том числе 40 статей), в основном касающихся механизма действия ингибиторов пропротеиновой конвертазы субтилизин-кексин типа 9 (PCSK9), результатов международной программы ODYSSEY [1], и достаточно кратко показывающих опыт применения PCSK9 в клинической практике (по данным www.elibrary.ru). Всего за эти годы в РФ проведено 6 многоцентровых исследований, вне рамок программы ODYSSEY, включающих преимущественно пациентов с семейной гиперхолестеринемией [2-6]. Особенностью PCSK9 является воздействие на уровень липопротеидов низкой плотности.
Эффективность и безопасность препарата подтверждены неоднократно [7], но как мы знаем, клиническая практика может расходится с данными рандомизированных исследований.
Цель исследования – проанализировать опыт применения в клинической практике ингибитора PCSK9 (алирокумаба) у пациентов очень высокого сердечно-сосудистого риска по данным наблюдения в условиях дневного стационара многопрофильной клиники.
Материал и методы
Дизайн исследования
В обсервационное исследование включались пациенты, наблюдавшиеся в дневном стационаре Тюменской больницы ФГБУЗ «Западно-Сибирского медицинского центра Федерального медико-биологического агентства России» (г. Тюмень) с июля 2021 г. Продолжительность набора в исследование составила 6 мес. Участвующие в исследование пациенты в условиях дневного стационара 1 раз в 2 нед получали за счет средств обязательного медицинского страхования ингибитор PCSK9 (алирокумаб) 150 мг подкожно (через систему шприц-ручка). В динамике терапии ежеквартально оценивались показатели липидного спектра, уровни трансаминаз, общего билирубина, креатинина, глюкозы, контролировалась электрокардиограмма, нежелательные лекарственные реакции при каждом введении препарата (наличие местных реакций на введение препарата, а также другие нежелательные реакции, описанные в инструкции к препарату) [8].
Критерии включения: возраст >18 лет, наличие сердечно-сосудистого заболевания без декомпенсации (отсутствие госпитализации или обращения за экстренной или неотложной помощью по причине основного сердечно-сосудистого заболевания в течении предшествующих 3 мес), очень высокий сердечнососудистый риск; отсутствие достижения целевого уровня холестерина липопротеидов низкой плотности (ХС ЛНП) при применении двойной гиполипидемической терапии с максимальными дозами статина и эзетимиба в течении предшествующих 3 мес, подписанное информированное добровольное согласие.
Критерии невключения: отказ от терапии ингибитором PCSK9; наличие других хронических неинфекционных заболеваний (не сердечно-сосудистых) за исключением сахарного диабета 2 типа; нуждающихся в госпитализации или коррекции терапии; подтверждение инфицирования новой коронаровирусной инфекцией (по данным ПЦР-теста).
В качестве конечных точек учитывалось развитие острого коронарного синдрома, острого нарушения мозгового кровообращения, транзиторных ишемических атак, выполненная в период наблюдения реваскуляризация миокарда, сердечно-сосудистая смерть. Оценка конечных точек исследования проводилась на основе предоставленной медицинской документации (запрашиваемой при пропуске пациентом срока явки для введения препарата).
Критериями оценки эффективности являлись: отсутствие конечных точек; доля пациентов, достигших целевого уровня ХС ЛНП; доля пациентов со снижением исходного уровня ХС ЛНП ≥50%. Безопасность оценивалась на основании клинических данных (отсутствие нежелательных реакций) и лабораторных показателей (отсутствие значений за пределами диапазона нормального распределения).
Этическая экспертиза
Исследование проведено в соответствии с принципами Хельсинской декларации. Этическая экспертиза о положительном решении относительно возможности проведения данного клинического исследования проведена в Комитете по этике при ФГБОУ ВО Тюменском ГМУ Минздрава России, протокол № 100 от 11 июня 2021 г. Все пациенты, принимающие участие в исследовании, подписали информированное добровольное согласие.
Статистический анализ
Размер выборки предварительно не рассчитывался и определен фактическим набором пациентов в исследование. Для анализа данных использована программа Statistica 22.0 (Statsoft Inc., США). Распределение числовых признаков, анализированное по критерию Колмогорова-Смирнова соответствовало распределению Гаусса, соответственно, для них рассчитаны средние значения и стандартное отклонение. Данные представлены в виде среднего (M) и стандартного отклонения (SD). Для определения статистической значимости различий использовали непарный t-критерий Стьюдента. Сравнение трех и более независимых групп по количественному показателю, имеющему нормальное распределение, выполнялось с помощью однофакторного дисперсионного анализа ANOVA (исключались случае с числом наблюдений менее 5). Различия считали статистически значимыми при р<0,05.
Результаты
Всего критериям включения в исследование соответствовало 39 пациентов: 28 мужчин и 11 женщин. После первого месяца исследования от дальнейшего участия отказались 3 мужчин и 1 женщина, после второго – еще 2 женщины и 2 мужчин. Причиной отказа в одном случае было инфицирование новой коронаровирусной инфекцией, в остальных – затруднение в явке на очередное введение препарата в связи с удаленностью проживания (по мнению пациентов). Таким образом, в анализ включены данные 31 пациента. Средний период наблюдения пациентов составил 7,5±2,3 месяца.
Не менее чем трехмесячный курс введения алирокумаба был проведен у 31 человек (23 мужчин и 8 женщин), средний возраст обследованных составил 59,4±5,8 лет. У всех пациентов была ишемическая болезнь сердца и сердечная недостаточность (табл. 1). Необходимо отметить, что хотя только 3 пациента неоднократно перенесли инфаркт миокарда, проведение повторной процедуры чрескожного коронарного вмешательства потребовалось 12 пациентам (38,7%).
Table 1. Concomitant pathology (n=31)
Таблица 1. Сопутствующая патология (n=31)

Все пациенты получали оптимальную медикаментозную терапию по основному и сопутствующим заболеваниям (табл. 2). Антиагреганты получали 29 пациентов (93,5%), в том числе двойную антитромбоцитарную терапию (71%), сопровождающуюся применением ингибиторов протонной помпы. В 1 (3,2%) случае пациент получал дабигатран. Ингибиторы ренин-ангиотензин-альдостероновой системы были назначены всем пациентам. Ингибиторы ангиотензинпревращаюшего фермента были представлен периндоприлом или лизиноприлом, блокаторы рецепторов ангиотензина II – лозартаном. Основным представителем класса бета-адреноблокаторов был бисопролол (n=25). Как петлевой диуретик во всех случаях использовался торасемид. В качестве антагониста минералокортикоидных рецепторов применяли спиронолактон (n=13) или эплеренон (n=3).
Table 2. Drug therapy of patients included in the analysis (n=31)
Таблица 2. Медикаментозная терапия пациентов, включенных в анализ (n=31)
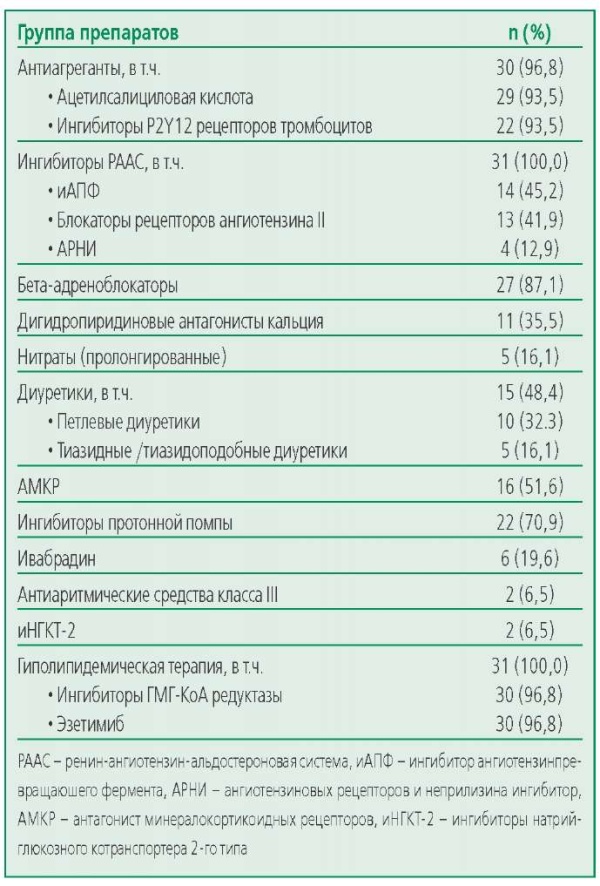
Гиполипидемическая терапия, получаемая пациентами в течении 3 мес, предшествующих включению в исследование, включала аторвастатин 80 мг/сут с эзетимибом 10 мг/сут (n=25; 80,6%), аторвастатин 40 мг /сут с эзетимибом 10 мг/сут (n=2; 6,5%), розувастатин 20 мг/сут и эзетимиб 10 мг/сут (n=2; 6,5%), эзетимиб 10 мг/сут на фоне непереносимости статинов (n=1; 3,2%), 1 (3,2%) пациент отказался от приема эзетимиба и получал аторвастатина 80 мг/сут. Всем пациентам на время исследования оставлена имеющаяся доза гиполипидемических препаратов.
За время наблюдения отмечено статистически значимое снижение уровня ХС ЛНП и общего холестерина (табл. 3). Уровень холестерина липопротеидов высокий плотности (ХС ЛВП) и триглицеридов статистически значимо не различался по сравнению с исходным значением.
Table 3. Dynamics of the lipid spectrum during the study
Таблица 3. Динамика липидного спектра за время исследования

Через 1 мес у 8 (25,8%) пациентов уровень ХС ЛНП снизился <1,4 ммоль/л, у 6 (19,4%) – <1,0 ммоль/л, у 1 (3,2%) пациента уровень ХС ЛНП снизился на 50% (не достигнув уровня 1,4 ммоль/л). После второго месяца терапии у этих же пациентов сохранялось достижение целевых показателей, при этом у всех уровень ХС ЛНП был <1,4 ммоль/л, у 9 – <1,0 ммоль/л. Таким образом целевых показателей достигли 14 (48,4%) пациентов. За время наблюдения у пациентов, регулярно применявших препарат, достигнутый эффект в виде снижения ХС ЛНП <1,4 ммоль/л сохранялся. Таких пациентов можно отнести в группу с полным ответом на проводимую терапию (группа 1).
У 13 пациентов (41,2%) за первые 2 мес приема препарата уровень ХС ЛНП несколько снижался, но не достигал целевых значений. У 10 пациентов из этой группы целевые показатели уровня ХС ЛНП <1,4 ммоль/л были достигнуты в сроки от 3 до 5 мес наблюдения (медиана 3,5 мес). Эти пациенты были отнесены в группу с неполным ответом на проводимую терапию (группа 2). Динамика снижения уровня ХС ЛНП в группах с полным и неполным ответом представлена на рис. 1.
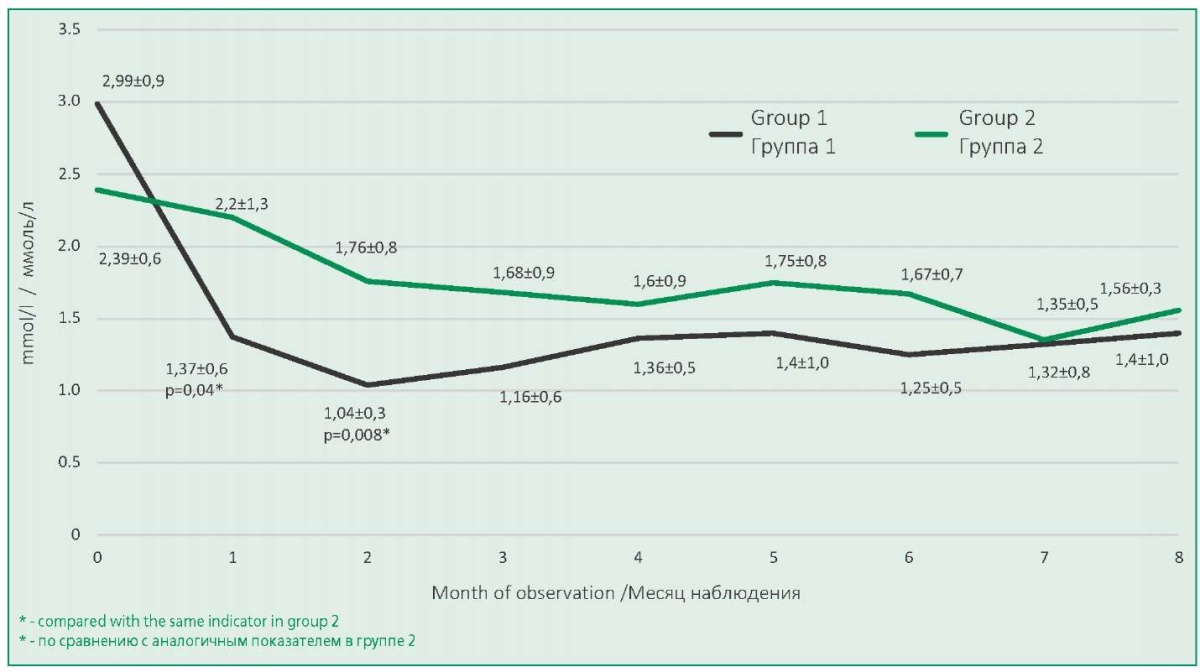
Figure 1. Dynamics of LDL-C decrease in groups with complete (Group 1) and incomplete (Group 2) response to alirocumab therapy
Рисунок 1. Динамика ХС ЛНП в группах с полным (Группа 1) и неполным (Группа 2) ответом на терапию алирокумабом
У трех пациентов на фоне начала терапии алирокумабом отмечено парадоксальное повышение уровня ХС ЛНП по сравнению с исходным. При дальнейшем наблюдении уровень ХС ЛНП несколько снижался, но менее чем на 50% от исходного.
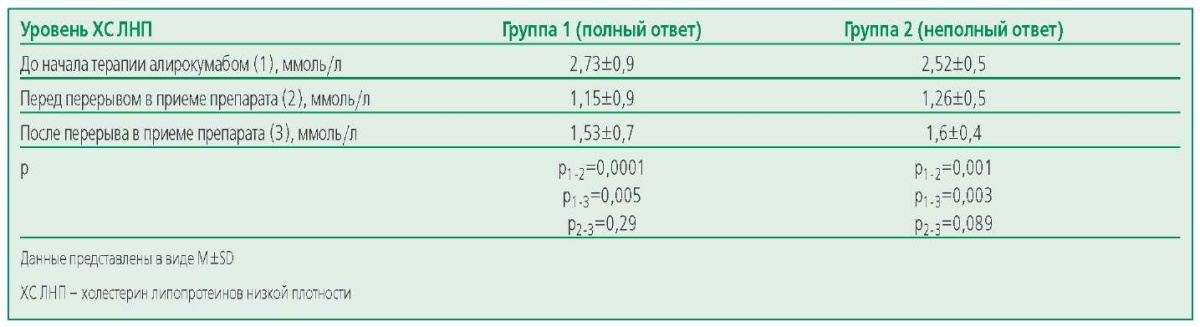
При оценке достижения критерия «снижение уровня исходного ХС ЛНП на ≥50%», в группе 1 (с полным ответом) такой результат был достигнут у 12 из 14 пациентов (85,7%) уже после первого месяца приема препарата, после второго – у всех пациентов в этой группе. В группе 2 (с неполным ответом) достижения этого целевого показателя в первый месяц не отмечено, во второй месяц терапии наблюдалось только у 4 из 13 (30,8%). В дальнейшем еще 4 пациента достигли снижения уровня ХС ЛНП на 50% и более от исходного в сроки от 4 до 6 мес (медиана 4,5 мес). По независящим от исследователей причинам в период с декабря 2021 г. по март 2022 г. 17 пациентов (9 из группы 1 и 8 из группы 2) вынуждено в течении 1 мес пропустили 2 инъекции алирокумаба. У всех пациентов до вынужденного прекращения приема препарата был достигнут целевой уровень ХС ЛНП <1,4 ммоль/л. Статистически значимого повышения уровня ХС ЛНП за время перерыва отмечено не было как в первой, так и во второй группах (табл. 4). Уровень ХС ЛНП<1,4 ммоль/л сохранялся у 5 пациентов (55,6%) в группе 1 (с полным ответом) и у 3 (37,5%) в группе 2.
Table 4. Dynamics of LDL-C during a break in taking alirocumab
Таблица 4. Динамика ХС ЛНП на фоне перерыва в приеме алирокумаба
Нежелательные явления
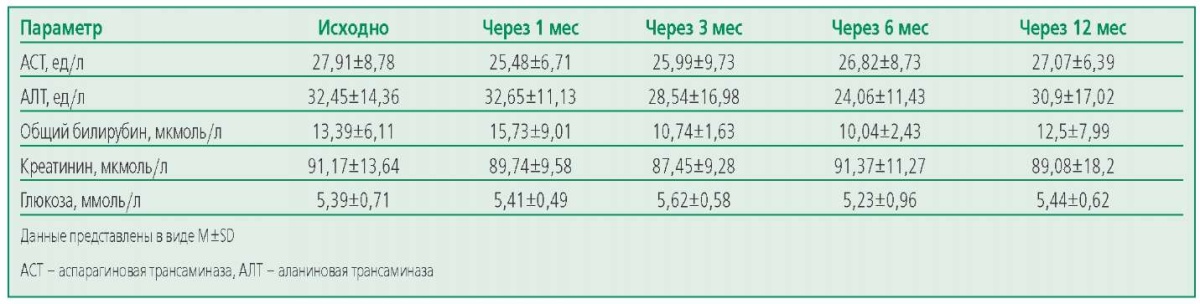
Показатели контрольных тестов: АСТ, АЛТ, общего билирубина, креатинина, глюкозы, на фоне приема препарата существенно не изменились (табл. 5). Новых случаев сахарного диабета отмечено не было. Переносимость подкожного введения препараты пациентами оценивалась как хорошая, жалоб на местные реакции не было, не было отмечено ни одного из побочных явлений, описываемых в инструкции к препарату.
Table 5. Dynamics of biochemical safety parameters during alirocumab therapy
Таблица 5. Динамика биохимических параметров безопасности на фоне терапии алирокумабом
При оценке конечных точек за время наблюдения был один летальный исход, связанный с повторным инфарктом миокарда у пациента из группы с полным ответом на терапию. За период исследования из исследования выбыло 6 пациентов из-за смены места проживания (n=2), инфицирования новой коронаровирусной инфекцией (n=1), отказа от приема препарата в условиях дневного стационара в связи с ограниченностью передвижения в условиях новой коронаровирусной инфекции (боязнь заражения; n=3).
Обсуждение
Наш опыт показал, что применение алирокумаба (на фоне двойной гиполипидемической терапии с максимальными дозами статина и эзетимиба) у пациентов очень высокого риска в клинической практике дневного стационара многопрофильной клиники показало высокую эффективность в достижении целевых уровней ХС ЛНП и приемлемую безопасность.
Необходимо отметить, что клиническая практика ставит вопросы, которые вряд ли возникали в многоцентровых исследованиях. Так, каждый пятый пациент после 1-2 мес приема препарата находил неудобство в посещении дневного стационара для инъекций несмотря на то, что финансовых затрат на препарат со стороны пациентов в нашем исследовании не было.
Исследование позволило выделить группы как с полным, так и с неполным ответом на терапию, причем соотношение этих пациентов было примерно равным. Для группы с полным ответом было характерно достижение целевых показателей в виде снижения целевого уровня ХС ЛНП <1,4 ммоль/л, либо снижения уровня ХС ЛНП на 50% и более в течении 2 мес терапии. При этом вынужденный месячный пропуск инъекций (при продолжении предшествующей гиполипидемической терапии) позволил сохранить достигнутые целевые уровни ХС ЛНП более чем у половины пациентов в этой группе. Только в этой группе были достигнуты уровни ХС ЛНП <1,0 ммоль/л у 9 пациентов (29%). Для группы с неполным ответом достижение одного или обоих показателей начиналось со 2-го месяца терапии, в среднем проходило около 3,5 мес для достижения уровня ХС ЛНП <1,4 ммоль/л и около 4,5 мес – для снижения уровня ХС ЛНП на ≥50% от исходного. Вынужденный перерыв в приеме препарата только у 37,5% больных позволил сохранить целевые уровни ХС ЛНП. Описания эффекта полного и неполного ответа на терапию алирокумабом в доступной литературе не отмечено. Достаточно интересным оказался тот факт, что три пациента в нашем исследовании показали парадоксальное повышение уровня ХС ЛНП по сравнению с исходным. При приеме препарата в дальнейшем уровень ХС ЛНП несколько снижался, но менее чем на 50% от исходного, и не достигал целевых показателей. Наличие такого разного ответа на препарат, по-видимому, связано с особенностями либо метаболизма препарата, либо особенностями рецепторов ЛНП [9], и, вероятно, может быть генетически детерминировано. Тем не менее, данных о фармакогеномике алирокумаба в настоящее время не имеется, хотя по ряду моноклональных антител такая информация представлена [10].
Наличие незапланированного перерыва в приеме препарата, позволило предположить, что у алирокумаба нет «синдрома отмены», так как уровень ХС ЛНП хоть и возрастал, но все равно был ниже исходного (на фоне продолжения приема остальных гиполипидемических препаратов). Оценки «синдрома отмены» или анализа динамики уровня ХС ЛНП в случае перерыва в приеме препарата в литературных источниках нами не найдено.
Оценивая эффективность алирокумаба, учитывая рекомендации Европейского общества кардиологов и Европейского общества по изучению атеросклероза, что «… целевым уровнем ХС ЛНП для пациентов очень высокого сердечно-сосудистого риска является показатель менее 1,4 ммоль/л, …» и помимо достижения целевого уровня, таким пациентам показано снижение уровня ХС ЛНП на 50% и более от исходного [11], можно сказать, что к 6-му мес беспрерывного приема целевые значения отмечены как в группе с полным, так и в группе с неполным ответом (90,3% от общего количества). Однако динамика достижения эффекта была соответственно разная в этих группах. В целом темп снижения ХС ЛНП мы оцениваем как благоприятный, так как снижение уровня ХС ЛНП на 1 ммоль/л за год показывает уменьшение общей смертности на 10% [12]. В нашем исследовании, в связи с его немногочисленностью, оценить снижение риска основных сердечно-сосудистых осложнений пока не представляется возможным. Уровня ХС ЛНП <1,0 ммоль/л достигла примерно треть пациентов, что сулит дальнейшие преимущества в снижении риска сердечнососудистых осложнений [13]. Ряд клинических исследований продемонстрировал, что не существует низшего предела снижения уровня ХС ЛНП, после которого польза от его снижения исчезает [14][15].
Безопасность интенсивного снижения ХС ЛНП на фоне высокодозовой гиполипидемической терапии с применением алирокумаба в дозе 150 мг подкожно раз в две недели подтверждена и отсутствием побочных явлений, в том числе местных реакций на введение препарата, а также отсутствием динамики контрольных биохимических тестов.
Ограничения исследования
Исследование носило наблюдательный характер и не предусматривало наличия группы сравнения. Результаты исследования относятся только к пациентам очень высокого сердечно-сосудистого риска и не могут быть применимы к пациентам с другим сроком приема препарата или с другой дозой вводимого препарата, а также с другой сопутствующей гиполипидемической терапией.
Заключение
Результаты проведенной оценки эффективности добавления к проводимой гиполипидемической терапии алирокумаба в дозе 150 мг подкожно с интервалом в две недели показали, что такая терапия в условиях дневного стационара многопрофильной больницы хорошо переносилась. У 90% пациентов достигнут либо целевой уровень ХС ЛНП <1,4 ммоль/л, либо снижения уровня ХС ЛНП на ≥50%, а у трети – достигнуты оба целевых показателя, что свидетельствует о высокой эффективности проводимого лечения. Прием алирокумаба уже в первые месяцы позволяет выделить группу пациентов с хорошим ответом на препарат.
Отношения и Деятельность. Нет.
Relationships and Activities. None.
Финансирование. Исследование финансировалось из бюджета Тюменской больницы ФГБУЗ ЗСМЦ ФМБА России. Назначение алирокумаба пациентам проводилось за счет средств обязательного медицинского страхования.
Funding. The study was funded from the budget of Tyumen Hospital FGBUZ West Siberian Medical Center FMBA of Russia. Alirocumab was administered to patients from the compulsory medical insurance fund.
Список литературы
1. Roth EM. Alirocumab for hyperlipidemia: ODYSSEY Phase III clinical trial results and US FDA approval indications. Future Cardiol. 2016 Mar;12(2):115-28. DOI:10.2217/fca.15.78.
2. Long Term Safety Study of PRALUENT [cited 2023 Jan 10]. Available from: https://clinicaltrials.gov/ct2/show/NCT03694197.
3. An Efficacy and Safety Study of Alirocumab in Children and Adolescents With Homozygous Familial Hypercholesterolemia [cited 2023 Jan 10]. Available from: https://clinicaltrials.gov/ct2/show/NCT03510715.
4. Evaluating Effect of the Study Drug Praluent (Alirocumab) on Neurocognitive Function When Compared to Placebo [cited 2023 Jan 10]. Available from: https://clinicaltrials.gov/ct2/show/NCT02957682.
5. An 8-Week Dose-Finding Study to Evaluate the Efficacy and Safety of Alirocumab in Children and Adolescents With Heterozygous Familial Hypercholesterolemia (ODYSSEY KIDS) [cited 2023 Jan 10]. Available from: https://clinicaltrials.gov/ct2/show/NCT02890992.
6. Open Label Study of Long Term Safety Evaluation of Alirocumab (ODYSSEY OLE) [cited 2023 Jan 10]. Available from: https://clinicaltrials.gov/ct2/show/NCT01954394.
7. Чаулин А.М. Новые группы гиполипидемических препаратов, основанные на ингибировании пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9). Часть 1. Клиническая Медицина. 2020;98(11-12):739-44. DOI:10.30629/0023-2149-2020-98-11-12-739-744
8. Государственный реестр лекарственных средств. Инструкция по медицинскому применению лекарственного препарата Пралуэнт [цитировано 10.01.2023]. Доступно из: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=001d648b-2755-4dd3-9a85-1097927d0077.
9. Чаулин А.М. Александров А.Г., Александрова О.С., и др. Роль про-протеин-конвертазы субтилизин/кексин типа 9 (PCSK9) в патофизиологии атеросклероза. Медицина в Кузбассе 2019;18(4):5-15.
10. Table of Pharmacogenomic Biomarkers in Drug Labeling [cited 2023 Jan 10]. Available from: https://www.fda.gov/drugs/science-and-research-drugs/table-pharmacogenomic-biomarkers-drug-labeling.
11. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-88. DOI:10.1093/eurheartj/ehz455.
12. Baigent C, Blackwell L, Emberson J et al. Cholesterol Treatment Trialists’ (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010;376(9753):1670-81. DOI:10.1016/S0140-6736(10)61350-5.
13. Wiviott SD, Cannon CP, Morrow DA, et al. Can low-density lipoprotein be too low? The safety and efficacy of achieving very low low-density lipoprotein with intensive statin therapy: a PROVE IT-TIMI 22 substudy. J Am Coll Cardiol. 2005;46(8):1411-6. DOI:10.1016/j.jacc.2005.04.064.
14. Sabatine MS, Giugliano RP, Keech AC, et al. FOURIER Steering Committee and Investigators. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med. 2017;376(18):1713-22. DOI:10.1056/NEJMoa1615664.
15. Robinson JG, Rosenson RS, Farnier M, et al. Safety of Very Low Low-Density Lipoprotein Cholesterol Levels With Alirocumab. J Am Coll Cardiol. 2017;69(5):471-82. DOI:10.1016/j.jacc.2016.11.037.
Об авторах
С. Ю. ВолковаРоссия
Волкова Светлана Юрьевна.
Тюмень
Л. А. Боярская
Россия
Боярская Лариса Александровна.
Тюмень
П. Ю. Торопыгин
Россия
Торопыгин Петр Юрьевич.
Тюмень
И. A. Морозов
Россия
Морозов Иван Андреевич.
Тюмень
Е. А. Боярская
Россия
Боярская Елизавета Алексеевна.
Тюмень
Рецензия
Для цитирования:
Волкова С.Ю., Боярская Л.А., Торопыгин П.Ю., Морозов И.A., Боярская Е.А. Анализ применения ингибиторов PCSK9 в клинической практике. Рациональная Фармакотерапия в Кардиологии. 2023;19(1):43-49. https://doi.org/10.20996/1819-6446-2023-02-01
For citation:
Volkova S.Yu., Boyarskaya L.A., Toropygin P.Yu., Morozov I.A., Boyarskaya E.A. Analysis of The Use of PCSK9 Inhibitors in Clinical Practice. Rational Pharmacotherapy in Cardiology. 2023;19(1):43-49. (In Russ.) https://doi.org/10.20996/1819-6446-2023-02-01

















































