Перейти к:
Эффективность и безопасность прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий и хронической болезнью почек: систематический обзор и метаанализ клинических исследований
https://doi.org/10.20996/1819-6446-2024-3092
EDN: XZILSS
Аннотация
Цель. Провести анализ опубликованных клинических исследований с целью оценки безопасности и эффективности прямых оральных антикоагулянтов в сравнении с варфарином в популяции пациентов с фибрилляцией предсердий и хронической болезнью почек (ХБП) 4-5 стадий (С4-С5).
Материал и методы. Метаанализ проведен в соответствии с рекомендациями PRISMA на основании поиска литературы в базе данных PubMed/MEDLINE за период с 01 января 2018 года по 25 декабря 2023 года. Ключевые слова включали MeSH термины "atrial fibrillation" и "dialysis" или "hemodialysis" или "end-stage kidney disease" или "end-stage renal disease" или "advanced renal disease" или "stage 4 or 5 chronic kidney disease" или "stage 5 chronic kidney disease" и "non-vitamin K antagonist oral anticoagulants" или "direct oral anticoagulants" или "novel oral anticoagulant" или "NOAC" или "DOAC" или "dabigatran" или "apixaban" или "rivaroxaban" и "vitamin K antagonist" или "warfarin" и "outcomes". Для оценки систематической ошибки исследований использовали ROBINS-I и RoB2.
Результаты. При поиске литературы на основе избранной стратегии отобрано 1895 публикаций, часть из которых исключена в связи с несоответствием критериям включения, в итоге в анализ включены 13 исследований. В метаанализ включено 60109 пациентов из 13 исследований, 9991 из которых получали прямые оральные антикоагулянты и 50118 — варфарин. Результаты продемонстрировали, что у пациентов с ХБП С4-С5 стадий, получавших лечение прямыми оральными антикоагулянтами, ишемический инсульт/системная эмболия развивались реже на 26% в сравнении с варфарином (отношение рисков (ОР)=0,74, 95% доверительный интервал (ДИ) 0,57-0,95, p=0,02). Объединенный эффект лечения прямыми оральными антикоагулянтами продемонстрировал меньший риск возникновения больших кровотечений (ОР=0,74, 95% ДИ 0,67-0,82, p<0,001). Имелась тенденция к снижению рисков как внутричерепных кровоизлияний (ОР=0,70, 95% ДИ 0,49–1,00, p=0,05), так и массивных желудочно-кишечных кровотечений в сравнении с варфарином (ОР=0,87, 95% ДИ 0,76-1,00, p=0,05). При анализе смерти от всех причин терапия прямыми оральными антикоагулянтами была также связана с её снижением на 14% (ОР=0,86, 95% ДИ 0,80-0,92, p<0,001).
Заключение. Проведенный метаанализ показывает, что в популяции пациентов с фибрилляцией предсердий и ХБП С4 и С5 стадий терапия прямыми оральными антикоагулянтами в сравнении с варфарином ассоциируется с большей эффективностью и безопасностью в отношении снижения риска развития ишемического инсульта/системной эмболии и больших кровотечений.
Ключевые слова
Для цитирования:
Межонов Е.М., Сафиуллина З.М., Вялкина Ю.А., Шалаев С.В. Эффективность и безопасность прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий и хронической болезнью почек: систематический обзор и метаанализ клинических исследований. Рациональная Фармакотерапия в Кардиологии. 2024;20(5):514-524. https://doi.org/10.20996/1819-6446-2024-3092. EDN: XZILSS
For citation:
Mezhonov E.M., Safiullina Z.M., Vyalkina Y.A., Shalaev S.V. Effectiveness and safety of direct oral anticoagulants in patients with atrial fibrillation and chronic kidney disease: a systematic review and meta-analysis of clinical trials. Rational Pharmacotherapy in Cardiology. 2024;20(5):514-524. (In Russ.) https://doi.org/10.20996/1819-6446-2024-3092. EDN: XZILSS
Введение
У пациентов с фибрилляцией предсердий (ФП) сосуществующая хроническая болезнь почек (ХБП) представляет существенную взаимодополняющую проблему для определения оптимальной тактики лечения, позволяющей привести к оптимальному балансу риск геморрагических и ишемических осложнений. ФП и ХБП часто сосуществуют из-за сложных двунаправленных взаимодействий, и ФП способствует возникновению или прогрессированию ХБП [1, 2]. Пациенты с ФП и ХБП имеют повышенную смертность из-за парадоксального увеличения как тромбоэмболического, так и геморрагического риска [3]. Стратификация риска и лечение антикоагулянтами в данных клинических условиях остаются предметом дискуссий.
Несмотря на то, что выведение варфарина почти полностью происходит за счет метаболизма в печени, по мере снижения клиренса креатинина происходит изменение терапевтического эффекта, что может привести как к субтерапевтическому эффекту, так и к чрезмерной антикоагуляции [4][5]. Прямые оральные антикоагулянты (ПОАК) в разной степени выводятся почками, уровень почечной экскреции в порядке возрастания можно представить в следующей последовательности: апиксабан (25%), ривароксабан (33%), эдоксабан (35%) и дабигатран (80%) [6][7].
ПОАК показали стабильную эффективность и безопасность у пациентов с ХБП С1-С3 стадий в сравнении с варфарином [8][9], в тоже время остается неясным влияние ПОАК на пациентов с тяжелой ХБП С4-С5 стадий или находящихся на заместительной почечной терапии. Некоторые ПОАК (ривароксабан, апиксабан и эдоксабан) одобрены в Европе в сниженных дозировках для применения в качестве антикоагулянтов у пациентов с ФП при ХБП С4 стадии (клиренс креатинина 15-29 мл/мин) [8][10][11], но недостаточно изучена эффективность и безопасность ПОАК в группе пациентов с ФП, находящихся на диализе. Согласно рекомендациям AHA/ACC/HRS (2019) по лечению ФП, нецелесообразно использование дабигатрана, ривароксабана и эдоксабана у пациентов с терминальной стадией почечной недостаточности [6].
Таким образом, цель метаанализа — обобщение имеющихся данных о применении ПОАК в сравнении с варфарином для принятия решения относительно выбора оптимальных антикоагулянтов у пациентов с ФП и ХБП С4-С5 стадий.
Материал и методы
Метаанализ проведен в соответствии с рекомендациями "Предпочтительных элементов отчетности для систематических обзоров и руководящих принципов метаанализа" (Preferred Reporting Items for Systematic Reviews and Meta-Analyses guidelines — PRISMA) [12]. Поиск литературы проводился в базе данных PubMed/MEDLINE в период с 01 января 2018 по 25 декабря 2023 года. Ключевые слова включали MeSH термины "atrial fibrillation" и "dialysis" или "hemodialysis" или "end-stage kidney disease" или "end-stage renal disease" или "advanced renal disease" или "stage 4 or 5 chronic kidney disease" или "stage 5 chronic kidney disease" и "non-vitamin K antagonist oral anticoagulants" или "direct oral anticoagulants" или "novel oral anticoagulant" или "NOAC" или "DOAC" или "dabigatran" или "apixaban" или "rivaroxaban" и "vitamin K antagonist" или "warfarin" и "outcomes". Фильтры по типу исследования и языку не использовались. Другие критерии включения: неклапанная ФП/трепетание предсердий как показание для назначения ПОАК, наличие информации о частоте ХБП С4-С5 стадий в исследуемой выборке и представление в результатах исследования отношения рисков (ОР) развития конечных точек (ишемический инсульт, системные артериальные эмболии, большие кровотечения, внутричерепные кровоизлияния, желудочно-кишечные кровотечения, общая смертность) в течение периода наблюдения, возраст пациентов старше 18 лет. Отсутствие в исследовании группы сравнения, получающей варфарин, обзоры и мнения экспертов, а также исследования, результаты которых опубликованные только в виде тезисов, исключались из анализа, как и исследования с участием менее 10 пациентов. Дополнительно выполнен ручной поиск ссылок в отобранных статьях для обнаружения дополнительных исследований, которые могут составлять интерес. Независимо друг от друга два автора анализировали заголовки и аннотации публикации относительно соответствия критериям включения, в случае наличия разногласий публикация рассматривалась третьим автором, и разногласия ликвидировались путем обсуждения в группе авторов метаанализа. Включенные исследования были изучены для определения клинико-демографических характеристик пациентов, частоты наступления конечных точек.
Кокрейновские инструменты оценки риска систематической ошибки исследований RoB2 и ROBINS-I использовали для рандомизированных клинических исследований (РКИ) и нерандомизированных клинических исследований (неРКИ), соответственно [13]. Статистический анализ проведен с использованием программы Review Manager 5.4. Статистическую гетерогенность исследований количественно определяли с помощью Chi2 и статистики I2. Для дихотомизированных данных рассчитали ОР и 95% доверительный интервал (ДИ). Модель случайных эффектов использовалась в случае p<0,10 или I2>40%.
Результаты
На основе первоначально избранной стратегии поиска общее количество публикации составило 1895. Рассмотрев название и аннотацию статей, из дальнейшей оценки были удалены 1816 статей. После изучения полнотекстовых статей оставшихся исследований были исключены 66 статей: 12 — дубликаты статей, 20 — отсутствовала контрольная группа, 10 — описание клинических случаев, 7 — отсутствие информации о конечных точках, 17 — обзоры и мнения экспертов. В итоге в метаанализ включены 13 исследований, соответствующих критериям включения и не имеющих критериев исключения (рис. 1). Три из них являлись РКИ, оставшиеся 10 — крупными неРКИ. Клиническая характеристика исследований, включенных в метаанализ, представлена в табл. На рис. 2 представлена оценка систематической ошибки исследований с использованием инструментов RoB2 и ROBINS-I.
Только одно из 13 исследований имело общий высокий риск систематической ошибки, 4 исследования (31%) были определены как имеющие низкий общий риск, а остальные 8 (62%) — как имеющие некоторые опасения или умеренный риск относительно общего риска систематической ошибки. Исследование S. H. Chang и соавт. являлось многоцентровым ретроспективным когортным неРКИ, в которое включали пациенты в возрасте ≥65 лет в период с 2001 по 2017 гг. Таким образом, возраст в данном исследовании может выступать в качестве конфаундера, а длительный период включения не позволяет исключить влияние медикаментозной терапии вследствие изменяющихся клинических рекомендации по лечению пациентов. Кроме того, согласно протоколу исследования, имеется возможность недооценки конечных точек [1]. В работах C. I. Coleman и соавт. [2] и Y. C. Lin и соавт. [14] для выравнивания групп в многоцентровых ретроспективных когортных неРКИ использован метод псевдорандомизации, в тоже время согласно протоколу исследований отсутствовала информация об уровне креатинина и СКФ, а диагноз ХБП устанавливали по кодам международной классификации болезней. P. T. Matusik и соавт. провели одноцентровое ретроспективное когортное неРКИ с небольшим количеством исследуемых пациентов [3]. В ретроспективных когортных неРКИ C. C. Hsu и соавт. [15], L. C. See и соавт. [16] и M. R. Weir и соавт. [17] был длительный период включения пациентов, составлявший около 10 лет, в исследованиях для выравнивания групп использовали метод псевдорандомизации, но, согласно протоколам исследования, имелась возможность недооценки конечных точек. В опубликованном многоцентровом ретроспективном когортном неРКИ A. Makani и соавт. не представлена частота назначения того или иного ПОАК внутри группы пациентов с СКФ ≤30 мл/мин [18]. Исследование J. B. Wetmore и соавт. [19] также является ретроспективным когортным неРКИ и, как и другие обсервационные исследования, не может полностью контролировать гетерогенность характеристик пациентов. В многоцентровых РКИ A. S. De Vriese и соавт. [20] и RENAL-AF (S. D. Pokomey и соавт.) [21] протокол исследования позволял исследователям быть осведомленными о группе вмешательства, а RENAL-AF было остановлено досрочно из-за проблем с набором участников, не достигнув необходимого расчетного количества пациентов, определенного протоколом. В работе J. W. Stanifer и соавт. представлен субанализ РКИ ARISTOTLE для пациентов с клиренсом креатинина 25-30 мл/мин, риски систематической ошибки отсутствовали [22].
В систематический обзор и метаанализ всего включено 60109 пациентов из 13 клинических исследований. 9991 пациентов получали ПОАК, 50118 — варфарин.
Результаты метаанализа продемонстрировали, что у пациентов, получавших лечение ПОАК, ишемический инсульт/системная эмболия развивались реже на 26% в сравнении с варфарином (ОР=0,74, 95% ДИ 0,57–0,95, p=0,02), рис. 3А. Относительно безопасности антикоагулянтной терапии в исследуемой популяции пациентов объединенный эффект лечения ПОАК продемонстрировал меньший риск возникновения больших кровотечений (ОР=0,74, 95% ДИ 0,67–0,82, p<0,001), рис. 3B. Имелась тенденция к снижению риска как внутричерепных кровоизлияний (ОР=0,70, 95% ДИ 0,49–1,00, p=0,05), так и массивных желудочно-кишечных кровотечений в сравнении с варфарином (ОР=0,87, 95% ДИ 0,76–1,00, p=0,05), рис. 3С, D. При анализе смерти от всех причин в 4 исследованиях, в которых регистрировалась данная конечная точка, терапия ПОАК ассоциировалась со снижением на 14% (ОР=0,86, 95% ДИ 0,80–0,92, p<0,001), рис. 4.
По результатам статических тестов не было значимой гетерогенности различий по выраженности эффекта терапии между исследованиями для всех конечных точек, кроме ишемического инсульта/системной эмболии, в связи с чем для них была использована модель фиксированного эффекта, а для ишемического инсульта/системной эмболии — модель случайных эффектов. Оценка публикационного смещения выявила некоторое смещение публикации в сторону положительного влияния ПОАК на частоту развития ишемического инсульта/системной эмболии на диаграммах funnel plot. Для остальных конечных точек не выявлено смещения публикации в ту или иную сторону влияния ингибиторов ПОАК.
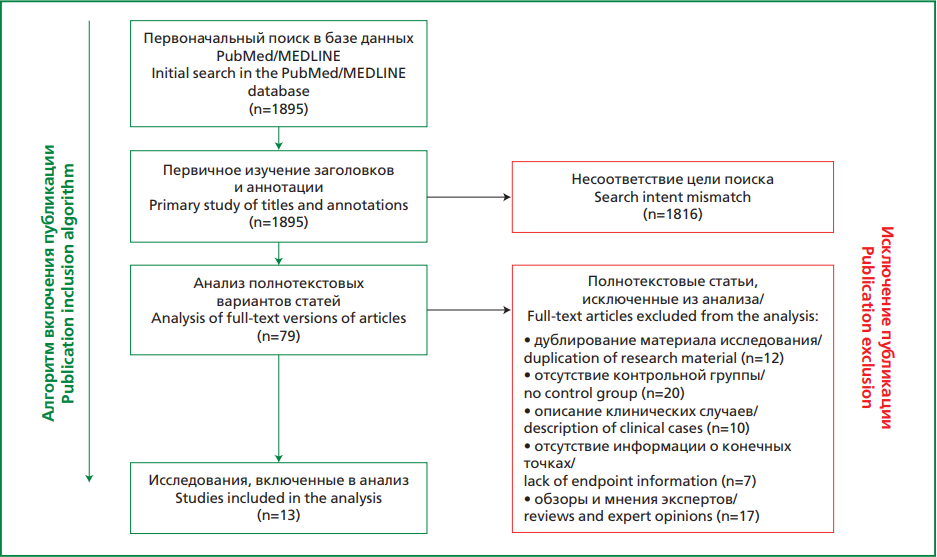
Рисунок 1. Алгоритм отбора публикаций
Таблица. Клиническая характеристика исследований, включенных в метаанализ
|
Исследование |
Год |
Возраст |
Длительность наблюдения |
Группы |
Основные результаты |
|
Исследование |
Год |
Возраст |
Длительность наблюдения |
Группы |
Основные результаты |
|
S.H. Chang и соавт. [33] |
2019 |
Медиана 78 лет (n=3771) |
Медиана 3,2 года |
ПОАК (n=280), Варфарин (n=520), 47,5٪ ХБП С5 Без оральных антикоагулянтов (n=2971), |
В сравнении с варфарином лечение ПОАК у пациентов ассоциировалось со снижением риска ишемического инсульта/системной эмболии (95٪ ДИ 0,55-1,71). |
|
C.I. Coleman и соавт. [34] |
2019 |
Медиана 72 года (63; 80) (n=6744) |
Медиана 1,4 года |
Ривароксабан (n=1896) Варфарин (n=4848) 88٪ ХБП С5 |
Ривароксабан существенно не снижал риск ишемического инсульта/системной эмболии |
|
A.S. De Vriese и соавт. [20] |
2021 |
Медиана 80,3 лет Медиана 79,9 лет (74,4; 83,9) ривароксабан (n=132) |
Медиана 1,88 года |
Ривароксабан 10 мг (n=46) Варфарин (n=44) Ривароксабан 10 мг + витамин К2 (n=42) Все пациенты ХБП С5 |
Частота больших кровотечений была ниже при приеме ривароксабана |
|
P.T. Matusik и соавт. [3] |
2020 |
70,4±7,61 лет ПОАК 68,79±7,51 лет варфарин |
26,3 месяца (от 17 до 40 месяцев) |
ПОАК (n=90): апиксабан, n=61, ривароксабан, n=29 Варфарин (n=92) Все пациенты ХБП С4 |
Не было различий в рисках системной эмболии между ПОАК и варфарином ЖКК — ОР 0,70 (95٪ ДИ 0,20-2,47), p=0,58 Большие кровотечения — ОР 1,12 (95٪ ДИ 0,53-2,39), p=0,76 Смерть от всех причин — ОР 2,22 (95٪ ДИ 0,89-5,53), p=0,09 |
|
C.C. Hsu и соавт. [15] |
2023 |
84±7,4 лет ПОАК 78,2±10,3 лет варфарин (n=1011) |
Не указано |
ПОАК (n=809), Варфарин (n=202), 33,2٪ ХБП С5 |
У ПОАК был значительно более низкий риск ишемического инсульта/системной эмболии (ОР 0,29 (95٪ ДИ 0,09-0,97), но имелся сопоставимый риск большого кровотечения |
|
Y.C. Lin и соавт. [14] |
2021 |
69±11 лет (n=3358) |
Медиана |
Ривароксабан (n=173) Варфарин (n=3185) Все пациенты ХБП С4 |
Суммарная частота серьезных кровотечений была одинаковой в двух группах (ОР 0,86 Системные эмболии — ОР 0,36 (95٪ ДИ 0,11-1,12), p=0,08. Ишемический инсульт — ОР 0,62 (95٪ ДИ 0,24-1,61), p=0,33. |
|
A. Makani и соавт. [18] |
2019 |
75,7±9,96 лет (n=1525) |
Медиана 3,4 года |
ПОАК (n=475), Варфарин (n=1050), 14٪ ХБП 5д |
В сравнении с варфарином терапия ПОАК у пациентов с нарушением функции почек была связана со снижением риска как смерти от всех причин (ОР 0,76 (95٪ ДИ 0,63-0,92), p<0,001), так и больших кровотечений (ОР 0,69 (95٪ ДИ 0,50-0,93), p=0,017). В тоже время не было статистически значимой разницы в риске возникновения ишемического инсульта (ОР 0,60 (95٪ ДИ 0,34-1,09), p=0,092) и внутричерепных кровоизлияний (ОР 0,55 (95٪ ДИ 0,19-1,61), p=0,276) |
|
S.D. Pokomey и соавт. [21] |
2022 |
68,75±4,32 лет апиксабан 67,25±3,46 лет варфарин (n=154) |
Медиана |
Апиксабан (n=82) Варфарин (n=72) Все пациенты ХБП С5д |
Частота больших или клинически значимых кровотечений в течение 1 года составила 32٪ и 26٪ в группах апиксабана и варфарина соответственно (ОР 1,20 (95٪ ДИ 0,63-2,30). |
|
L.C. See и соавт. [16] |
2020 |
74,3±10,9 лет ПОАК 75,2±10,9 лет варфарин (n=3237) |
Не указано |
ПОАК (n=490) Варфарин (n=2747) |
Не было различий в рисках ишемического инсульта/системной эмболии между ПОАК и варфарином (ОР 1,21 (95٪ ДИ 0,76-1,92), p=0,29), Внутричерепные кровоизлияния — ОР 0,78 (95٪ ДИ 0,29-2,10) ЖКК — ОР 1,06 (95٪ ДИ 0,65–1,74) Большие кровотечения — ОР 0,98 (95٪ ДИ 0,64-1,51) |
|
K.S. Sionti и соавт. [32] |
2018 |
68,2±11,9 лет (n=25523) |
Не указано |
Апиксабан (n=2351) Варфарин (n=23172) Все пациенты ХБП С5д |
Отсутствовали различия в рисках ишемического инсульта/системной эмболии между апиксабаном и варфарином (ОР 0,88 (95٪ ДИ 0,69-1,12), p=0,29), апиксабан ассоциировался с более низким риском больших кровотечений (ОР 0,72 (95٪ ДИ 0,59-0,87), p<0,001). ЖКК — ОР 0,86 (95٪ДИ 0,72-1,02), p=0,09. Внутричерепные кровоизлияния — ОР 0,79 (95٪ ДИ 0,49-1,26), p=0,32. Смерть от всех причин — ОР 0,85 (95٪ ДИ 0,71-1,01), p=0,06. |
|
J.W. Stanifer и соавт. [22] |
2020 |
Медиана 81 год (76; 85) (n=269) |
Медиана 1,8 года |
Апиксабан (n=136) Варфарин (n=133) Все пациенты ХБП С4 |
У пациентов с СКФ 25-30 мл/мин апиксабан вызывал меньшее количество больших кровотечений (ОР 0,34 (95٪ ДИ 0,14-0,80) и больших или клинически значимых незначительных кровотечений (ОР 0,35 (95٪ ДИ 0,17-0,72) по сравнению с варфарином. Риск ишемического инсульта или системной эмболии (ОР 0,55 |
|
M.R. Weir и соавт. [17] |
2020 |
79,9±8,2 лет ривароксабан 79,9±8,2 лет варфарин |
389 дней 370 дней |
Ривароксабан (n=781), ХБП С4 81,8٪ Варфарин (n=1536), ХБП С4 80,9٪ |
Статистически значимой разницы в риске возникновения ишемического инсульта/системных эмболий (ОР 0,93 (95٪ ДИ 0,46-1,90), p=0,85) и больших кровотечений (ОР 0,91 (95٪ ДИ 0,65-1,28), p=0,6) между пациентами, получавшими ривароксабан и варфарин, не было обнаружено. ЖКК — ОР 1,14 (95٪ ДИ 0,77-1,69), p=0,52 Внутричерепные кровоизлияния — ОР 0,60 (95٪ ДИ 0,22-1,68), p=0,33 |
|
J.B. Wetmore и соавт. [19] |
2022 |
n=17156 |
Не указано |
Апиксабан 5 мг х 2 (n=2382) Апиксабан 2,5 мг х 2 (n=2257) Варфарин (n=12517) |
Ишемический инсульт/системная эмболия: различий между группами апиксабан 5 мг х 2 по сравнению с варфарином нет (ОР 0,89 Большое кровотечение апиксабан 5 мг х 2 по сравнению с варфарином ОР 0,67 (95٪ ДИ 0,55-0,81), апиксабан 2,5 мг х 2 и варфарин ОР 0,68 (95٪ ДИ 0,55-0,84). Смерть от всех причин апиксабан 5 мг х 2 по сравнению с варфарином ОР 0,85 (95٪ ДИ 0,78-0,92); апиксабан 2,5 мг х 2 и варфарин ОР 0,97 (95٪ ДИ 0,89-1,05). |
|
ДИ — доверительный интервал, ЖКК — желудочно-кишечное кровотечение, ОР — отношение рисков, ПОАК — прямые оральные антикоагулянты, СКФ — скорость клубочковой фильтрации |
|||||
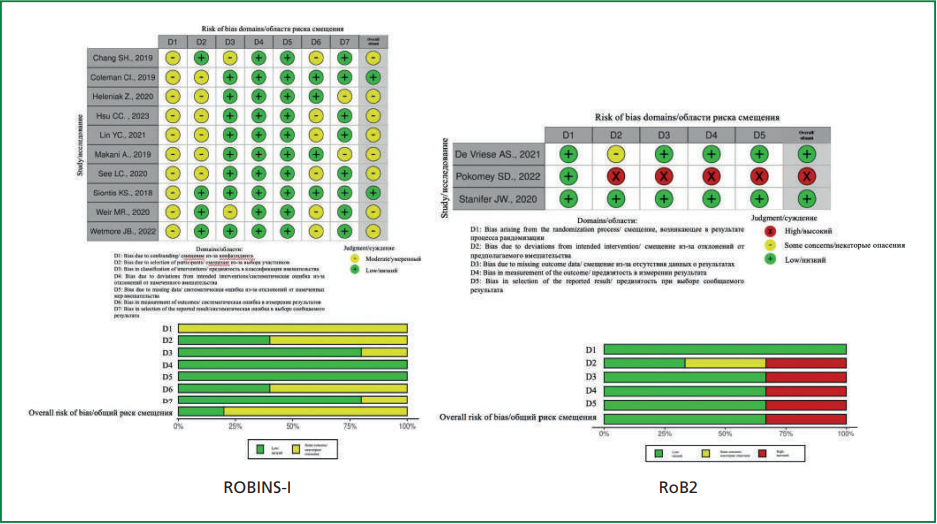
Рисунок 2. Риск систематической ошибки исследований, включенных в метаанализ
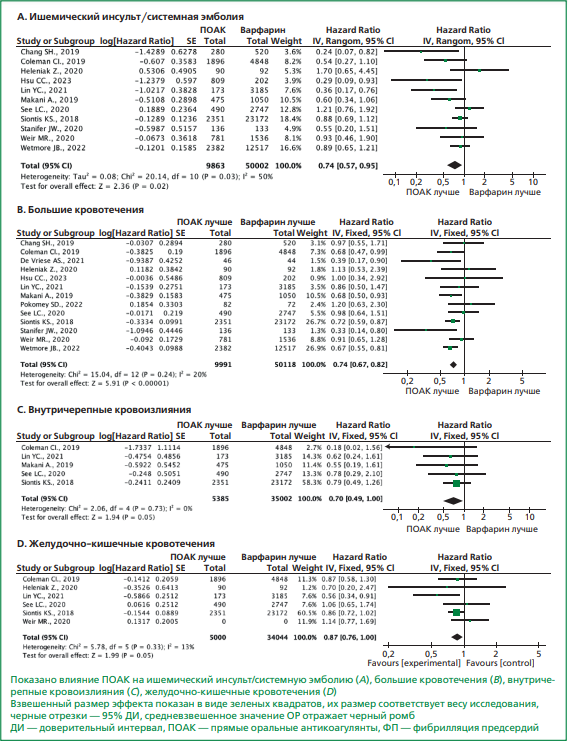
Рисунок 3. Метаанализ ПОАК в сравнении с варфарином для ишемического инсульта/системной эмболии, внутричерепных кровоизлияний, массивных желудочно-кишечных кровотечениях и всех крупных кровотечений у пациентов с неклапанной ФП и ХБП С4-С5 стадий
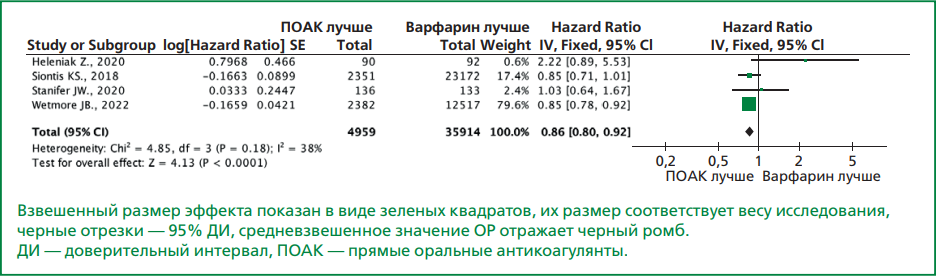
Рисунок 4. Метаанализ ПОАК в сравнении с варфарином для смерти от всех причин
Обсуждение
ПОАК — альтернатива варфарину для предотвращения инсульта при ФП и в настоящее время являются предпочтительным выбором для пациентов с ФП [11][23], поскольку оптимальные результаты применения варфарина зависят от поддержания международного нормализованного отношения (МНО) в терапевтическом диапазоне от 2 до 3, а многочисленные взаимодействия с пищевыми продуктами и другими лекарственными препаратами приводят к узкому терапевтическому окну и непредсказуемой реакции на варфарин [11][23][24]. ПОАК по сравнению с варфарином обладают улучшенным соотношением показателей эффективности и безопасности, предсказуемым антикоагулянтным действием без необходимости регулярного контроля свертываемости крови и меньшим количеством взаимодействий с пищевыми продуктами и лекарственными средствами. Ввиду исключения пациентов с клиренсом креатинина менее 15–30 мл/мин из основных РКИ в исследовательских программах ПОАК остается недостаточно изученным вопрос о применении этой группы препаратов у пациентов с ФП и тяжелой ХБП или находящихся на заместительной почечной терапии [25-27]. Основным антикоагулянтом у таких пациентов в клинической практике остается варфарин в силу того, что он не выводится почками.
ХБП является независимым фактором риска развития инсульта у пациентов с ФП [2]. В свою очередь достаточно высока распространенность ФП, включая бессимптомную, среди пациентов с ХБП 5д [28].
Ранний опыт использования дабигатрана и ривароксабана в популяции пациентов с ФП и ХБП свидетельствует о повышенном риске кровотечений по сравнению с варфарином, обусловленном более высокой дозой препаратов у части пациентов [29]. Частота серьезных кровотечений возрастала с увеличением дозы ПОАК: 69,1 и 25,4 случаев на пациенто-год при лечении дабигатраном в дозе 150 мг и 75 мг 2 раза в день соответственно, 42,6 и 23,9 случаев при лечении ривароксабаном в дозе 20 мг и 15 мг в сутки соответственно. Пациенты, находящиеся на диализе, которым назначалась полная доза дабигатрана или ривароксабана, имели более высокий риск крупного кровотечения в сравнении с пациентами, которым была назначена редуцированная доза: для дагибатрана 150 мг 2 раза в день относительный риск 2,90, 95% ДИ 1,93-4,34, p<0,0001, для ривароксабана 20 мг в сутки относительный риск 1,93, 95% ДИ 1,22-3,04, p=0,04 [29].
Ретроспективное исследование, включавшее пациентов с ФП и ХБП С3b-4 стадий, продемонстрировало, что ривароксабан был более безопасным препаратом в плане геморрагических осложнений в сравнении с варфарином [10]. В исследовании ARISTOTLE было выявлено значительно меньшее количество инсультов и больших кровотечений в группе пациентов с СКФ 25-30 мл/мин при приеме апиксабана, чем при лечении варфарином [22].
Имеющиеся данные по применению антикоагулянтов в группе пациентов с ФП и ХБП 4-5 стадий в значительной степени базируются на данных наблюдательных исследований. Проспективное многоцентровое когортное исследование пациентов с ФП, перенесших инфаркт миокарда, продемонстрировало, что назначение варфарина при выписке из стационара связано со снижением риска смерти, повторной госпитализации из-за инфаркта миокарда, ишемического инсульта и кровотечений во всем диапазоне СКФ, в том числе и среди пациентов с СКФ <25-30 мл/мин [30]. На основании результатов фармакокинетических исследований в США апиксабан получил одобрение FDA для лечения пациентов с терминальной стадией почечной недостаточности, в том числе находящихся на гемодиализе [31]. Фармакокинетическое исследование показало, что концентрация препарата при лечении пациентов на гемодиализе апиксабаном в дозировке 5 мг/сут. сопоставима с таковой при приеме апиксабана в стандартной дозировке 10 мг/сут. у пациентов с нормальной функцией почек, что позволило предположить, что 2,5 мг является более подходящей однократной дозой для таких пациентов [31]. Крупное ретроспективное когортное исследование пациентов, получавших медицинскую помощь по программе Medicare, не обнаружило различий в частоте тромбоэмболии, но выявило меньшее количество серьезных кровотечений у пациентов, получавших апиксабан по сравнению с варфарином [32].
В современных рекомендациях ACC (2023) пациентам с ФП, имеющим высокий риск развития инсульта и ХБП С3 стадии, рекомендуется лечение варфарином или, предпочтительно, прямыми ингибиторами тромбина или фактора Ха в дозах, использованных в РКИ, для снижения риска развития инсульта (класс 1, уровень B) [23]. Для пациентов с ФП, имеющих высокий риск развития инсульта и ХБП 4-й стадии, лечение варфарином или указанными в рекомендациях дозами ПОАК является разумным для снижения риска инсульта (класс 2а, уровень B). Пациентам с ФП, имеющим повышенный риск развития инсульта, а также с терминальной стадией ХБП (клиренс креатинина <15 мл/мин) или находящимся на диализе, может быть целесообразным назначение варфарина (МНО 2,0-3,0) или апиксабана в дозе, основанной на данных доказательной медицины, в качестве ПОАК для снижения риска инсульта (класс 2b, уровень B) [23].
В рекомендациях ESC (2020) позиция экспертов, касающаяся назначения антикоагулянтов у пациентов с ФП и ХБП С4-С5 стадий, заключается в том, что применение апиксабана, ривароксабана, эдоксабана у пациентов с ХБП С4 стадии (клиренс креатинина 15-29 мл/мин) может быть рассмотрено "с осторожностью" в редуцированных дозировках с учетом клиренса данных препаратов, использование дабигатрана не одобрено [11]. У пациентов с ХБП С5 стадии (клиренс креатинина <15 мл/мин) и у пациентов на диализе назначение ПОАК не одобрено [11].
Ограничения исследования
К ораничениям данного исследования следует отнести то, что большинство включенных исследований являлись ретроспективными когортными неРКИ, кроме того, в исследованиях оценивались разные ПОАК в неоднородных дозировках, продолжительность наблюдения пациентов различалась. Также использовано ОР для представления результатов, значения ОР может меняться со временем, а также при наличии возможной систематической ошибки отбора. Смерть от всех причин оценивалась только в 4 исследованиях из 13, включенных в метаанализ.
Заключение
Проведенный метаанализ показывает, что в популяции пациентов с ФП и ХБП С4 и С5 стадий терапия ПОАК ассоциируется с большей эффективностью в снижении риска ишемического инсульта/системной эмболии по сравнению с варфарином. Применительно к безопасности ПОАК в изучаемой популяции пациентов продемонстрировано снижение риска развития больших кровотечений и тенденцию к снижению риска как внутричерепных кровоизлияний, так и массивных желудочно-кишечных кровотечений в сравнении с варфарином.
Отношения и Деятельность. Нет.
Relationships and Activities. None.
Финансирование: Работа выполнена при поддержке Тюменского государственного медицинского университета.
Funding: The study was performed with the support of the Tyumen State Medical University.
Список литературы
1. Bansal N, Zelnick LR, Alonso A, et al. eGFR and Albuminuria in Relation to Risk of Incident Atrial Fibrillation: A Meta-Analysis of the Jackson Heart Study, the MultiEthnic Study of Atherosclerosis, and the Cardiovascular Health Study. Clin J Am Soc Nephrol. 2017;12(9):1386-98. DOI: 10.2215/CJN.01860217.
2. Go AS, Fang MC, Udaltsova N, et al; ATRIA Study Investigators. Impact of Proteinuria and Glomerular Filtration Rate on Risk of Thromboembolism in Atrial Fibrillation: the anticoagulation and risk factors in atrial fibrillation (ATRIA) study. Circulation. 2009;119(10):1363-9. DOI: 10.1161/CIRCULATIONAHA.108.816082.
3. Matusik PT, Heleniak Z, Undas A. Anticoagulant Treatment in Patients with Atrial Fibrillation and Chronic Kidney Disease: Practical Issues. Anatol J Cardiol. 2022;26(12):857-63. DOI: 10.5152/AnatolJCardiol.2022.2426.
4. Kumar S, Lim E, Covic A, et al. Anticoagulation in Concomitant Chronic Kidney Disease and Atrial Fibrillation: JACC Review Topic of the Week. J Am Coll Cardiol. 2019;74(17):2204-15. DOI: 10.1016/j.jacc.2019.08.1031.
5. Dahal K, Kunwar S, Rijal J, et al. Stroke, Major Bleeding, and Mortality Outcomes in Warfarin Users With Atrial Fibrillation and Chronic Kidney Disease: A MetaAnalysis of Observational Studies. Chest. 2016;149(4):951-9. DOI: 10.1378/chest.15-1719.
6. January CT, Wann LS, Calkins H, et al. 2019 AHA/ACC/HRS Focused Update of the 2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society in Collaboration With the Society of Thoracic Surgeons. Circulation. 2019;140(2):e125-e151. DOI: 10.1161/CIR.0000000000000665.
7. Weber J, Olyaei A, Shatzel J. The efficacy and safety of direct oral anticoagulants in patients with chronic renal insufficiency: A review of the literature. Eur J Haematol. 2019;102(4):312-8. DOI: 10.1111/ejh.13208.
8. Steffel J, Verhamme P, Potpara TS, et al; ESC Scientific Document Group. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39(16):1330-93. DOI: 10.1093/eurheartj/ehy136.
9. Hijazi Z, Hohnloser SH, Andersson U, et al. Efficacy and Safety of Apixaban Compared With Warfarin in Patients With Atrial Fibrillation in Relation to Renal Function Over Time: Insights From the ARISTOTLE Randomized Clinical Trial. JAMA Cardiol. 2016;1(4):451-60. DOI: 10.1001/jamacardio.2016.1170.
10. Di Lullo L, Tripepi G, Ronco C, et al. Safety and effectiveness of rivaroxaban and warfarin in moderate-to-advanced CKD: real world data. J Nephrol. 2018;31(5):751-6. DOI: 10.1007/s40620-018-0501-7.
11. Hindricks G, Potpara T, Dagres N, et al; ESC Scientific Document Group. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS): The Task Force for the diagnosis and management of atrial fibrillation of the European Society of Cardiology (ESC) Developed with the special contribution of the European Heart Rhythm Association (EHRA) of the ESC. Eur Heart J. 2021;42(5):373-498. DOI: 10.1093/eurheartj/ ehaa612.
12. Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71. DOI: 10.1136/bmj.n71.
13. Higgins JP, Altman DG, Gøtzsche PC, et al; Cochrane Bias Methods Group; Cochrane Statistical Methods Group. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ. 2011;343:d5928. DOI: 10.1136/bmj.d5928.
14. Lin YC, Chen BL, Shih CM, et al. Effectiveness and safety of rivaroxaban versus warfarin in Taiwanese patients with end-stage renal disease and nonvalvular atrial fibrillation: A real-world nationwide cohort study. PLoS One. 2021;16(4):e0249940. DOI: 10.1371/journal.pone.0249940.
15. Hsu CC, Chen CC, Chou CY, et al. Effectiveness and safety of direct oral anticoagulants versus warfarin in patients with atrial fibrillation and advanced kidney disease. J Thromb Thrombolysis. 2023;56(4):518-28. DOI: 10.1007/s11239-023-02859-x.
16. See LC, Lee HF, Chao TF, et al. Effectiveness and Safety of Direct Oral Anticoagulants in an Asian Population with Atrial Fibrillation Undergoing Dialysis: A Population-Based Cohort Study and Meta-Analysis. Cardiovasc Drugs Ther. 2021;35(5):975-86. DOI: 10.1007/s10557-020-07108-4.
17. Weir MR, Ashton V, Moore KT, et al. Rivaroxaban versus warfarin in patients with nonvalvular atrial fibrillation and stage IV-V chronic kidney disease. Am Heart J. 2020;223:3-11. DOI: 10.1016/j.ahj.2020.01.010.
18. Makani A, Saba S, Jain SK, et al. Safety and Efficacy of Direct Oral Anticoagulants Versus Warfarin in Patients With Chronic Kidney Disease and Atrial Fibrillation. Am J Cardiol. 2020;125(2):210-14. DOI: 10.1016/j.amjcard.2019.10.033.
19. Wetmore JB, Weinhandl ED, Yan H, et al. Apixaban Dosing Patterns Versus Warfarin in Patients With Nonvalvular Atrial Fibrillation Receiving Dialysis: A Retrospective Cohort Study. Am J Kidney Dis. 2022;80(5):569-79.e1. DOI: 10.1053/j.ajkd.2022.03.007.
20. De Vriese AS, Caluwé R, Van Der Meersch H, et al. Safety and Efficacy of Vitamin K Antagonists versus Rivaroxaban in Hemodialysis Patients with Atrial Fibrillation: A Multicenter Randomized Controlled Trial. J Am Soc Nephrol. 2021;32(6):1474-83. DOI: 10.1681/ASN.2020111566.
21. Pokorney SD, Chertow GM, Al-Khalidi HR, et al; RENAL-AF Investigators. Apixaban for Patients With Atrial Fibrillation on Hemodialysis: A Multicenter Randomized Controlled Trial. Circulation. 2022;146(23):1735-45. DOI: 10.1161/CIRCULATIONAHA.121.054990.
22. Stanifer JW, Pokorney SD, Chertow GM, et al. Apixaban Versus Warfarin in Patients With Atrial Fibrillation and Advanced Chronic Kidney Disease. Circulation. 2020;141(17):1384-92. DOI: 10.1161/CIRCULATIONAHA.119.044059.
23. Writing Committee Members; Joglar JA, Chung MK, Armbruster AL, et al. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2024;83(1):109-279. DOI: 10.1016/j.jacc.2023.08.017.
24. Klijn CJ, Paciaroni M, Berge E, et al. Antithrombotic treatment for secondary prevention of stroke and other thromboembolic events in patients with stroke or transient ischemic attack and non-valvular atrial fibrillation: A European Stroke Organisation guideline. Eur Stroke J. 2019;4(3):198-223. DOI: 10.1177/2396987319841187.
25. Fox KA, Piccini JP, Wojdyla D, et al. Prevention of stroke and systemic embolism with rivaroxaban compared with warfarin in patients with non-valvular atrial fibrillation and moderate renal impairment. Eur Heart J. 2011;32(19):2387-94. DOI: 10.1093/eurheartj
26. Granger CB, Alexander JH, McMurray JJ, et al; ARISTOTLE Committees and Investigators. Apixaban versus Warfarin in Patients with Atrial Fibrillation. N Engl J Med. 2011;365(11):981-92. DOI: 10.1056/NEJMoa1107039.
27. Connolly SJ, Ezekowitz MD, Yusuf S, et al; RE-LY Steering Committee and Investigators. Dabigatran versus Warfarin in Patients with Atrial Fibrillation. N Engl J Med. 2009;361(12):1139-51. DOI: 10.1056/NEJMoa0905561.
28. Roberts PR, Stromberg K, Johnson LC, et al. A Systematic Review of the Incidence of Arrhythmias in Hemodialysis Patients Undergoing Long-Term Monitoring With Implantable Loop Recorders. Kidney Int Rep. 2021;6(1):56-65. DOI: 10.1016/j.ekir.2020.10.020.
29. Chan KE, Edelman ER, Wenger JB, et al. Dabigatran and Rivaroxaban Use in Atrial Fibrillation Patients on Hemodialysis. Circulation. 2015; 131(11):972-9. DOI: 10.1161/CIRCULATIONAHA.114.014113.
30. Carrero JJ, Evans M, Szummer K, et al. Warfarin, Kidney Dysfunction, and Outcomes Following Acute Myocardial Infarction in Patients With Atrial Fibrillation. JAMA. 2014;311(9):919-28. DOI: 10.1001/jama.2014.1334.
31. Mavrakanas TA, Samer CF, Nessim SJ, et al. Apixaban Pharmacokinetics at Steady State in Hemodialysis Patients. J Am Soc Nephrol. 2017;28(7):2241-8. DOI: 10.1681/ASN.2016090980.
32. Siontis KC, Zhang X, Eckard A, et al. Outcomes Associated With Apixaban Use in Patients With End-Stage Kidney Disease and Atrial Fibrillation in the United States. Circulation. 2018;138(15):1519-29. DOI: 10.1161/CIRCULATIONAHA.118.035418.
33. Chang SH, Wu CV, Yeh YH, et al. Efficacy and Safety of Oral Anticoagulants in Patients With Atrial Fibrillation and Stages 4 or 5 Chronic Kidney Disease. Am J Med. 2019;132(11):1335-43.e6. DOI: 10.1016/j.amjmed.2019.06.006.
34. Coleman CI, Kreutz R, Sood NA, et al. Rivaroxaban Versus Warfarin in Patients With Nonvalvular Atrial Fibrillation and Severe Kidney Disease or Undergoing Hemodialysis. Am J Med. 2019;132(9):1078-83. DOI: 10.1016/j.amjmed.2019.04.013.
Об авторах
Е. М. МежоновРоссия
Межонов Евгений Михайлович
Тюмень
З. М. Сафиуллина
Россия
Сафиуллина Земфира Мидхатовна
Тюмень
Ю. А. Вялкина
Россия
Вялкина Юлия Александровна
Тюмень
С. В. Шалаев
Россия
Шалаев Сергей Васильевич
Тюмень
Дополнительные файлы
Рецензия
Для цитирования:
Межонов Е.М., Сафиуллина З.М., Вялкина Ю.А., Шалаев С.В. Эффективность и безопасность прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий и хронической болезнью почек: систематический обзор и метаанализ клинических исследований. Рациональная Фармакотерапия в Кардиологии. 2024;20(5):514-524. https://doi.org/10.20996/1819-6446-2024-3092. EDN: XZILSS
For citation:
Mezhonov E.M., Safiullina Z.M., Vyalkina Y.A., Shalaev S.V. Effectiveness and safety of direct oral anticoagulants in patients with atrial fibrillation and chronic kidney disease: a systematic review and meta-analysis of clinical trials. Rational Pharmacotherapy in Cardiology. 2024;20(5):514-524. (In Russ.) https://doi.org/10.20996/1819-6446-2024-3092. EDN: XZILSS
JATS XML
















































