Перейти к:
Феномен no-reflow: современные возможности лечения и профилактики
https://doi.org/10.20996/1819-6446-2025-3134
Аннотация
Феномен no-reflow остаётся серьёзным препятствием в лечении инфаркта миокарда, несмотря на прогресс в реперфузионной терапии, включая широкое применение первичного чрескожного коронарного вмешательства. Это явление, характеризующееся недостаточной микроциркуляцией после восстановления коронарного кровотока, значительно ухудшает клинические исходы, повышая риск сердечной недостаточности и смерти. С развитием методов диагностики, таких как магнитно-резонансная томография и динамическая сцинтиграфия миокарда, стала возможной более точная оценка микроциркуляторных изменений, позволяющая лучше понять механизмы no-reflow и целенаправленно подойти к его профилактике. Профилактические стратегии включают использование пролонгированного баллонирования стента, антитромботических препаратов (ингибиторов IIb/IIIa и внутрикоронарного тромболизиса), а также никорандила, который благодаря своим вазодилатирующим и цитопротективным свойствам демонстрирует обнадеживающие результаты в улучшении ангиографических и суррогатных маркеров реперфузии. Лечение уже развившегося no-reflow остаётся сложной задачей, так как текущие методы улучшают лишь суррогатные маркеры (TIMI и сегмент ST) без влияния на долгосрочные клинические исходы. Приоритетными средствами для лечения рефрактерного no-reflow являются никорандил и эпинефрин, особенно второй, который благодаря мощному коронаролитическому действию показал хорошие результаты в виде улучшения коронарного кровотока и снижения объёма микроваскулярной обструкции. Перспективные направления исследований включают использование моноклональных антител, способных избирательно блокировать ключевые воспалительные пути, а также гипероксемическую реперфузию. Однако требуется проведение дополнительных клинических исследований для подтверждения эффективности и безопасности данных подходов. Таким образом, поиск оптимальных терапевтических решений для управления no-reflow является важной задачей, требующей дальнейшего изучения для улучшения исходов у пациентов с инфарктом миокарда.
Ключевые слова
Для цитирования:
Диль С.В., Вышлов Е.В., Керчева М.А., Маслов Л.Н., Рябов В.В. Феномен no-reflow: современные возможности лечения и профилактики. Рациональная Фармакотерапия в Кардиологии. 2025;21(1):65-73. https://doi.org/10.20996/1819-6446-2025-3134
For citation:
Dil S.V., Vyshlov E.V., Kercheva M.A., Maslov L.N., Ryabov V.V. The no-reflow phenomenon: current treatment and prevention strategies. Rational Pharmacotherapy in Cardiology. 2025;21(1):65-73. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3134
Введение
Несмотря на значительные достижения в области реперфузионной терапии инфаркта миокарда (ИМ), феномен no-reflow остаётся серьёзной клинической проблемой, ограничивающей улучшение исходов у пациентов. Внедрение систем маршрутизации и создание специализированных региональных сосудистых центров, работающих круглосуточно, позволили существенно снизить смертность и улучшить доступность своевременной помощи [1]. Современные методы лечения, такие как чрескожное коронарное вмешательство (ЧКВ) и тромболизис, привели к значительному снижению летальности, однако даже при успешной реваскуляризации у ряда пациентов сохраняются нарушения микроциркуляции миокарда, известные как феномен no-reflow [2]. Этот феномен ассоциирован с ухудшением перфузии миокарда и увеличением риска ранних и поздних осложнений, включая увеличение зоны инфаркта, развитие сердечной недостаточности и повышение летальности [3]. Феномен no-reflow был изучен в экспериментальных моделях, однако его патогенез у людей существенно сложнее [4].
Понимание патогенеза no-reflow расширилось благодаря новым диагностическим и терапевтическим инструментам. Современные методы визуализации, такие как магнитно-резонансная томография (МРТ) сердца и динамическая сцинтиграфия миокарда, дают детальное представление о функциях микроциркуляции и степени ишемии на тканевом уровне. Эти методы позволили более точно диагностировать no-reflow, что даёт возможность более полно оценить микроциркуляторные нарушения, влияющие на клинические исходы.
Также в последние годы появились новые препараты и терапевтические подходы, которые нацелены на устранение основных компонентов no-reflow, включая воспаление и эндотелиальное повреждение.
В свете этих достижений важно оценить эффективность новых методов в лечении феномена no-reflow и определить, насколько они способствуют улучшению клинических исходов.
Цель обзора — синтез актуальных данных и оценка влияния современных диагностических и терапевтических подходов на управление no-reflow. Это позволит выявить возможности для дальнейшего внедрения инновационных методов в лечение ИМ, что в перспективе может улучшить прогноз пациентов в этой сложной клинической ситуации.
Методология исследования
Проанализированы результаты исследований и метаанализов. Поиск проводили в библиографической базе данных PubMed по ключевым словам: no-reflow, intracoronary, percutaneous coronary intervention без ограничений по языку. Глубина поиска составила 2019–2024 гг., однако, учитывая значимость ранее опубликованных данных, в анализ также были включены ключевые рандомизированные контролируемые исследования и метаанализы 2015-2018 гг. (2 работы — 2015 г., 1 — 2016 г., 1 — 2017 г., 2 — 2018 г.), имеющие высокую научную ценность для рассматриваемой темы. В качестве фильтров были установлены типы статей (Article Type): Clinical Trial, Meta-Analysis, Randomized Controlled Trial. Исключены исследования с неподходящим названием, небольшие по количеству ретроспективные исследования, клинические случаи и обзоры литературы. Основные фармакологические и нефармакологические методы лечения и профилактики феномена no-reflow приведены в таблице.
Таблица. Фармакологические и нефармакологические методы лечения и профилактики феномена no-reflow
Метод, исследование, год | Когорта, n | Конечные точки | Результат |
Профилактика no-reflow | |||
Тромбаспирация | ИМпST, | TIMI | Нет эффекта в общей группе. |
Дистальная эмболическая защита (2020) | ИМпST + АБ >5 мм, | TIMI, cTFC, MACE через 12 мес. | ↑TIMI, ↓ cTFC, ↑ MACE в группе вмешательства |
Отсроченная реваскуляризация | ИМпST, | TIMI, дистальная эмболизация | ↑TIMI, ↓ эмболизации |
Пролонгированное баллонирование стента (2022) [17] | ИМпST, | TIMI, cTFC, MBG, разрешение ST, MACE через 1 мес., МВО | ↑TIMI и MBG, ↓ cTFC, лучшее разрешение ST, ↓ МВО |
Гипероксемическая реперфузия | Передний ИМпST, | Индекс спасённого миокарда по МРТ | ↑Индекса спасенного миокарда по МРТ |
ИК тромболизис | ИМпST, | TIMI, MBG, разрешение ST, MACE | ↑TIMI и MBG, лучшее разрешение ST, ↓ MACE в группе ИК тромболизиса |
ИК тромболизис | ИМпST, | TIMI, cTFC, MBG, разрешение ST, MACE 6 мес. | ↑TIMI и MBG, ↓ cTFC, лучшее разрешение ST, снижение MACE в группе ИК тромболизиса и ингибиторов IIb/IIIa |
Тирофибан + нитроглицерин + | ИМпST+СД, | cTFC, MBG, ФВ 6 мес., MACE 6 мес. | ↑ MBG, ↓ cTFC, ↑ ФВ ЛЖ в группе комбинированного лечения |
Аденозин (2022) [26] | ИМпST, | TIMI, cTFC, MBG | ↑TIMI и MBG, ↓ cTFC |
Колхицин | ИМпST, | TIMI, разрешение ST, маркеры воспаления, MACE через 1 мес. и год | Нет эффекта |
Простагландин E1 (2024) [34] | ИМпST, | TIMI, MACE 30 и 180 дней | ↑TIMI, ↓ MACE на 30 и 180 день в группе простогландина |
Никорандил CHANGE (2022) [30] | ИМпST, | TIMI, cTFC, разрешение ST, ФВ ЛЖ, размер инфаркта по МРТ | ↑TIMI, ↓ cTFC, лучшее разрешение ST, ↓ размер инфаркта и ↑ФВ ЛЖ |
Лечение no-reflow | |||
Аденозин | no-reflow, | Размер ИМ, объём МВО по МРТ, разрешение ST, MACE через 6 мес. | Нет эффекта, ↓ ФВ и ↑ частоты ОСН в группе аденозина |
Никорандил (2021) [31] | no-reflow, | TIMI, cTFC | ↑ TIMI, ↓ cTFC, |
Верапамил | no-reflow, | Кровоток по шкале TIMI, cTFC, ИНЛС, ФВ ЛЖ, | ↑ TIMI, ↓ cTFC, ↓ ИНЛС, ↓ события MACE через 6 мес. |
Абциксимаб (2020) [23] | no-reflow, | TIMI, разрешение ST, MACE через 1 мес. | Нет эффекта |
Эпинефрин (2024) [40] | Рефрактерный no-reflow, | TIMI, разрешение ST, объём МВО по МРТ, ФВ ЛЖ, MACE через 1 мес. | ↑ TIMI, лучшее разрешение ST, ↓ МВО, ↑ ФВ ЛЖ в группе эпинефрина |
АБ — атеросклеротическая бляшка, ИК — интракоронарное, ИМпST — инфаркт миокарда с подъёмом сегмента ST, | |||
Результаты
Диагностика
Долгое время изучение феномена no-reflow было затруднено из-за отсутствия точного метода диагностики. Феномен диагностируется во время коронарной ангиографии (КАГ) сразу после коронарной реканализации в виде замедления коронарного кровотока по шкале, разработанной для стратификации риска развития смерти и ИМ (Thrombolysis In Myocardial Infarction (TIMI) [5]. Однако более точной метрикой стала корректированная шкала TIMI (cTFC), которая учитывает количество кадров для достижения контраста дистальных отделов в эпикардиальных артериях [6]. Другим подходом является оценка перфузии миокарда с помощью степени миокардиального контрастирования по шкале Myocardial Blush Grade (MBG), при этом значения MBG 0-1 указывают на наличие no-reflow даже при нормальном эпикардиальном кровотоке [7].
Но диагностируемый на КАГ no-reflow является только "вершиной айсберга" как наиболее выраженное проявление микроваскулярной обструкции (МВО), которая в свою очередь диагностируется с помощью контрастной магнитно-резонансной томографии и выявляется намного чаще, чем no-reflow по данным КАГ. Таким образом, МВО можно рассматривать как no-reflow по данным МРТ. МРТ предоставляет информацию не только о размере инфаркта, но и о функциях левого желудочка (ЛЖ), отёке и геморрагическом пропитывании миокарда, что делает её "золотым стандартом" в диагностике МВО [8].
В последние годы был проведён ряд исследований с использованием МРТ-визуализациии. Показано, что МВО ассоциирована с большим ИМ и увеличением частоты серьёзных неблагоприятных сердечных событий (major adverse cardiovascular events (MACE)) [3][9]. При этом объём МВО прямо коррелировал с увеличением смертности, госпитализаций по поводу острой сердечной недостаточности и неблагоприятным ремоделированием ЛЖ, независимо от размера инфаркта [10]. На этой основе было предложено использовать этот феномен не только для прогнозирования исходов заболевания [11], но и в качестве новой мишени в лечении ИМ с подъёмом сегмента ST (ИМпST) [9].
Распространенность феномена no-reflow у пациентов с ИМпST варьирует от 5 до 50% в зависимости от метода верификации [12]. Важно отметить, что даже при достижении TIMI 3, которое обычно свидетельствует о полноценной реперфузии, по данным контрастной МРТ, у части пациентов выявляется МВО [9]. Это указывает на вероятность недооценки истинной распространенности no-reflow при использовании стандартных методов оценки. Современные методы визуализации, такие как МРТ, позволяют точнее выявлять скрытые микроциркуляторные нарушения, подчеркивая, что феномен no-reflow может быть более распространённым, чем предполагалось ранее.
Патогенез феномена no-reflow и методы воздействия
Дистальная эмболизация
Манипулирование в окклюзированной коронарной артерии с использованием проводников, баллонов и стентов, неизбежно приводит к дистальной эмболизации фрагментов тромба, атеросклеротической бляшки, кристаллов холестерина, гиалина [13]. Это важное патогенетическое звено феномена no-reflow. Предотвращение дистальной эмболизации может способствовать потенциальному снижению степени МВО и, следовательно, вероятности развития no-reflow.
Несмотря на обнадеживающие результаты ранних исследований по применению тромбаспирации, последующие работы, post hoc-анализы и метаанализы показали, что эта процедура улучшает лишь ранние ангиографические показатели, такие как более быстрое снижение сегмента ST и более высокая частота достижения потока TIMI 3, но не сопровождается улучшением долгосрочных клинических результатов и может быть связана с повышенной частотой ишемических инсультов [14][15]. В связи с этим рутинная тромбоаспирация в настоящее время не рекомендуется как стандартная практика при ИМпST.
Другим механическим методом предотвращения эмболизации является использование устройств дистальной эмболической защиты перед стентированием. Однако применение этой технологии у пациентов с атеросклеротическими бляшками, выявленными с помощью внутрисосудистого ультразвука перед ЧКВ, может привести к повышению частоты нежелательных событий MACE в течение 12 мес., несмотря на снижение частоты no-reflow [16].
Пилотное рандомизированное исследование, оценивающее эффективность пролонгированного (>30 с) баллонирования стента, продемонстрировало положительные результаты в профилактике феномена no-reflow у пациентов с ИМпST. В группе вмешательства ангиографический кровоток значительно улучшился, а частота МВО снизилась до 6,7% по сравнению с 50% в контрольной группе (р=0,023) [17]. Механизм такого профилактического действия заключается в оптимизации раскрытия стента и снижении риска дистальной эмболии тромботического материала, что является ключевым фактором в развитии no-reflow. Пролонгированное баллонирование также минимизирует повреждение эндотелия, улучшая микроциркуляцию и снижая частоту микрососудистой обструкции.
Внутрикоронарное введение тромболитиков, согласно последним исследованиям и их метаанализам, продемонстрировало улучшение ангиографических показателей, скорости разрешения элевации ST и снижение частоты MACE [18-21]. Применение ингибиторов IIb/IIIa рецепторов тромбоцитов также значительно улучшает реперфузию миокарда и снижает частоту MACE в течение 6 мес. после ЧКВ, при этом не увеличивая риск кровотечений [20]. Комбинированное внутрикоронарное введение эптифибатида с вазодилататорами показало преимущество в снижении частоты no-reflow у пациентов с высокой тромботической нагрузкой, превосходя тромбоаспирацию [22]. В то же время применение абциксимаба не продемонстрировало значимого улучшения реперфузии1. В недавнем исследовании применение ингибиторов IIb/IIIa у пациентов с высоким риском развития no-reflow по специально разработанной шкале [23] привело к снижению частоты этого осложнения, что было сопоставимо с результатами в группе низкого риска [24].
Таким образом, ингибиторы IIb/IIIa и тромболитики способствуют предотвращению тромбообразования, что, в свою очередь, снижает риск развития no-reflow. Однако применение ингибиторов IIb/IIIa и тромболитиков требует осторожности из-за потенциально высокого риска кровотечений. Вопрос использования устройств дистальной эмболической защиты остаётся спорным: хотя они могут снизить риск эмболизации, их влияние на долгосрочные клинические исходы до сих пор неясно.
Вазоконстрикция
Вазоспазм является ключевым компонентом патогенеза феномена no-reflow и благодаря своей динамической природе представляет привлекательную терапевтическую цель. Это стимулировало проведение большого количества исследований для оценки эффективности коронаролитических агентов. Вазоспазм может быть частично обусловлен эмболизацией микроциркуляторного русла компонентами атеросклеротической бляшки.
Аденозин, воздействуя на рецепторы миокарда и артериол, вызывает расслабление гладких мышц за счет активации аденозиновых A2A-рецепторов, что приводит к расширению сосудов и улучшению микрососудистого кровотока. В нескольких исследованиях было показано, что интракоронарное введение аденозина перед стентированием улучшает показатели ангиографического кровотока, включая шкалу TIMI, TIMI frame count и степень миокардиального контрастирования по шкале MBG [25]. Исследования, направленные на оценку эффективности аденозина в лечении феномена no-reflow, демонстрировали улучшение суррогатных маркеров реперфузии, хотя без влияния на общую смертность [26]. В то же время исследование REFLO-STEMI (REperfusion Facilitated by LOcal adjunctive therapy in STEMI) показало увеличение частоты MACE в течение шести месяцев после интракоронарного введения аденозина [27].
Метаанализ 9 рандомизированных клинических исследований, проведённый позже, не подтвердил значимого снижения частоты неблагоприятных исходов или улучшения ангиографического кровотока по шкале TIMI. Более того, был отмечен рост частоты побочных эффектов, особенно у пациентов с ИМпST, прошедших первичную коронарную ангиопластику [28]. Таким образом, аденозин демонстрирует перспективные результаты в улучшении микроциркуляции, однако для окончательной оценки его клинической эффективности и безопасности требуются дополнительные исследования, особенно в контексте долгосрочных исходов.
Нитропруссид натрия, являясь донором оксида азота, вызывает активную вазодилатацию. В ряде исследований его применение в сочетании со стандартной терапией при ИМпST снижало частоту ангиографического феномена no-reflow после первичной коронарной ангиопластики. Однако улучшений в ключевых конечных точках, таких как частота MACE, размер инфаркта и МВО, не выявлено [27].
Никорандил, активируя калиевые каналы благодаря своему двойному механизму действия — вазодилатации и цитопротекции — выделяется среди других препаратов и демонстрирует обнадеживающие результаты в профилактике no-reflow. Никорандил показал положительный эффект в исследовании CHANGE (Effects of Nicorandil Administration on Infarct Size in Patients With ST-Segment–Elevation Myocardial Infarction Undergoing Primary Percutaneous Coronary Intervention), где его применение перед первичной коронарной ангиопластикой улучшило перфузию миокарда, фракцию выброса (ФВ) ЛЖ и уменьшило размер инфаркта по данным МРТ [29]. В недавних исследованиях указано, что дистальная инфузия никорандила через перфорированный баллон улучшает эпикардиальный кровоток по шкале TIMI и TIMI frame count у пациентов с феноменом no-reflow [30].
Наиболее изученными блокаторами кальциевых каналов для профилактики и лечения феномена no-reflow являются верапамил и дилтиазем. Эти агенты оказывают коронаролитическое действие и положительно влияют на реперфузионное повреждение за счёт модуляции ионного обмена, что способствует улучшению коронарной микроциркуляции. Метаанализ 8 рандомизированных исследований с участием 494 пациентов показал, что блокаторы кальциевых каналов снижают проявления феномена no-reflow и частоту MACE в течение 6 мес. [31]. Также в недавнем исследовании отмечено, что комплексный подход, включающий использование ингибиторов IIb/IIIa, тромбаспирации и вазодилататоров, при ЧКВ у пациентов с ИМпST ассоциирован с четырехкратным снижением риска смерти в течение 805 дней наблюдения [32].
Rho-киназы играют ключевую роль в регуляции тонуса сосудистой стенки и сосудистого сопротивления. Их подавление приводит к расслаблению гладких мышц артерий и улучшению микрососудистого кровотока. Таким образом, фасудил, блокируя активность Rho-киназы, уменьшает спазм сосудов и улучшает перфузию, что потенциально эффективно при феномене no-reflow. В ретроспективном исследовании показано, что интракоронарное введение селективного ингибитора Rho-киназы, фасудила, улучшает ангиографический кровоток по шкале TIMI и корригированной шкалы TIMI Frame Count у пациентов с феноменом no-reflow [33].
Простагландин E1, являясь вазодилататором и антиагрегантом, улучшает микроциркуляцию и снижает воспалительные реакции, что объясняет его потенциал как средство профилактики no-reflow. Метаанализ, включающий 5 исследований с участием 1,200 пациентов, показал, что применение простагландина E1 при ИМпST значительно снижает частоту феномена no-reflow и улучшает исходы после ЧКВ, включая снижение MACE в течение 30 и 180 дней [34].
Эпинефрин (адреналин), обладая положительными инотропными и хронотропными эффектами, в низких дозах активирует бета-2 адренорецепторы артериол, что приводит к расслаблению сосудов и коронаролитическому эффекту. В сравнительных исследованиях эпинефрин превзошел аденозин по улучшению ангиографического кровотока по шкале TIMI и cTFC, а также по долгосрочным исходам [35][36]. В недавних рандомизированных исследованиях с участием пациентов с рефрактерным no-reflow эпинефрин улучшил коронарный кровоток и привёл к снижению частоты MACE и повышению ФВ ЛЖ [37][38]. В последнем исследовании, основанном на модифицированном протоколе, опубликованном в 2022 г. [39], продемонстрирована эффективность интракоронарного эпинефрина при рефрактерном no-reflow, что выразилось в улучшении показателей микроциркуляции, увеличении ФВ ЛЖ и тенденции к снижению частоты MACE [40].
Таким образом, эпинефрин благодаря своему мощному коронаролитическому эффекту показал высокую эффективность в ситуациях, когда другие методы, такие как аденозин или ингибиторы IIb/IIIa рецепторов, не дали должного эффекта. Однако, как и в случае с никорандилом, требуется больше рандомизированных исследований для окончательного подтверждения его клинической эффективности и безопасности.
Ишемическое и реперфузионное повреждение
Ишемическое повреждение не только приводит к некрозу кардиомиоцитов, но также вызывает повреждение эндотелия микрососудов. Это сопровождается образованием эндотелиальных выступов, некрозом эндотелиальных клеток с разрывом межклеточных соединений и увеличением осмолярности интерстиция, что является одним из механизмов развития no-reflow. Реперфузионное повреждение приводит к интенсивной нейтрофильной и тромбоцитарной инфильтрации. Поврежденные нейтрофилы, тромбоциты и эндотелиальные клетки высвобождают воспалительные цитокины, вазоконстрикторы и активные формы кислорода. Ишемическое и реперфузионное повреждение миокарда сопровождаются развитием отека, который приводит к экстравазальной компрессии микрососудистого русла. В свете этого были предприняты попытки разработать вспомогательные методы реперфузии с целью снижения выраженности реперфузионного повреждения [4][41].
Для лечения ишемических и реперфузионных повреждений после остановки кровообращения и повреждения головного мозга с успехом используется гипотермия. Есть основание считать, что такое воздействие может быть эффективным с целью профилактики no-reflow во время коронарной реперфузии. Терапевтическая гипотермия успешно прошла испытания на животных, однако результаты на людях оказались менее обнадеживающими. При охлаждении всего тела пациентов с помощью теплообменных одеял и внутривенных инфузий охлаждённого физиологического раствора уменьшения размеров ИМ не получено [42]. Однако в настоящее время продолжаются рандомизированные исследования, в том числе исследование COOL-AMI EU, в которых изучается локальная гипотермия путем интракоронарного введения охлажденного физиологического раствора [43].
Гипероксемическая реперфузия — это альтернативный метод, который недавно получил предварительное одобрение FDA (Food and Drug Administration). Результаты проспективного исследования IC-HOT (Evaluation of intracoronary hyperoxemic oxygen therapy in acute anterior myocardial infarction), проведённого на 100 пациентах с передним ИМпST, показали эффективность и безопасность внутрикоронарного введения гипероксемической крови в течение 60 мин после ангиопластики в отношении увеличения индекса спасенного миокарда по данным МРТ [44].
Результаты метаанализа, объединившего 2175 пациентов, показали, что стратегия отсроченного стентирования не оказывает влияния на частоту no-reflow и клиническое течение заболевания, однако наблюдается улучшение функции ЛЖ в долгосрочной перспективе [45]. В другом метаанализе выявлено, что отсроченное стентирование способствует улучшению ангиографического кровотока, однако не оказывает влияния на объём МВО и клинические результаты [46]. Последующее небольшое одноцентровое исследование показало эффективность отсроченной реваскуляризации у больных с массивным тромбозом КА при наличии кровотока TIMI 2-3 в профилактике развития no-reflow [47]. Согласно результатам исследования DANAMI 3-DEFER (deferred versus conventional stent implantation in patients with ST-segment elevation myocardial infarction), при обнаружении кровотока TIMI 2-3 или достижении его "минимальным" вмешательством проводником и/или тромбаспирацией во время первичной ангиопластики, рутинная задержка реваскуляризации на 48 ч способствует снижению частоты развития no-reflow [48].
Воспаление
Воспаление играет ключевую роль в развитии феномена no-reflow. Повреждение эндотелия и снижение выработки оксида азота (NO) способствуют адгезии лейкоцитов к сосудистой стенке, что усугубляет микроциркуляторные нарушения. Лейкоциты создают механическое препятствие для кровотока, усиливая эндотелиальную дисфункцию и провоцируя локальное воспаление. Этот процесс связан с оксидативным стрессом, когда избыток реактивных кислородных форм снижает доступность NO, что усиливает воспалительный ответ и способствует дальнейшему повреждению сосудов и ткани [49].
Применение противовоспалительного препарата колхицина в исследовании PodCAST-PCI не улучшило показатели реперфузии ИМ [50]. Вероятно, требуются более эффективные противовоспалительные препараты с сильным воздействием на ключевые патогенетические механизмы воспаления. Перспективным направлением может быть использование моноклональных антител, которые способны селективно блокировать ключевые воспалительные пути и мишени. Такие препараты могут предложить более выраженное подавление воспалительного каскада по сравнению с традиционными средствами.
Ключевые механизмы и терапевтические стратегии при феномене no-reflow представлены на рисунке.
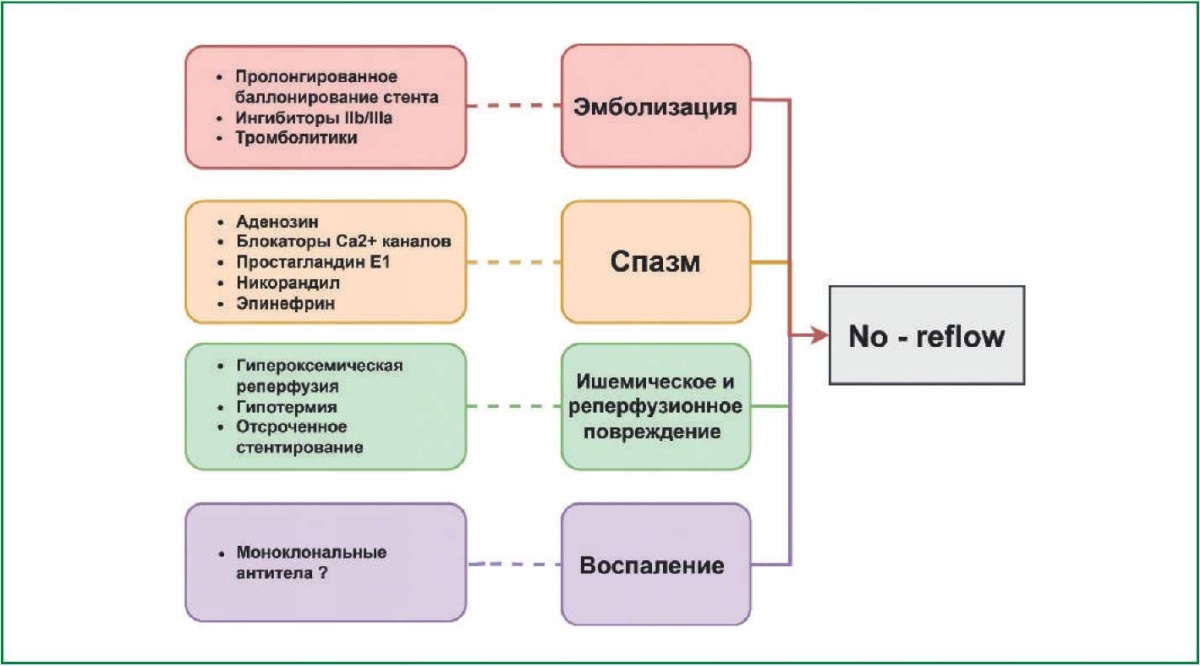
Рисунок. Механизмы и подходы к лечению феномена no-reflow
Заключение
Феномен no-reflow остаётся значительной клинической проблемой, несмотря на существенный прогресс в его изучении. Основные ограничения современных данных связаны с небольшими размерами выборок, отсутствием единых диагностических критериев и использованием суррогатных маркеров реперфузии, которые зачастую недостаточно чувствительны для точного выявления МВО. Недостаточное применение МРТ ограничивает возможности точной диагностики и оценки микроциркуляции. Кроме того, исследований, посвящённых долгосрочной оценке клинических исходов у пациентов с no-reflow, крайне мало.
Ряд методов, таких как пролонгированное баллонирование стента, никорандил и антитромботические препараты, показали перспективность в профилактике no-reflow, однако для подтверждения их эффективности требуются крупные рандомизированные исследования. В настоящее время эффективные и универсальные подходы к лечению no-reflow остаются неразработанными, вероятно, из-за сложной многофакторной патофизиологии, требующей индивидуализированного подхода в терапии. Особый интерес вызывают никорандил и эпинефрин, последний из которых способен быстро улучшить коронарный кровоток и уже продемонстрировал свою эффективность в нескольких исследованиях.
Перспективными направлениями в борьбе с no-reflow являются применение моноклональных антител, селективно блокирующих ключевые воспалительные пути и мишени, а также гипероксемическая реперфузия. Оба подхода открывают новые горизонты для адресного воздействия на ключевые патогенетические процессы, лежащие в основе микроциркуляторных нарушений.
Отношения и деятельность. Нет.
Relationships and Activities. None.
Финансирование: НИИ Кардиологии Томского НИМЦ.
Funding: Tomsk National Research Medical Center, Russian Academy of Sciences.
1. Бессонов И. С., Дьячков С. М. Калькулятор расчета риска возникновения феномена "no-reflow". Свидетельство о регистрации программы для ЭВМ 2020661255 (21.09.2020)
Список литературы
1. Бессонов И. С., Сапожников С. С., Шадрин А. А. и др. Влияние времени "дверь–баллон" на результаты лечения пациентов с острым инфарктом миокарда с элевацией сегмента ST в зависимости от длительности догоспитальной задержки. Кардиология. 2023;63(6):28-36. DOI: 10.18087/cardio.2023.6.n2245.
2. Ma M, Diao K, Yang Z, et al. Clinical associations of microvascular obstruction and intramyocardial hemorrhage on cardiovascular magnetic resonance in patients with acute ST segment elevation myocardial infarction (STEMI): An observational cohort study. Medicine (Baltimore). 2018;97(30):e11617. DOI: 10.1097/MD.0000000000011617.
3. De Waha S, Patel MR, Granger CB, et al. Relationship between microvascular obstruction and adverse events following primary percutaneous coronary intervention for ST-segment elevation myocardial infarction: an individual patient data pooled analysis from seven randomized trials. Eur Heart J. 2017;38(47):3502-10. DOI: 10.1093/eurheartj/ehx414.
4. Рябов В. В., Попов С. В., Вышлов Е. В. и др. Реперфузионное повреждение сердца. Роль микроваскулярной обструкции. Сибирский журнал клинической и экспериментальной медицины. 2023;38(2):14-22. DOI: 10.29001/2073-8552-2023-39-2-14-22.
5. TIMI Study Group. The Thrombolysis in Myocardial Infarction (TIMI) trial. Phase I findings. N Engl J Med. 1985;312(14):932-6. DOI: 10.1056/NEJM198504043121437.
6. Gibson CM, Cannon CP, Daley WL, et al. TIMI frame count: а quantitative method of assessing coronary artery flow. Circulation. 1996;93(5):879-88. DOI: 10.1161/01.cir.93.5.879.
7. Van ’t Hof AW, Liem A, Suryapranata H, et al. Angiographic assessment of myocardial reperfusion in patients treated with primary angioplasty for acute myocardial infarction: Myocardial blush grade. Zwolle Myocardial Infarction Study Group. Circulation. 1998;97(23):2302-6. DOI: 10.1161/01.cir.97.23.2302.
8. Beijnink CWH, van der Hoeven NW, Konijnenberg LSF, et al. Cardiac MRI to Visualize Myocardial Damage after ST-Segment Elevation Myocardial Infarction : A Review of Its Histologic Validation. Radiology. 2021;301(1):4-18. DOI:10.1148/radiol.2021204265.
9. Kranenburg MV, Magro M, Thiele H, et al. Prognostic value of microvascular obstruction and infarct size, as measured by CMR in STEMI patients. JACC Cardiovasc Imaging. 2014;7(9):930-9. DOI: 10.1016/j.jcmg.2014.05.010.
10. Kloner RA. The importance of no-reflow/microvascular obstruction in the STEMI patient. Eur Heart J. 2017;38(47):3511-3. DOI: 10.1093/eurheartj/ehx288.
11. Reinstadler SJ, Stiermaier Т, Reindl М, et al. Intramyocardial haemorrhage and prognosis after ST-elevation myocardial infarction. Eur Heart J Cardiovasc Imaging. 2019;20(2):138-46. DOI: 10.1093/ehjci/jey101.
12. Bouleti C, Mewton N, Germain S. The no-reflow phenomenon: State of the art. Arch Cardiovasc Dis. 2015;108(12):661-74. DOI: 10.1016/j.acvd.2015.09.006.
13. Limbruno U, De Carlo M, Pistolesi S. et al. Distal embolization during primary angioplasty: histopathologic features and predictability. Am Heart J. 2005; 150(1):102-8. DOI: 10.1016/j.ahj.2005.01.016.
14. Рябов В. В., Самойлова Ю. О., Гомбожапова А. Э. и др. Применение метода тромбоаспирации у пациентов с инфарктом миокарда с подъемом сегмента ST: обзор литературы. Кардиоваскулярная терапия и профилактика. 2023;22(7):3577. DOI: 10.15829/1728-8800-2023-3577.
15. d’Entremont MA, Alazzoni A, Dzavik V, et al. No-reflow after primary percutaneous coronary intervention in patients with ST-elevation myocardial infarction: an angiographic core laboratory analysis of the TOTAL Trial. EuroIntervention. 2023;19(5):e394-401. DOI: 10.4244/EIJ-D-23-00112.
16. Hibi K, Kozuma K, Maejima N, et al.; VAMPIRE 3 Investigators. Long-Term Clinical Outcomes After Filter Protection During Percutaneous Coronary Intervention in Patients With Attenuated Plaque — 1-Year Follow up of the VAMPIRE 3 (Vacuum Aspiration Thrombus Reemoval 3) Trial. Circ J. 2020;85(1):44-9. DOI:10.1253/circj.CJ-20-0449.
17. Ma M, Wang L, Diao KY, et al. A randomized controlled clinical trial of prolonged balloon inflation during stent deployment strategy in primary percutaneous coronary intervention for ST-segment elevation myocardial infarction: a pilot study. BMC Cardiovasc Disord. 2022;22(1):30. DOI: 10.1186/s12872-022-02477-0.
18. Kaddoura R, Mohamed Ibrahim MI, Al-Badriyeh D, et al. Intracoronary pharmacological therapy versus aspiration thrombectomy in STEMI (IPAT-STEMI) : A systematic review and meta-analysis of randomized trials. PLoS One. 2022;17(5):e0263270. DOI: 10.1371/journal.pone.0263270.
19. Alexiou S, Patoulias D, Theodoropoulos KC, et al. Intracoronary Thrombolysis in ST-Segment Elevation Myocardial Infarction Patients Undergoing Primary Percutaneous Coronary Intervention: an Updated Meta-analysis of Randomized Controlled Trials. Cardiovasc Drugs Ther. 2024;38(2):335-46. DOI: 10.1007/s10557-022-07402-3.
20. Geum MJ, Yu YM, Jeon J, et al. Intracoronary antithrombotic therapy during primary percutaneous coronary intervention in patients with STEMI : A systematic review and network meta-analysis. Thromb Res. 2024;233:127-34. DOI: 10.1016/j.thromres.2023.11.022.
21. Yu S, Jia H, Ding S, et al. Efficacy and safety of intracoronary pro-urokinase combined with low-pressure balloon pre-dilatation during percutaneous coronary intervention in patients with anterior ST-segment elevation myocardial infarction. J Cardiothorac Surg. 2024;19(1):180. DOI: 10.1186/s13019-024-02699-7.
22. Hamza M, Elgendy IY. Intracoronary eptifibatide with vasodilators to prevent no-reflow in diabetic STEMI with high thrombus burden. A randomized trial. Rev Esp Cardiol (Engl Ed). 2022;75(9):727-33. DOI: 10.1016/j.rec.2021.10.012.
23. Rgeeb AN, Alsalkh HA, Radhi AK, et al. Effect of Intravenous Abciximab on Coronary Flow Improvement After Re-vascularization in Primary Coronary Intervention and Short Term Impact. Med Arch. 2020;74(4):265-9. DOI: 10.5455/medarh.2020.74.265-269.
24. Бессонов И. С., Шадрин А. А., Сапожников С. С. и др. Превентивное использование ингибиторов гликопротеина IIb/IIIa рецепторов тромбоцитов при проведении чрескожных коронарных вмешательств у пациентов с острым инфарктом миокарда с подъемом сегмента ST и высоким риском развития феномена микроваскулярной обструкции. Сибирский журнал клинической и экспериментальной медицины. 2023;38(2):122-31. DOI: 10.29001/2073-8552-2023-38-2-122-131.
25. Sadeghian M, Mousavi SH, Aamaraee Z, Shafiee A. Administration of intracoronary adenosine before stenting for the prevention of no-reflow in patients with ST-elevation myocardial infarction. Scand Cardiovasc J. 2022;56(1):23-7. DOI: 10.1080/14017431.2022.2035807.
26. Niu X, Zhang J, Bai M, et al. Effect of intracoronary agents on the no-reflow phenomenon during primary percutaneous coronary intervention in patients with ST-elevation myocardial infarction: a network meta-analysis. BMC Cardiovasc Disord. 2018;18(1):3. DOI: 10.1186/s12872-017-0722-z.
27. Nazir SA, Khan JN, Mahmoud IZ, et al. The REFLO-STEMI (REperfusion Facilitated by LOcal adjunctive therapy in ST-Elevation Myocardial Infarction) trial: a randomised controlled trial comparing intracoronary administration of adenosine or sodium nitroprusside with control for attenuation of microvascular obstruction during primary percutaneous coronary intervention. Southampton (UK): NIHR Journals Library; 2016.
28. Su Q, Nyi TS, Li L. Adenosine and verapamil for no-reflow during primary percutaneous coronary intervention in people with acute myocardial infarction. Cochrane Database Syst Rev. 2015;2015(5):CD009503. DOI: 10.1002/14651858.CD009503.pub3.
29. Qian G, Zhang Y, Dong W, et al. Effects of Nicorandil Administration on Infarct Size in Patients With ST-Segment- Elevation Myocardial Infarction Undergoing Primary Percutaneous Coronary Intervention: The CHANGE Trial. J Am Heart Assoc. 2022;11(18):e026232. DOI: 10.1161/JAHA.122.026232.
30. Sinha SK, Kumar P, Sharma AK et al. Perforated balloon technique mediated intracoronary delivery of nicorandil to treat coronary no-reflow phenomenon: a novel pharmacological solution to precarious situation. Am J Cardiovasc Dis. 2021;11(5):544-54.
31. Wang L, Cheng Z, Gu Y, Peng D. Short- Term Effects of Verapamil and Diltiazem in the Treatment of No Reflow Phenomenon: A Meta- Analysis of Randomized Controlled Trials. Biomed Res Int. 2015;2015:382086. DOI: 10.1155/2015/382086.
32. Фролов А. А., Починка И. Г., Фролов И. А. и др. Синдром коронарной микрососудистой обструкции при чрескожных коронарных вмешательствах у пациентов с инфарктом миокарда: комплексный подход к профилактике и лечению. Патология кровообращения и кардиохирургия. 2024;28(3):64-77. DOI: 10.21688/1681-3472-2024-3-64-77.
33. Kikuchi Y, Takahashi J, Hao K, et al. Usefulness of intracoronary administration of fasudil, a selective Rho-kinase inhibitor, for PCI-related refractory myocardial ischemia. Int J Cardiol. 2019;297:8-13. DOI: 10.1016/j.ijcard.2019.09.057.
34. Chen Y, Wang M, Yang Y, et al. Efficacy and Safety of Alprostadil in Microcirculatory Disturbances During Emergency PCI: A Meta-Analysis of Randomized Controlled Trials. Am J Cardiovasc Drugs. 2024;24(4):547-56. DOI: 10.1007/s40256-024-00655-3.
35. Khan KA, Qamar N, Saghir T, et al. Comparison of Intracoronary Epinephrine and Adenosine for No- Reflow in Normotensive Patients With Acute Coronary Syndrome (COAR Trial). Circ Cardiovasc Interv. 2022;15(2):e011408. DOI: 10.1161/CIRCINTERVENTIONS.121.011408.
36. Darwish A, Frere AF, Abdelsamie M, et al. Intracoronary epinephrine versus adenosine in the management of refractory no-reflow phenomenon: a single-center retrospective cohort study. Ann Saudi Med. 2022;42(2):75-82. DOI: 10.5144/0256-4947.2022.75.
37. Вышлов Е. В., Диль С. В., Баев А. Е. и др. Интракоронарное введение эпинефрина при рефрактерном феномене No-reflow у пациентов с острым инфарктом миокарда. Кардиология. 2024;64(6):34-42. DOI: 10.18087/cardio.2024.6.n2493.
38. Navarese EP, Frediani L, Kandzari DE, et al. Efficacy and safety of intracoronary epinephrine versus conventional treatments alone in STEMI patients with refractory coronary no-reflow during primary PCI: The RESTORE observational study. Catheter Cardiovasc Interv. 2021;97(4):602-11. DOI: 10.1002/ccd.29113.
39. Диль С. В., Вышлов Е. В., Рябов В. В. Интракоронарное введение эпинефрина и верапамила при рефрактерном феномене no-reflow у пациентов с острым инфарктом миокарда. Кардиоваскулярная терапия и профилактика. 2022;21(1):2936. DOI:10.15829/1728-8800-2022-2936.
40. Ryabov V, Dil S, Vyshlov E, et al. Efficiency and Safety of Intracoronary Epinephrine Administration in Patients With ST-Elevation Myocardial Infarction With Refractory Coronary No-Reflow. Am J Cardiol. 2024;226:118-27. DOI:10.1016/j.amjcard.2024.07.011.
41. Ryabov VV, Vyshlov EV, Maslov LN, et al. The Role of Microvascular Obstruction and Intra-Myocardial Hemorrhage in Reperfusion Cardiac Injury. Analysis of Clinical Data. Rev Cardiovasc Med. 2024;25(3):105. DOI: 10.31083/j.rcm2503105.
42. Ryabov VV., Vyshlov EV. Therapeutic hypothermia in acute myocardial infarction. Russian Journal of Cardiology. 2023;28(7):5412 (In Russ.) [Рябов В. В., Вышлов Е. В. Терапевтическая гипотермия при остром инфаркте миокарда. Российский кардиологический журнал. 2023;28(7):5412]. DOI: 10.15829/1560-4071-2023-5412.
43. Keeble TR, Karamasis GV, Noc M, et al. Effect of intravascular cooling on microvascular obstruction (MVO) in conscious patients with ST-elevation myocardial infarction undergoing primary PCI: results from the COOL AMI EU pilot study. Cardiovasc. Revasc. Med. 2019;20(9):799-804. DOI: 10.1016/j.carrev.2018.09.014.
44. David SW, Khan ZA, Patel NC, et al. Evaluation of intracoronary hyperoxemic oxygen therapy in acute anterior myocardial infarction: The IC-HOT study. Catheter Cardiovasc Interv. 2019;93(5):882-90. DOI: 10.1002/ccd.27905.
45. Qiao J, Pan L, Zhang B, et al. Deferred Versus Immediate Stenting in Patients With ST-Segment Elevation Myocardial Infarction : A Systematic Review and Meta-Analysis. J Am Heart Assoc. 2017;6(3):e004838. DOI: 10.1161/JAHA.116.004838.
46. Cassese S, Belle L, Ndrepepa G, et al. Deferred vs Immediate Stenting in Primary Percutaneous Coronary Intervention: A Collaborative Meta-analysis of Randomized Trials With Cardiac Magnetic Resonance Imaging Data. Can J Cardiol. 2018;34(12):1573-80. DOI: 10.1016/j.cjca.2018.07.480.
47. Вышлов Е. В., Крылов А. Л., Сыркина А. Г. и др. Двухэтапная реваскуляризация у пациентов с острым инфарктом миокарда и массивным тромбозом коронарной артерии. Кардиология. 2019;59(2):5-9. DOI: 10.18087/cardio.2019.2.10224.
48. Nepper-Christensen L, Kelbæk H, Ahtarovski KA, et al. Angiographic outcome in patients treated with deferred stenting after ST-segment elevation myocardial infarction- results from DANAMI-3-DEFER. Eur Heart J Acute Cardiovasc Care. 2022;11(10):742-8. DOI: 10.1093/ehjacc/zuac098.
49. Janaszak-Jasiecka A, Płoska А, Wierońska JM, et al. Endothelial dysfunction due to eNOS uncoupling: molecular mechanisms as potential therapeutic targets. Cell Mol Biol Lett. 2023;28(1):21. DOI: 10.1186/s11658-023-00423-2.
50. Hosseini SH, Talasaz AH, Alidoosti M, et al. Preprocedural Colchicine in Patients With Acute ST-elevation Myocardial Infarction Undergoing Percutaneous Coronary Intervention: A Randomized Controlled Trial (PodCAST-PCI). J Cardiovasc Pharmacol. 2022;80(4):592-9. DOI: 10.1097/FJC.0000000000001317.
Об авторах
С. В. ДильРоссия
Станислав Викторович Диль
Томск
Е. В. Вышлов
Россия
Евгений Викторович Вышлов
Томск
М. А. Керчева
Россия
Мария Анатольевна Керчева
Томск
Л. Н. Маслов
Россия
Леонид Николаевич Маслов
Томск
В. В. Рябов
Россия
Вячеслав Валерьевич Рябов
Томск
Дополнительные файлы
Рецензия
Для цитирования:
Диль С.В., Вышлов Е.В., Керчева М.А., Маслов Л.Н., Рябов В.В. Феномен no-reflow: современные возможности лечения и профилактики. Рациональная Фармакотерапия в Кардиологии. 2025;21(1):65-73. https://doi.org/10.20996/1819-6446-2025-3134
For citation:
Dil S.V., Vyshlov E.V., Kercheva M.A., Maslov L.N., Ryabov V.V. The no-reflow phenomenon: current treatment and prevention strategies. Rational Pharmacotherapy in Cardiology. 2025;21(1):65-73. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3134
JATS XML
















































