Перейти к:
Сравнительная эффективность фиксированных комбинаций азилсартана медоксомила/хлорталидона и лозартана/гидрохлортиазида у пациентов с артериальной гипертензией и сердечной недостаточностью с сохранной фракцией выброса
https://doi.org/10.20996/1819-6446-2022-04-01
Аннотация
Цель. Изучение влияния фиксированных комбинаций азилсартана медоксомил/хлорталидона (АЗМ/ХТД) и лозартана/гидрохлортиазида (ЛОЗ) на уровень натрийуретических пептидов (НУП), показателей теста 6-ти минутной ходьбы (ТШХ), статус гидратации и уровней периферического и центрального артериального давления (АД) у пациентов с артериальной гипертонией (АГ) и сердечной недостаточностью с сохраненной фракцией выброса (СНсФВ).
Материал и методы. В открытое проспективное клинико-фармакологическое исследование включено 56 пациентов с неконтролируемой или нелеченной АГ и СНсФВ, рандомизированных к приему комбинации в первой группе АЗМ/ ХТД (40/12,5 мг) и во второй группе ЛОЗ/ГХТ (100/12,5 мг) в течение 4 нед. Пациентам, не достигшим целевого АД<140/<90 мм рт.ст., усиливали терапию, назначая комбинации с удвоением дозы диуретика до 25 мг. Период наблюдения составил 12 нед. Всем пациентам выполнены клиническое обследование с оценкой симптомов и/или признаков сердечной недостаточности, лабораторно-инструментальные исследования, в том числе, NT-proBNP, суточное мониторирование АД, аппланационная тонометрия, ТШХ, эхокардиография. С целью оценки статуса гидратации выполнен биоимпедансный векторный анализ (БИВА). Диагностику СНсФВ проводили по алгоритму HFA-PEFF.
Результаты. Через 12 нед целевого офисного и суточного АД достигли 92% и 78% пациентов (р<0,05); 82% и 67% (р<0,05) первой и второй группы соответственно. У пациентов из обеих групп через 12 нед выявлено значимое снижение систолического и диастолического АД, центрального АД, снижение скорости распространения пульсовой волны, более выраженное в первой группе пациентов (p<0,05). На фоне терапии в обеих группах пациентов наблюдалось значимое снижение уровня NT-proBNP: в первой группе с 300 [199;669] пг/мл до 156 [157; 448] пг/мл (p=0,003), во второй группе с 298 [180; 590] пг/мл до 194 [140; 360] пг/мл (p=0,006), увеличение дистанции при ТШХ с 317 [210;398] м до 380 [247; 455)]м (p=0,006) в первой группе и улучшение статуса гидратации по данным БИВА, но более выраженное в первой группе (p<0,001).
Заключение. У пациентов с АГ и СНсФВ терапия комбинацией АЗМ/ХТД по сравнению с ЛОЗ/ГХТ сопровождалась более выраженным гипотензивным эффектом в отношении суточного и периферического АД, центрального АД, уровня NTproBNP, увеличением дистанции при прохождении ТШХ и достижением статуса эуволемии.
Ключевые слова
Для цитирования:
Кобалава Ж.Д., Сафарова А.Ф., Гудиева Х.М., Маркова М.А., Петросян А.Е. Сравнительная эффективность фиксированных комбинаций азилсартана медоксомила/хлорталидона и лозартана/гидрохлортиазида у пациентов с артериальной гипертензией и сердечной недостаточностью с сохранной фракцией выброса. Рациональная Фармакотерапия в Кардиологии. 2022;18(2):127-134. https://doi.org/10.20996/1819-6446-2022-04-01
For citation:
Kobalava Zh.D., Safarova A.F., Gudieva Kh.M., Markova M.A., Petrosyan A.E. Comparative Efficacy of Single Pill Combinations of Azilsartan Medoxomil/Chlorthalidone and Losartan/Hydrochlorothiazide in Patients with Hypertension and Heart Failure with Preserved Ejection Fraction. Rational Pharmacotherapy in Cardiology. 2022;18(2):127-134. (In Russ.) https://doi.org/10.20996/1819-6446-2022-04-01
Введение
Сердечная недостаточность (СН) характеризуется высокой коморбидностью: у половины пациентов встречается пять и более сопутствующих заболеваний [1]. Длительная неконтролируемая артериальная гипертония (АГ) с гипертрофией левого желудочка (ГЛЖ) является ключевым фактором риска развития сердечной недостаточности с сохраненной фракцией выброса (СНсФВ). В многочисленных исследованиях было установлено, что более 90% пациентов с СНсФВ имеют в анамнезе АГ [1-4]. По результатам эпидемиологического исследования ЭПОХА 84% пациентов с СНсФВ имели АГ [5]. Эффективная антигипертензивная терапия является одним из ключевых компонентов профилактики СНсФВ [6][7].
Установлены существенные различия антигипертензивных препаратов по способности предупреждать развитие СН. Исследование ALLHAT продемонстрировало, что антигипертензивная терапия на основе хлорталидона (ХТД) статистически значимо уменьшала риск развития не только СН вообще, но СНсФВ по сравнению с лизиноприлом, амлодипином и доксазозином [8-10]. Превосходство тиазидных диуретиков над другими классами антигипертензивных препаратов в предупреждении СН подтверждено в крупном метаанализе [11]. Превосходящая антигипертензивная эффективность ХТД над гидрохлоротиазидом (ГХТ) установлена в многочисленных исследованиях, в том числе, с использованием суточного мониторирования артериального давления (СМАД) [12][13]. В крупных рандомизированных двойных слепых исследованиях с использованием СМАД доказана более выраженная антигипертензивная эффективность азилсартана медоксомила (АЗМ) по сравнению с другими блокаторами рецепторов ангиотензина II (БРА) [14-18]. Эти данные подтверждены в Российской популяции пациентов с АГ [19]. В сравнительных исследованиях было показано, что АЗМ в сочетании с ХТД 12,5-25 мг/сут более эффективен в снижении артериального давления (АД), чем в сочетании с ГХТ 12,5-25 мг [20] и индапамидом 1,5 мг [21]. Важность выраженного антигипертензивного эффекта в профилактике СН подтвердило исследование SPRINT (Systolic Blood Pressure Intervention Trial), которое продемонстрировало снижение острой декомпенсация СН на 38% в группе интенсивного снижения АД [22].
Таким образом, представляется актуальным сравнительное изучение эффектов комбинации АЗМ и ХТД, потенциально обладающей более высокой эффективностью, у пациентов с АГ и СНсФВ по сравнению с широко применяемой в клинической практике комбинацией лозартана (ЛОЗ) и ГХТ для проверки гипотезы, что более выраженный антигипертензивный эффект приведет к более выраженному уменьшению симптомов СНсФВ.
Цель исследования – изучить влияние комбинаций АЗМ/ХТД и ЛОЗ/ГХТ на уровень натрийуретических пептидов (НУП), показатели теста шестиминутной ходьбы (ТШХ), статус гидратации наряду с их антигипертензивной эффективностью по данным центрального, клинического и суточного АД у пациентов с АГ и СНсФВ.
Материал и методы
В открытое рандомизированное исследование включали пациентов с неконтролируемой или нелеченной АГ и СНсФВ, подписавших информированное согласие на участие в исследовании. Диагностику СНсФВ проводили по модифицированному пошаговому алгоритму HFA-PEFF с учетом структурно-функциональных параметров миокарда и НУП, с четкими критериями для пациентов с фибрилляцией предсердий (ФП) (рис. 1). В отличие от предложенного алгоритма HFA-PEFF [23] на шаге 3 мы использовали диастолический стресс-тест с пассивным подъемом ног и неинвазивное определение давления заклинивания легочной артерии (ДЗЛА) при эхокардиографии (ЭхоКГ).

Figure 1. Modified algorithm for diagnosing heart failure with preserved ejection fraction HFA-PEFF [23]
Рисунок 1. Модифицированный алгоритм диагностики СНсФВ HFA-PEFF [23]
Критерии невключения: индекс массы тела ≥40 кг/м2; острый коронарный синдром или острое нарушение мозгового кровообращения в течение предшествующих 3 мес; онкологические заболевания; тяжелые клапанные пороки сердца; обострение хронической обструктивной болезни или бронхиальной астмы; анемия тяжелой степени; скорость клубочковой фильтрации <30 мл/мин/1,73 м2.
Методом простых конвертов пациенты с АГ и СНсФВ были рандомизированы на две группы. Пациентам первой группы (n=28) была назначена стартовая терапия комбинацией АЗМ/ХТД 40/12,5 мг 1 р/сут. Пациентам второй группы (n=28) – комбинацией препарата ЛОЗ/ГХТ 100/12,5 мг 1 р/сут. Целевой уровень офисного АД для пациентов с АГ составил <140/90 мм рт.cт., при СМАД – <130/<80 мм рт.ст. По истечении 4 нед пациентам, не достигшим целевого уровня АД, проводили усиление антигипертензивной терапии (АГТ): в первой группе – увеличение дозы АЗМ/ХТД до 40/25 мг 1 р/сут; во второй группе – увеличение дозы ЛОЗ/ГХТ до 100/25 мг 1 р/сут.
Всем пациентам проводили рутинное клиническое обследование с оценкой симптомов и/или признаков СН. Уровень NT-proBNP анализировали иммунохемилюминесцентным методом (PathFast, Япония). Функциональный статус пациентов определяли с помощью проведения ТШХ.
Эхокардиографию (ЭхоКГ) выполняли на аппарате экспертного класса VIVID E90 (GE Healthcare, США) с оценкой систолической и диастолической функций ЛЖ согласно предложенному алгоритму HFA-PEFF [24].
Измерение клинического АД проводили с помощью автоматического валидированного осциллометрического прибора OMRON 705CP-II (Япония) на каждом визите: исходно, через 1, 4, 12 нед. АД измеряли в положении сидя после 10 минутного отдыха пациента на правой руке трехкратно. Среднее значение АД принимали за его уровень на данном визите.
СМАД проводили при помощи BPLab Vasotens (ООО «Петр Телегин», Нижний Новгород) с оценкой стандартных параметров периферического АД.
Аппланационную тонометрию лучевой артерии проводили при помощи прибора Sphygmocor (AtCor, Австралия) c оценкой артериальной ригидности и параметров центральной пульсовой волны. Скорость распространения пульсовой волны (СРПВ) оценивали путем регистрации пульсовой волны на сонной и бедренной артериях с одновременной регистрацией ЭКГ. Повышением СРПВ считали показатель выше 10 м/с.
Биоимпедансный векторный анализ (БИВА) проводили на анализаторе АВС-01 (ОООНТЦ «МЕДАСС», Россия) для оценки статуса гидратации и компонентного состава тела. Принцип данного метода основан на разнице электропроводимости, которая зависит от комбинации активного сопротивления (вне- и внутриклеточных растворов электролитов) и реактивного сопротивления (сопротивления мембран).
Статус гидратации определяли по графическому изображению результатов БИВА, представленных в виде эллипсов, ограничивающих 50-й, 75-й, 95-й центили распределения. В ранних исследованиях была продемонстрирована эффективность БИВА для оценки застоя у пациентов с декомпенсацией ХСН [25-27], для мониторинга динамики на фоне терапии [25][28], а также прогностическая значимость в отношении неблагоприятного прогноза у пациентов с СНсФВ без клинических признаков декомпенсации [29]. Благодаря своей безопасности и быстроте проведения БИВА потенциально может стать хорошей альтернативой клиническим и лабораторным методам диагностики признаков субклинического застоя у пациентов с СНсФВ.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинской Декларации. Протокол исследования был одобрен этическим комитетом Медицинского института РУДН.
Статистический анализ результатов исследования проводили с использованием пакета прикладных статистических программ Statistica (версия 8.0; Statsoft) и SPSS (версия 22.0) с применением стандартных алгоритмов вариационной статистики. Качественные переменные представляли абсолютными (n) и относительными (%) значениями. Количественные переменные описывали как среднее арифметическое значение (М) и стандартное отклонение среднего значения (SD) (при нормальном распределении), или как медиана (Me) и интерквартильный размах (IQR – при асимметричном распределении). Для сравнения частот признаков и качественных переменных пользовались критерием хи-квадрат Пирсона (χ2). Статистическую значимость различий между двумя группами по количественным переменным оценивали при помощи U-критерия Манна-Уитни. Различия средних величин и корреляций считались значимыми при уровне значимости р<0,05.
Результаты
Клинико-демографическая характеристика обследованных пациентов представлена в табл. 1.
По результатам проведения ЭхоКГ были выявлены структурно-функциональные изменения сердца у 95% пациентов в обеих группах (табл. 2). По истечении 4 нед пациентам, не достигшим целевого уровня АД, проводили усиление АГТ: в группе АЗМ/ХТД – 11 (39,3%) пациентам, в группе ЛОЗ/ГХТ – 14 (50%).
Через 1, 4, 12 нед наблюдения отмечено значимое снижение уровня офисного систолического артериального давления (САД) в обеих группах, более выраженное в группе АЗМ/ХТД (рис. 2). Через 12 нед 92% пациентов первой группы и 78% пациентов второй группы достигли целевого офисного АД.
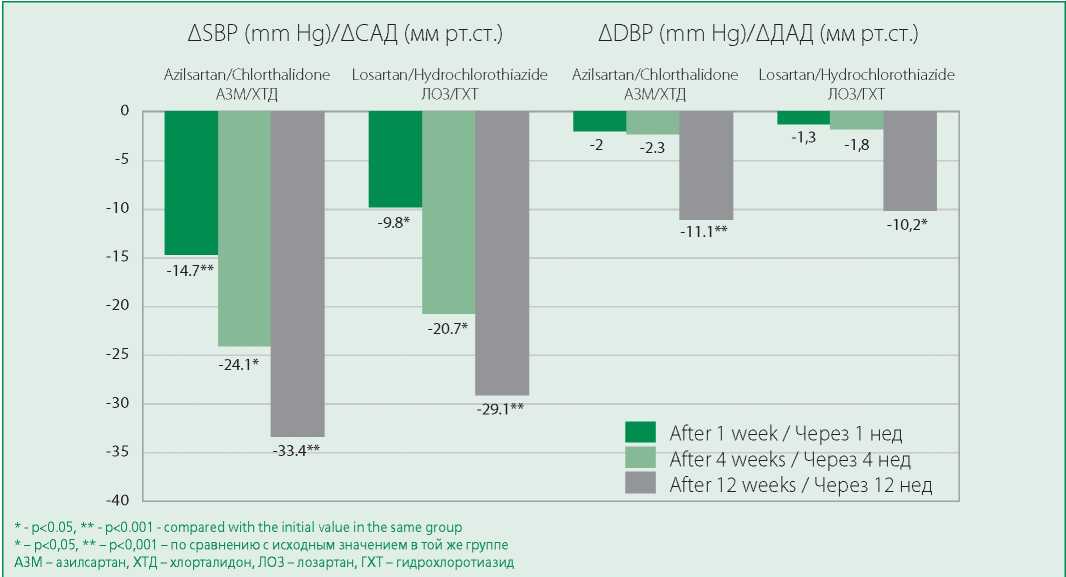
Figure 2. Change in office systolic and diastolic blood pressure
Рисунок 2. Динамика офисного АД в изучаемых группах
На фоне терапии отмечалось тенденция к улучшению параметров СМАД с большим эффектом в группе ́ АЗМ/ХТД (табл. 3). Через 12 нед 23 (82,1%) пациента группы АЗМ/ХТД достигли целевых значений среднесуточного АД по сравнению с 17 (67,9%) пациентами, получавших ЛОЗ/ГХТ (χ2=3,15; p=0,08).
У пациентов обеих групп через 12 нед выявлено значимое снижение систолического, диастолического и пульсового центрального АД, СРПВ (табл. 4), а также улучшение статуса гидратации (рис. 3).

Figure 3. Change in hydration status in study groups
Рисунок 3. Динамика статуса гидратации в изучаемых группах
В обеих группах через 12 нед отмечено значимое снижение уровня НУП и увеличение толерантности к физической нагрузке в первой группе пациентов (табл. 5).
Table 1. Baseline characteristics
Таблица 1. Клинико-демографическая характеристика обследованных пациентов
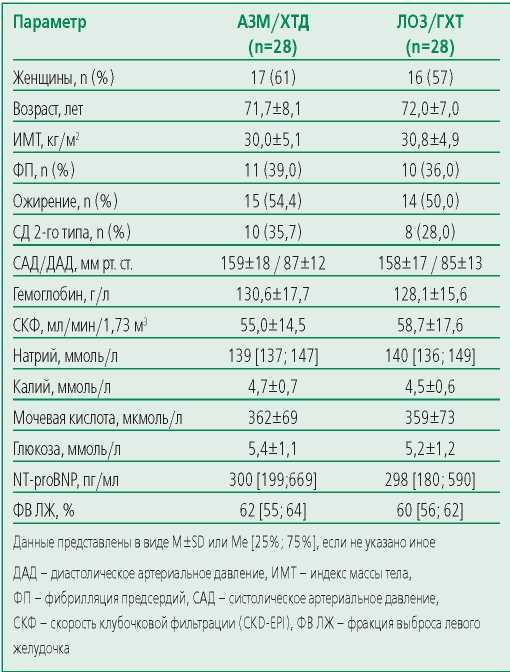
Table 2. Echocardiographic parameters
Таблица 2. Эхокардиографические параметры в изучаемых группах
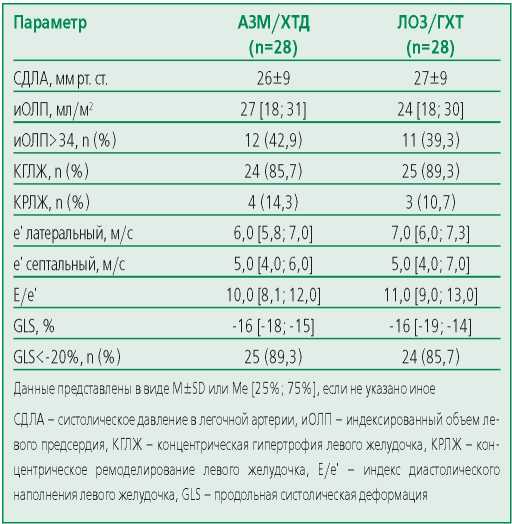
Table 3. Changes in parameters of daily monitoring of blood pressure
Таблица 3. Динамика показателей СМАД в изучаемых группах
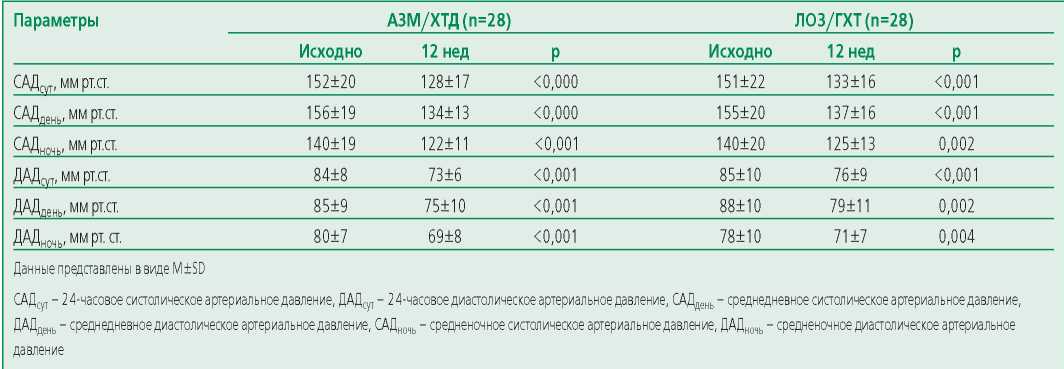
Table 4. Changes in parameters of central blood pressure and arterial stiffness
Таблица 4. Динамика параметров центрального АД и артериальной ригидности в изучаемых группах

Table 5. Changes in NT-proBNP level and 6MWT distance
Таблица 5. Динамика NT-proBNP и Т6МХ в изучаемых группах

Обсуждение
Выполненное нами исследование подтвердило более выраженную эффективность комбинация АЗМ/ХТД по сравнению с ЛОЗ/ГХТ в снижении как офисного АД, так и суточного периферического АД у пациентов с АГ и СНсФВ.
В двойном слепом рандомизированном многоцентровом исследовании продемонстрировано преимущество фиксированной комбинации АЗМ/ХТД по сравнению с комбинацией олмесартана медоксомила/ГХТ в снижении САД и ДАД [30]. Через 12 нед в группе АЗМ/ХТД отмечено снижение офисных САД (на 43 мм рт.ст.) и ДАД (на 19 мм рт.ст.), а также динамика САД и ДАД по данным СМАД (соответственно на 34 и 19 мм рт.ст.), что согласуется с нашими данными.
В исследовании Ж.Д. Кобалава и соавт. [21] было продемонстрировано, что комбинация АЗМ/ХТД по сравнению с комбинацией АЗМ/индапамид-ретард сопровождалась более выраженным антигипертензивным эффектом в отношении клинического периферического АД, а также нормализацией суточного профиля АД. Показано, что уровня среднесуточного АД<130/<80 мм рт.ст. достигли 40% пациентов, получавших терапию комбинацией АЗМ/ХТД по сравнению с 32% пациентов, получавшими комбинацию АЗМ/индапамид-ретард (р<0,05) [21].
В нашем исследовании через 12 нед 82% пациентов группы АЗМ/ХТД достигли уровня среднесуточного АД<130/<80 мм рт.ст. по сравнению с 67% пациентов группы ЛОЗ/ГХТ (p<0,05). Целевого офисного АД через 12 нед достигли 92% пациентов первой группы и 78% пациентов второй группы.
Имеются данные о значимом снижении офисного и суточного центрального САД и улучшение показателей артериальной ригидности у пациентов с неконтролируемой АГ и СД 2 типа [31].
В нашем исследовании АГТ применение фиксированной комбинации АЗМ/ХТД по сравнению с комбинацией ЛОЗ/ГХТ сопровождалась улучшением, в том числе, показателей центрального АД, что было также показано в исследовании Н.Б. Перепеч и соавт. у пациентов с АГ и метаболическим синдромом [32]. Также продемонстрирована эффективность и безопасность АЗМ у пациентов с метаболическими нарушениями в исследовании CONSTANT [33].
На сегодняшний день имеется большая доказательная база, демонстрирующая значение ХТД в снижении риска сердечно-сосудистых осложнений у пациентов с АГ. В исследовании MRFIT впервые показана клиническая польза ХТД при сравнении с ГХТ [34], снижение смертности от ишемической болезни сердца на 58,2% в группе пациентов, принимавших ХТД, а также снижение риска сердечно-сосудистых осложнений на 21% при сравнении с пациентами, получавшими ГХТ (отношение рисков 0,79; 95% доверительный интервал 0,68-0,92; р=0,0016) [35].
В нашем исследовании у пациентов с АГ и СНсФВ на фоне терапии фиксированной комбинацией АЗМ/ХТД при сравнении с терапией ЛОЗ/ГХТ отмечены более выраженное увеличение проходимой дистанции в ТШХ, снижение уровня NT-proBNP и достижение статуса эуволемии по данным БИВА. В ряде клинических исследований подтверждено, что при приеме АГТ уменьшается частота развития СНсФВ [6][35][36].
Ограничения исследования. Ограничения нашего исследования связаны с небольшой выборкой пациентов и относительно коротким сроком наблюдения в течение 12 нед.
Очевидна необходимость крупного рандомизированного клинического исследования, в котором бы изучали эффективность фиксированной комбинации АЗМ/ХТД в отношении функционального состояния и прогноза у пациентов с СНсФВ.
Заключение
У пациентов с АГ и СНсФВ терапия фиксированной комбинацией АЗМ/ХТД при сравнении с терапией ЛОЗ/ГХТ привела к более выраженному снижению суточного и периферического АД, центрального АД, уровня NTproBNP, увеличению дистанции при прохождении ТШХ и достижению статуса эуволемии, что позволяет рекомендовать применение комбинации АЗМ/ХЛТ у пациентов с СНсФВ, имеющих неконтролируемую или нелеченную АГ.
Отношения и Деятельность. Нет.
Relationships and Activities. None.
Финансирование: Исследование проведено при поддержке Российского университета дружбы народов.
Funding: The study was performed with the support of the Peoples Friendship University of Russia.
Список литературы
1. Dunlay SM, Roger VL, Redfield MM. Epidemiology of heart failure with preserved ejection fraction. Nat Rev Cardiol. 2017;14(10):591-602. DOI:10.1038/nrcardio.2017.65.
2. Slivnick J, Lampert BC. Hypertension and Heart Failure. Heart Fail Clin. 2019;15(4):531-41. DOI:10.1016/j.hfc.2019.06.007.
3. Gladden JD, Chaanine AH, Redfield MM. Heart Failure with Preserved Ejection Fraction. Annu Rev Med. 2018;69:65-79. DOI:10.1146/annurev-med-041316-090654.
4. Tadic M, Cuspidi C, Frydas A, Grassi G. The role of arterial hypertension in development heart failure with preserved ejection fraction: just a risk factor or something more? Heart Fail Rev. 2018;23(5):6319. DOI:10.1007/s10741-018-9698-8.
5. Мареев В. Ю., Даниелян М. О., Беленков Ю. Н. Сравнительная характеристика больных с ХСН в зависимости от величины ФВ по результатам Российского многоцентрового исследования ЭПОХА О ХСН: снова о проблеме ХСН с сохраненной систолической функцией ЛЖ. Журнал Сердечная Недостаточность. 2006;7(4):164-71.
6. Pfeffer MA. Heart Failure and Hypertension: Importance of Prevention. Med Clin North Am. 2017;101(1):19-28. DOI:10.1016/j.mcna.2016.08.012.
7. Piepoli MF, Adamo M, Barison A, et al. Preventing heart failure: a position paper of the Heart Failure Association in collaboration with the European Association of Preventive Cardiology. Eur J Heart Fail. 2022 Jan;24(1):143-68. DOI:10.1002/ejhf.2351.
8. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA. 2002;288(23):2981-97. DOI:10.1001/jama.288.23.2981.
9. Grimm RH, Davis BR, Piller LB, et al. ALLHAT Collaborative Research Group. Heart failure in ALLHAT: did blood pressure medication at study entry influence outcome? J Clin Hypertens (Greenwich). 2009;11(9):466-74. DOI:10.1111/j.1751-7176.2009.00149.x.
10. Davis BR, Kostis JB, Simpson LM, et al. ALLHAT Collaborative Research Group. Heart failure with preserved and reduced left ventricular ejection fraction in the antihypertensive and lipid-lowering treatment to prevent heart attack trial. Circulation. 2008;118(22):2259-67. DOI:10.1161/CIRCULATIONAHA.107.762229.
11. Chen P, Chaugai S, Zhao F, Wang DW. Cardioprotective Effect of Thiazide-Like Diuretics: A MetaAnalysis. Am J Hypertens. 2015;28(12):1453-63. DOI:10.1093/ajh/hpv050.
12. Pareek AK, Messerli FH, Chandurkar NB, Dharmadhikari SK, et al. Efficacy of Low-Dose Chlorthalidone and Hydrochlorothiazide as Assessed by 24-h Ambulatory Blood Pressure Monitoring. J Am Coll Cardiol. 2016;67(4):379-89. DOI:10.1016/j.jacc.2015.10.083.
13. Ernst ME, Carter BL, Goerdt CJ, et al. Comparative antihypertensive effects of hydrochlorothiazide and chlorthalidone on ambulatory and office blood pressure. Hypertension. 2006;47(3):352-8. DOI:10.1161/01.HYP.0000203309.07140.d3.
14. Sica D, White WB, Weber MA, et al. Comparison of the novel angiotensin II receptor blocker azilsartan medoxomil vs valsartan by ambulatory blood pressure monitoring. J Clin Hypertens (Greenwich). 2011;13(7):467-72. DOI:10.1111/j.1751-7176.2011.00482.x.
15. Rakugi H, Enya K, Sugiura K, Ikeda Y. Comparison of the efficacy and safety of azilsartan with that of candesartan cilexetil in Japanese patients with grade I-II essential hypertension: a randomized, double-blind clinical study. Hypertens Res. 2012; 35(5):552-8. DOI:10.1038/hr.2012.8.
16. Bakris GL, Sica D, Weber M, et al. The comparative effects of azilsartan medoxomil and olmesartan on ambulatory and clinic blood pressure. J Clin Hypertens (Greenwich). 2011;13(2):81-8. DOI:10.1111/j.1751-7176.2010.00425.x.
17. White WB, Weber MA, Sica D, et al. Effects of the angiotensin receptor blocker azilsartan medoxomil versus olmesartan and valsartan on ambulatory and clinic blood pressure in patients with stages 1 and 2 hypertension. Hypertension. 2011;57(3):413-20. DOI:10.1161/HYPERTENSIONAHA.110. 163402.
18. Wang JG, Zhang M, Feng YQ, et al. Is the newest angiotensin-receptor blocker azilsartan medoxomil more efficacious in lowering blood pressure than the older ones? A systematic review and network meta-analysis. J Clin Hypertens (Greenwich). 2021;23(5):901-14. DOI:10.1111/jch.14227.
19. Недогода С.В., Чумачек Е.В., Цома В.В., и др. Возможности азилсартана в коррекции инсулинорезистентности и уровня адипокинов при артериальной гипертензии в сравнении с другими сартанами. Российский Кардиологический Журнал. 2019;(1):70-9. DOI:10.15829/1560-4071-2019-1-70-79.
20. Bakris GL, Sica D, White WB, et al. Antihypertensive efficacy of hydrochlorothiazide vs chlorthalidone combined with azilsartan medoxomil. Am J Med. 2012;125(12):1229.e1-1229.e10. DOI:10.1016/j.amjmed.2012.05.023.
21. Кобалава Ж.Д., Кулаков В.В., Горева Л.А., Виллевальде С.В. Сравнительные антигипертензивные эффекты хлорталидона и индапамида-ретард в комбинации с азилсартаном медоксомил у пациентов с артериальной гипертонией. Российский Кардиологический Журнал. 2019;(6):122-30. DOI:10.15829/1560-4071-2019-6-122-130.
22. SPRINT Research Group, Wright JT Jr, Williamson JD, Whelton PK, et al. A Randomized Trial of Intensive versus Standard Blood-Pressure Control. N Engl J Med. 2015;373(22):2103-16. DOI:10.1056/NEJMoa1511939.
23. Pieske B, Tschöpe C, de Boer RA, et al. How to diagnose heart failure with preserved ejection fraction: the HFA-PEFF diagnostic algorithm: a consensus recommendation from the Heart Failure Association (HFA) of the European Society of Cardiology (ESC). Eur Heart J. 2019;40(40):3297317. DOI:10.1093/eurheartj/ehz641.
24. Lancellotti P, Pellikka PA, Budts W, et al. The clinical use of stress echocardiography in non-ischaemic heart disease: recommendations from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. Eur Heart J Cardiovasc Imaging. 2016;17(11):1191-1229. DOI:10.1093/ehjci/jew190.
25. Маматов Б.М., Виллевальде С.В., Клименко А.С., Кобалава Ж.Д. Значение биоимпедансного векторного анализа в диагностике субклинического застоя крови у пациентов с декомпенсацией сердечной недостаточности Клиническая Фармакология и Терапия. 2016;25(5):45-9.
26. Park CS, Lee SE, Cho HJ, et al. Body fluid status assessment by bio-impedance analysis in patients presenting to the emergency department with dyspnea. Korean J Intern Med. 2018;33(5):91121. DOI:10.3904/kjim.2016.358.
27. Parrinello G, Paterna S, Di Pasquale P, et al. The usefulness of bioelectrical impedance analysis in differentiating dyspnea due to decompensated heart failure. J Card Fail. 2008;14(8):676-86. DOI:10.1016/j.cardfail.2008.04.005.
28. Alves FD, Souza GC, Aliti GB, et al. Dynamic changes in bioelectrical impedance vector analysis and phase angle in acute decompensated heart failure. Nutrition. 2015;31(1):84-9. DOI:10.1016/j.nut.2014.05.004.
29. Koell B, Zotter-Tufaro C, Duca F, et al. Fluid status and outcome in patients with heart failure and preserved ejection fraction. Int J Cardiol. 2017;230:476-481. DOI:10.1016/j.ijcard.2016.12.080.
30. Cushman WC, Bakris GL, White WB, et al. Azilsartan medoxomil plus chlorthalidone reduces blood pressure more effectively than olmesartan plus hydrochlorothiazide in stage 2 systolic hypertension. Hypertension. 2012;60(2):310-8. DOI:10.1161/HYPERTENSIONAHA.111.188284.
31. Starostina E, Troitskaya E, Kulakov V, et al. Azilsartan medoxomil decreases 24-h central BP and arterial stiffness in patients with arterial hypertension and type 2 diabetes mellitus. J Hypertens. 2017;35 (e-Supplement 2): e106.
32. Скибицкий В.В., Фендрикова А.В., Сиротенко Д.В., и др. Хронотерапевтические аспекты эффективности азилсартана медоксомила в составе комбинированнои терапии у пациентов с артериальной гипертонией й метаболическим синдромом. Кардиология. 2016;56(10):35-40. DOI:10.18565/cardio.2016. 10.35-40.
33. Перепеч Н.Б., Чазова И.Е., Жернакова Ю.В. от имени участников исследования. Эффективность и безопасность азилсартана медоксомила в различных дозах и режимах назначения у пациентов с метаболическими нарушениями по данным исследования CONSTANT. Системные Гипертензии. 2021;18(3):130-9. DOI:10.26442/2075082X.2021.3.201078.
34. Five-year findings of the hypertension detection and follow-up program. I. Reduction in mortality of persons with high blood pressure, including mild hypertension. Hypertension Detection and Followup Program Cooperative Group. JAMA. 1979;242(23):2562-71.
35. Multiple Risk Factor Intervention Trial Research Group. Mortality after 10 1/2 years for hypertensive participants in the Multiple Risk Factor Intervention Trial. Circulation. 1990;82(5):1616-28. DOI:10.1161/01.cir.82.5.1616.
36. Shah SJ, Borlaug BA, Kitzman DW, et al. Research Priorities for Heart Failure With Preserved Ejection Fraction: National Heart, Lung, and Blood Institute Working Group Summary. Circulation. 2020;141(12):1001-26. DOI:10.1161/CIRCULATIONAHA.119.041886.
Об авторах
Ж. Д. КобалаваРоссия
Кобалава Жанна Давидовна
Москва
А. Ф. Сафарова
Россия
Сафарова Айтен Фуад кызы
Москва
Х. М. Гудиева
Россия
Гудиева Хяди Магометовна
Москва
М. А. Маркова
Россия
Маркова Мария Александровна
Москва
А. Е. Петросян
Россия
Петросян Ануш Егоровна
Москва
Рецензия
Для цитирования:
Кобалава Ж.Д., Сафарова А.Ф., Гудиева Х.М., Маркова М.А., Петросян А.Е. Сравнительная эффективность фиксированных комбинаций азилсартана медоксомила/хлорталидона и лозартана/гидрохлортиазида у пациентов с артериальной гипертензией и сердечной недостаточностью с сохранной фракцией выброса. Рациональная Фармакотерапия в Кардиологии. 2022;18(2):127-134. https://doi.org/10.20996/1819-6446-2022-04-01
For citation:
Kobalava Zh.D., Safarova A.F., Gudieva Kh.M., Markova M.A., Petrosyan A.E. Comparative Efficacy of Single Pill Combinations of Azilsartan Medoxomil/Chlorthalidone and Losartan/Hydrochlorothiazide in Patients with Hypertension and Heart Failure with Preserved Ejection Fraction. Rational Pharmacotherapy in Cardiology. 2022;18(2):127-134. (In Russ.) https://doi.org/10.20996/1819-6446-2022-04-01

















































