Перейти к:
Влияние носительства гена ABCB1 и межлекарственных взаимодействий на фармакокинетику апиксабана и ривароксабана и клинические исходы у пациентов с фибрилляцией предсердий и тромбозом глубоких вен
https://doi.org/10.20996/1819-6446-2022-12-02
Аннотация
Цель. Изучить влияние носительства гена ABCB1 и межлекарственных взаимодействий на фармакокинетику апиксабана и клинические исходы у пациентов с фибрилляцией предсердий и тромбозом глубоких вен.
Материал и методы. В исследовании принимали участие пациенты, госпитализированные в ГКБ им. С.С. Юдина. Всего было включено 92 пациента (50 пациентов получали апиксабан и 42 – ривароксабан) с неклапанной фибрилляцией предсердий и тромбозом глубоких вен. Генотипирование осуществляли методом полимеразной цепной реакции в режиме реального времени. Измерение концентраций прямых оральных антикоагулянтов проводилось с помощью масс-спектрометра с ионизацией электроспреем в режиме положительной ионизации.
Результаты. Мы обнаружили, что у пациентов – носителей генотипа CT+TT ABCB1 (rs4148738) C>T, кодирующего белок-переносчик (P-gp), статистически значимо была выше концентрация ривароксабана в плазме крови (p=0,026). Кроме того, мы выявили, что у пациентов на фоне приема апиксабана совместно с ингибитором CYP3A4/P-gp в 3,5 раза чаще встречались геморрагические осложнения, чем без ингибиторов (р=0,004).
Заключение. В результате проведенного нами исследования выявлено, что у пациентов, носителей аллели Т полиморфизма ABCB1 (rs4148738) C>T, концентрация ривароксабана в плазме крови была выше, а у пациентов, принимающих апиксабан совместно с ингибитором CYP3A4/P-gp, был выше риск геморрагических осложнений в отличие от пациентов, не принимающих такие препараты. Необходимы дальнейшие исследования влияния фармакогенетики и фармакокинетики на профиль безопасности и эффективности апиксабана и ривароксабана с учетом тренда системного подхода к оптимизации антикоагулянтной терапии прямыми оральными антикоагулянтами на основании фармакокинетических, фармакогенетических биомаркеров.
Ключевые слова
Для цитирования:
Федина Л.В., Сычев И.Н., Растворова Т.Д., Стригункова Е.В., Качанова А.А., Созаева Ж.А., Бочков П.О., Варданян А.В., Мирзаев К.Б., Сычев Д.А. Влияние носительства гена ABCB1 и межлекарственных взаимодействий на фармакокинетику апиксабана и ривароксабана и клинические исходы у пациентов с фибрилляцией предсердий и тромбозом глубоких вен. Рациональная Фармакотерапия в Кардиологии. 2022;18(6):624-629. https://doi.org/10.20996/1819-6446-2022-12-02
For citation:
Fedina L.V., Sychev I.N., Rastvorova T.D., Strigunkova E.V., Kachanova A.A., Sozaeva Z.A., Bochkov P.O., Vardanyan A.V., Mirzayev K.B., Sychev D.A. Effect of ABCB1 Gene Carriage and Drug-Drug Interactions on Apixaban and Rivaroxaban Pharmacokinetics and Clinical Outcomes in Patients with Atrial Fibrillation and Deep Vein Thrombosis. Rational Pharmacotherapy in Cardiology. 2022;18(6):624-629. (In Russ.) https://doi.org/10.20996/1819-6446-2022-12-02
Введение
Прямые оральные антикоагулянты (ПОАК) – современная группа антикоагулянтов, применяющихся у пациентов с неклапанной фибрилляцией предсердий (ФП) для профилактики тромбоэмболических осложнений после эндопротезирования коленного и тазобедренного сустава, а также лечения тромбоза глубоких вен нижних конечностей (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) [1].
Для ривароксабана и апиксабана мишенью действия является активный центр Ха фактора в свободном состоянии и в протромбиназном комплексе (комплекс Ха, Vа и Ca2+) [2]. Связывая эти звенья, ПОАК препятствуют образованию фибрина из фибриногена и дальнейшему формированию тромба [2].
Рост потребления ПОАК, имеющих ряд преимуществ по сравнению с варфарином в виде улучшенного профиля эффективности и безопасности ассоциирован с неизбежным ростом серьёзных и даже фатальных нежелательных лекарственных реакций при применении данных препаратов – геморрагических осложнений, что подтверждается многочисленными клиническими исследованиями [3]. Во вторичном анализе многоцентровых рандомизированных клинических исследований III фазы было показано, что высокие концентрации ПОАК в плазме коррелируют с большей частотой нежелательных лечебных реакций в виде кровотечений [4-6], и наоборот, недавние обсервационные исследования выявили взаимосвязь между низкими плазменными уровнями ПОАК, измеренными в первый месяц лечения, и возникновением тромбоэмболических осложнений [7].
В вариабельность фармакологического ответа на ПОАК вносят вклад различные клиническо-демографические (возраст, нарушение функции почек, расовая и этническая принадлежность, пол, курение, межлекарственные взаимодействия, диета и др.) и генетические факторы (полиморфизм генов, кодирующих изоферменты цитохрома Р-450 и транспортеры лекарственных средств и др.) [8]. Ривароксабан и апиксабан являются субстратами P-гликопротеина (P-gp), трансмембранного белка-транспортера, который осуществляет эффлюкс антикоагулянтов из просвета желудочно-кишечного тракта, а также участвует в их печеночной и почечной элиминации и кодируется геном ABCB1 [9]. Кроме того, ривароксабан и апиксабан имеют CYP450-опосредованный метаболизм (ривароксабан, в основном, через CYP3A4 (~18%), с незначительным участием CYP2J2 (~14%), а апиксабан метаболизируется через CYP3A4 (~15%), и в меньшей степени – через CYP2C19, CYP1A2, CYP2C8 и CYP2C9 [10]. Знание фармакокинетики апиксабана и ривароксабана позволяет выделить гены-кандидаты, для оценки взаимосвязи носительства конкретных аллельных вариантов генов с риском нежелательных лечебных реакций на фоне терапии, и прежде всего – кровотечений. Соответственно, можно предположить, что носительство следующих полиморфных маркеров может повлиять на безопасность терапии апиксабаном и ривароксабаном: CYP3A4*22, CYP3A5*3, ABCB1 rs1045642 (3435С>T) и rs4148738 [11].
Таким образом, для оптимизации клинической эффективности и максимальной безопасности современной антикоагулянтной терапии необходим системный индивидуальный подход на основе фармакокинетических исследований и фармакогенетического тестирования, которые позволят прогнозировать и предотвращать развитие геморрагических осложнений у пациентов, принимающих ПОАК.
Цель исследования – изучить влияние полиморфных маркеров генов CYP3A4*22 (rs35599367) C>T и CYP3A5*3 A>G, кодирующих ферменты, метаболизирующие апиксабан и ривароксабан и ABCB1 (rs4148738) C>T, ABCB1 (rs1045642) C>T, кодирующих P-гликопротеин, а также определить влияние ингибиторов CYP3A4 и P-гликопротеина на фармакокинетику апиксабана и ривароксабана у пациентов с ФП и ТГВ, и оценить безопасность применения пероральных антикоагулянтов.
Материал и методы
Дизайн исследования и популяция пациентов
В открытое проспективное обсервационное исследование было включено 92 пациента (50 пациентов получали апиксабан и 42 – ривароксабан) с неклапанной ФП и ТГВ. В исследовании принимали участие пациенты, госпитализированные в ГКБ им. С.С. Юдина. Критерии включения: подтвержденный диагноз неклапанной ФП (отсутствие искусственных клапанов сердца); подтвержденный диагноз ТГВ; подтвержденный диагноз ТЭЛА и прием апиксабана в рекомендованных дозах. Критерии невключения: повышенная чувствительность к апиксабану или вспомогательным компонентам препарата; подтвержденный диагноз клапанной ФП (наличие искусственных клапанов сердца или митрального стеноза); нарушение функции почек с клиренсом креатинина менее 15 мл/мин или процедура диализа; тяжелая печеночная недостаточность класс В, С по Чайлд-Пью; геморрагический синдром, активное внутреннее кровотечение, внутричерепное кровоизлияние; врожденный дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция; возраст до 18 лет; беременность или период грудного вскармливания. Все пациенты получали апиксабан (в дозах 2,5 мг 2 р/сут, 5 мг 2 р/сут или 10 мг 2 р/сут) и ривароксабан (в дозах 20 мг 1 р/сут, 15 мг 1 р/сут или 15 мг/ 2 р/сут) в соответствии с инструкцией по применению препарата. Исследование было одобрено заседанием локального этического комитета ФГБОУ ДПО РМАНПО Российской медицинской академией непрерывного профессионального образования Минздрава России (Протокол № 12 от 20 октября 2021 г.) и проводилось в соответствии с Хельсинкской декларацией, все пациенты дали информированное согласие на участие.
Измерение плазменной концентрации апиксабана и ривароксабана
Взятие плазмы крови для измерения минимальной равновесной концентрации апиксабана и ривароксабана в плазме крови осуществлялся перед очередным приемом ПОАК (на 4-6 день от начала приема ривароксабана или апиксабана) с использованием вакуумных пробирок VACUETTE® (Greiner Bio-One, Австрия) с гепарином натрия. Определение концентрации апиксабана и ривароксабана в крови проводили методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием. Пробы анализировали на жидкостном хроматографе Agilent 1200 (в составе четырехканальный насос, дегазатор подвижной фазы, термостат хроматографических колонок). В работе использовалась колонка Agilent Extend-C18 (длина 100 мм; внутренний диаметр 2,1 мм; зернение 3,5 мкм). Разделение проводили при температуре колонки 40°C. Подвижная фаза: раствор «А» (50 мл 0,1 М раствора ацетата аммония и 5 мл муравьиной кислоты разбавляли водой, деионизованной до общего объема 1 л) и раствор «Б» (50 мл 0,1 М раствора ацетата аммония и 5 мл муравьиной кислоты разбавляли ацетонитрилом до общего объема 1 л). Хроматографическое разделение проводили в изократическом режиме элюирования при соотношении компонентов «А»:«Б» 70:30. Скорость потока подвижной фазы составляла 0,3 мл/мин. Объем вводимой пробы – 10 мкл. Анализ проводили в течение 7 мин. В работе использовали масс-спектрометр (тип тройной квадруполь) Agilent Triple Quad LC/MS 6410 с ионизацией электроспреем в режиме положительной ионизации. Регистрацию спектров ривароксабана проводили в режиме множественных молекулярных реакций. Давление газа распылителя 35 psi. Объемная скорость осушающего газа 11 л/мин, температура 350°C. Значение напряжения фрагментации составляло 135 В, напряжения на ячейке соударений – 25 В. Пробоподготовку проводили осаждением белков плазмы крови. Образцы плазмы размораживали при комнатной температуре, далее 100 мкл плазмы переносили в пластиковые пробирки типа Eppendorf, добавляли 250 мкл смеси метанола с 0,1% соляной кислотой в соотношении компонентов 9:1, перемешивали на встряхивателе Vortex, оставляли на 10 мин и перемешивали еще раз. Полученные образцы центрифугировали со скоростью вращения 10000 об/мин в течение 10 мин. Надосадочный слой переносили в хроматографическиевиалы и помещали на автосемплер хроматографа.
Генотипирование
Для отбора генов-кандидатов в исследование использовали данные по фармакокинетике и фармакодинамике из инструкции по применению препарата и базу данных PharmGKB [11]. Для генотипирования использовали венозную кровь, собранную в вакуумные пробирки VACUETTE® (GreinerBio-One, Автрия) с этилендиаминтетраацетатом. Носительство полиморфных маркеров генов CYP3A4*22 (rs35599367) C>T, CYP3A5*3 A>G, ABCB1 (rs4148738) C>T и ABCB1 (rs1045642) C>T определяли методом полимеразной цепной реакции в реальном времени (Real-Time PCR) с помощью коммерческих наборов (ЗАО «Синтол», Россия; Thermo Fisher Scientific, США) на амплификаторе Real-Time CFX96 Touch (Bio-Rad Laboratories, Inc., США).
Статистическая обработка
Статистический анализ результатов проводился с помощью программы IBM SPSS Statistics 20.0. Все количественные переменные были проверены на нормальное распределение по критерию Шапиро-Уилка, что показало анормальное распределение данных (Z<1,0; p<0,0001). Для последующего анализа количественных переменных между подгруппами применялся непараметрический критерий Манна-Уитни, сравнение частот категориальных переменных проводилось с помощью критерия хи-квадрат Пирсона. Для подтверждения независимого распределения аллелей оценивали соответствие закону Харди-Вайнберга с использованием онлайн-калькулятора [12].
Результаты
Базовая характеристика демографических, клинических и лабораторных признаков представлена в табл. 1. Группы были сопоставимы по полу и возрасту.
Полученные результаты популяционного исследования соответствовали закону Харди-Вайнберга при значении р>0,05 (табл. 2).
CYP3A4*22 (rs35599367) C>T был исключен из анализа, так как среди пациентов, принимающих апиксабан, было обнаружено всего 3 носителя аллели Т, а среди пациентов, принимающих ривароксабан – лишь 2 носителя. Аналогично этому были исключены из анализа CYP3A5*3 A>G и ABCB1 (rs1045642) C>T.
Пациенты с полиморфизмом гена ABCB1 (rs4148738)C>T были разделены на две группы: СС (n=10) и СТ+ТТ (n=40) для апиксабана и СС (n=15) и СТ+ТТ (n=27) для ривароксабана. При оценке сопоставимости сравниваемых групп пациентов статистически значимые различия по факторам, которые могут повлиять на основные и вторичные исходы, не обнаружены. При анализе Манна-Уитни не было обнаружено ассоциаций между носительством полиморфизма ABCB1 (rs4148738) C>T и остаточной равновесной концентрацией апиксабана (p=0,297). У пациентов носителей аллели Т статистически значимо концентрация ривароксабана была выше (p=0,026; табл. 3), при этом не было выявлено увеличения частоты кровотечений у носителей этого полиморфизма (p=0,666).
При оценке фармакокинетики апиксабана и ривароксабана в группах пациентов, принимавших и не принимавших препараты, которые являлись ингибиторами CYP3A4/P-gp (верапамил, амиодарон, дилтиазем), статистически значимых различий выявлено не было, хотя у пациентов, принимавших ривароксабан совместно с ингибиторами CYP3A4/P-gp, отмечалась тенденция к повышению уровня равновесной концентрации [102,6 (44;165) против 60,9 (25;80); p=0,065; табл. 4].
После статистической обработки результатов у пациентов на фоне приема апиксабана совместно с ингибитором CYP3A4/P-gp в 3,5 раза чаще встречались геморрагические осложнения, чем у тех, которые ингибиторы не принимали (57,1 % против 16,7%; р=0,004). При этом у пациентов, получавших ривароксабан совместно с ингибиторами CYP3A4/P-gp, отсутствовали ассоциации с увеличением частоты кровотечений по сравнению с пациентами, которые получали ривароксабан без ингибиторов CYP3A4/P-gp (табл. 5).
Table 1. Baseline clinical and demographic characteristics of patients with AF and DVT
Таблица 1. Исходные клинико-демографические характеристики пациентов с ФП и ТГВ
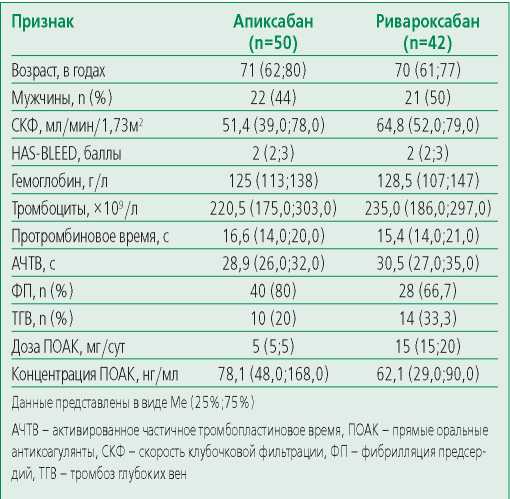
Table 2. Distribution of genotype frequencies of the studied polymorphic variants with the results of Hardy-Weinberg distribution matching analysis
Таблица 2. Распределение частот генотипов изученных полиморфных вариантов с результатами анализа на соответствие распределению по Харди-Вайнбергу
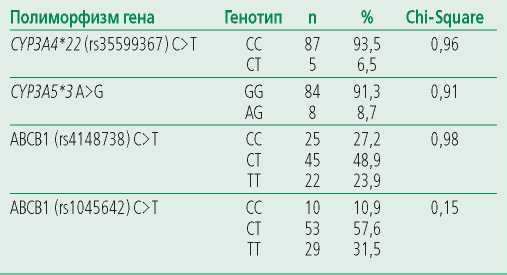
Table 3. Association of ABCB1 gene polymorphism carriage with equilibrium concentration of apixaban and rivaroxaban
Таблица 3. Ассоциация носительства полиморфизма гена ABCB1 с равновесной концентрацией апиксабана и ривароксабана

Table 4. Effect of CYP3A4/P-gp inhibitors on the pharmacokinetics of apixaban and rivaroxaban
Таблица 4. Влияние приема ингибиторов CYP3A4/P-gp на фармакокинетику апиксабана и ривароксабана

Table 5. Effect of CYP3A4/P-gp inhibitors on the incidence of hemorrhagic complications
Таблица 5. Влияние приема ингибиторов CYP3A4/P-gp на частоту развития геморрагических осложнений

Обсуждение
Персонализация терапии ПОАК, в том числе, апиксабана и ривароксабана, является ведущей задачей для обеспечения эффективности и безопасности применения этих препаратов. Важную роль в вариабельности фармакокинетики играют полиморфизмы генов ферментов биотрансформации (СYР3А4/5) а также белков-переносчиков (P-gp) [13]. На данный момент больших исследований в области фармакогенетики ПОАК не так много.
В нашем исследовании мы обнаружили, что у пациентов носителей генотипа CT+TT ABCB1 (rs4148738) C>T, кодирующего белок-переносчик (P-gp), статистически значимо концентрация ривароксабана в плазме крови была выше (p=0,026). По данным систематического обзора и метаанализа, проведенного Q. Xie и соавт., показано, что максимальная равновесная концентрация ниже у носителей ABCB1 rs1045642 CC, чем у носителей TT, и у носителей rs2032582 GG, чем у носителей аллеля A/T, а AUC 0-∞ ниже у носителей rs1045642 CC, чем у носителей TT [14]. В исследовании I. Gouin-Thibault и соавт. два аллельных варианта гена ABCB1 rs2032582 и rs1045642 не показали значительного увеличения пиковых концентраций ривароксабана в когорте здоровых добровольцев [15]. Авторы считают, что полиморфизмы гена ABCB1 нельзя рассматривать, как значимую детерминанту индивидуальной вариабельности фармакокинетики ривароксабана [15]. В исследованиях, проведенных Д.А. Сычевым и соавт., также не было обнаружено существенной разницы в пиковой равновесной концентрации ривароксабана между мутантными гаплотипами и дикими гаплотипами [16][17].
В нашем исследовании не обнаружено ассоциаций между носительством полиморфизма ABCB1 (rs4148738) C>T и остаточной равновесной концентрацией апиксабана (p=0,297), однако носители аллельного варианта CT+TT ABCB1 (rs4148738) C>T имели более высокие пиковые концентрации. В 2016 г. C. Dimatteo и соавт. продемонстрировали связь между интронным вариантом ABCB1 rs4148738 и увеличением пиковой концентрации апиксабана (p<0,05) [18]. В исследовании A.V. Kryukov и соавт. на выборке из 17 пациентов, получавших апиксабан в дозе 10 мг/сут, не было показано значимого влияния ABCB1 rs4148738 на фармакокинетику апиксабана [19].
Апиксабан взаимодействует с препаратами, которые индуцируют или ингибируют CYP3A4 или P-gp [20]. Фармакокинетический анализ сообщает о значительном снижении AUC∞ апиксабана с рифампицином, комбинированным индуктором P-gp и сильным индуктором CYP3A4. Снижение экспозиции препарата может привести к повышению риска тромботических исходов и снижению эффективности [21], и наоборот, комбинированные ингибиторы P-gp и сильные ингибиторы CYP3A4 повышают максимальную концентрацию и AUC∞ апиксабана, что повышает риск кровотечения [22,23]. В нашем исследовании у пациентов на фоне приема апиксабана совместно с ингибитором CYP 3A4/P-gp в 3,5 раза чаще встречались геморрагические осложнения, чем при приеме препарата без ингибиторов (р=0,004).
Ривароксабан имеет такой же профиль межлекарственного взаимодействия, как и апиксабан, поскольку он метаболизируется ферментами CYP3A4/A5 и 2J2 и также является субстратом P-gp [23]. Известно, что умеренные ингибиторы CYP3A4 и P-gp повышают концентрацию ривароксабана в плазме крови, хотя это не коррелирует с повышенным риском кровотечения у пациентов с нормальной функцией почек [24-26]. В нашем исследовании у пациентов, принимавших ривароксабан совместно с ингибиторами CYP3A4/P-gp, отмечалась тенденция к повышению уровня остаточной равновесной концентрации (p=0,065), но при этом не увеличивалась частота развития кровотечений.
Вероятно, следует избегать сочетания апиксабана и ривароксабана с сильным ингибитором CYP3A4 и P-gp, а если комбинация с сильными ингибиторами CYP3A4 неизбежна, можно обсудить возможность снижения дозы апиксабана и ривароксабана на 50% [27]. Эмпирическое снижение стандартных доз ПОАК не рекомендуется при совместном приеме с умеренными ингибиторами CYP3A4 [27].
Заключение
В результате проведенного нами исследования выявлено, что у пациентов – носителей аллели Т полиморфизма ABCB1 (rs4148738)C>T остаточная концентрация ривароксабана в плазме крови была выше, а у пациентов, принимающих апиксабан совместно с ингибитором CYP 3A4/P-gp, был выше риск геморрагических осложнений в отличие от пациентов, не принимающих такие препараты. Необходимы дальнейшие исследования влияния фармакогенетики и фармакокинетики на профиль безопасности и эффективности апиксабана и ривароксабана с учетом системного подхода к оптимизации антикоагулянтной терапии ПОАК на основании фармакокинетических, фармакогенетических биомаркеров.
Отношение и Деятельность. Нет.
Relationships and Activities. None.
Финансирование исследования. Работа выполнена при поддержке гранта Российского научного фонда 22-15-00251 №122060600001-4, «Персонализированное применение прямых пероральных антикоагулянтов на основе фармакогеномного подхода». Авторы не имеют других соответствующих связей или финансового участия с какой-либо организацией или предприятием, имеющим финансовый интерес или финансовый конфликт с предметом или материалами, обсуждаемыми в рукописи, кроме тех, которые были раскрыты.
Funding. This work was supported by Russian Science Foundation grant 22-15-00251 №122060600001-4, “Personalized Use of Direct Oral Anticoagulants Based on a Pharmacogenomic Approach”. The authors have no other relevant affiliations or financial involvement with any organization or enterprise that has a financial interest or financial conflict with the subject matter or materials discussed in the manuscript, other than those disclosed.
Список литературы
1. Kruger PC, Eikelboom JW, Douketis JD, et al. Deep vein thrombosis: update on diagnosis and management. Med J Aust. 2019;210(11):516-24. DOI:10.5694/mja2.50201.
2. Brighton T. New oral anticoagulant drugs - mechanisms of action. Aust Prescr. 2010;33:38-41. DOI:10.18773/austprescr.2010.017.
3. Benamouzig R, Guenoun M, Deutsch D, et al. Review Article: Gastrointestinal Bleeding Risk with Direct Oral Anticoagulants. Cardiovasc Drugs Ther. 2022;36(5):973-89. DOI:10.1007/s10557-021-07211-0
4. Southworth MR, Reichman ME, Unger EF. Dabigatran and postmarketing reports of bleeding. N Engl J Med. 2013;368(14):1272-74. DOI:10.1056/NEJMp1302834.
5. Giugliano RP, Ruff CT, Braunwald E, et al. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2013;369(22):2093-104. DOI:10.1056/NEJMoa1310907.
6. Lip GYH, Keshishian A, Li X, et al. Effectiveness and Safety of Oral Anticoagulants Among Nonvalvular Atrial Fibrillation Patients. Stroke. 2018;49(12):2933-44. DOI:10.1161/STROKEAHA.118.020232.
7. Overvad TF, Larsen TB, Albertsen IE, et al. Balancing bleeding and thrombotic risk with new oral anticoagulants in patients with atrial fibrillation. Expert Rev Cardiovasc Ther. 2013;11(12):1619-29. DOI:10.1586/14779072.2013.839214.
8. Скрипка А.И., Когай В.В., Листратов А.И. и др. Персонализированный подход к назначению прямых оральных антикоагулянтов: от теории к практике. Тер Архив. 2019;91(7):111-20. DOI:10.26442/00403660.2019.07.000045.
9. Byon W, Garonzik S, Boyd RA, et al. Apixaban: A Clinical Pharmacokinetic and Pharmacodynamic Review. Clin Pharmacokinet. 2019;58(10):1265-79. DOI:10.1007/s40262-019-00775-z.
10. Wiggins BS, Dixon DL, Neyens RR, et al. Select Drug-Drug Interactions With Direct Oral Anticoagulants: JACC Review Topic of the Week. J Am Coll Cardiol. 2020;75(11):1341-50. DOI:10.1016/j.jacc.2019.12.068.
11. PharmGKB [cited 2022 Oct 13]. Available from: https://www.pharmgkb.org/.
12. Online Calculator of Hardy-Weinberg equilibrium. WpCalc. [cited 2022 Oct 2]. Available from: https://wpcalc.com/en/equilibrium-hardy-weinberg/.
13. Raymond J, Imbert L, Cousin T, et al. Pharmacogenetics of Direct Oral Anticoagulants: A Systematic Review. J Pers Med. 2021;11(1):37. DOI:10.3390/jpm11010037.
14. Xie Q, Xiang Q, Mu G, et al. Effect of ABCB1 Genotypes on the Pharmacokinetics and Clinical Outcomes of New Oral Anticoagulants: A Systematic Review and Meta-analysis. Curr Pharm Des. 2018;24(30):3558-65. DOI:10.2174/1381612824666181018153641.
15. Gouin-Thibault I, Delavenne X, Blanchard A, et al. Interindividual variability in dabigatran and rivaroxaban exposure: contribution of ABCB1 genetic polymorphisms and interaction with clarithromycin. J Thromb Haemost. 2017;15(2):273-83. DOI:10.1111/jth.13577.
16. Sychev D, Minnigulov R, Bochkov P, et al. Effect of CYP3A4, CYP3A5, ABCB1 Gene Polymorphisms on Rivaroxaban Pharmacokinetics in Patients Undergoing Total Hip and Knee Replacement Surgery. High Blood Press Cardiovasc Prev. 2019;26(5):413-20. DOI:10.1007/s40292-019-00342-4.
17. Sychev D, Ostroumova O, Cherniaeva M, et al. The Influence of ABCB1 (rs1045642 and rs4148738) Gene Polymorphisms on Rivaroxaban Pharmacokinetics in Patients Aged 80 Years and Older with Nonvalvular Atrial Fibrillation. High Blood Press Cardiovasc Prev. 2022;29(5):469-80. DOI:10.1007/s40292-022-00536-3.
18. Dimatteo C, D’Andrea G, Vecchione G, et al. ABCB1 SNP rs4148738 modulation of apixaban interindividual variability. Thromb Res. 2016;145:24-6. DOI:10.1016/j.thromres.2016.07.005.
19. Kryukov AV, Sychev DA, Andreev DA, et al. Influence of ABCB1 and CYP3A5 gene polymorphisms on pharmacokinetics of apixaban in patients with atrial fibrillation and acute stroke. Pharmgenomics Pers Med. 2018;11:43-9. DOI:10.2147/PGPM.S157111.
20. Terrier J, Gaspar F, Fontana P, et al. Drug-Drug Interactions with Direct Oral Anticoagulants: Practical Recommendations for Clinicians. Am J Med. 2021;134(8):939-42. DOI:10.1016/j.amjmed.2021.04.003.
21. Vakkalagadda B, Frost C, Byon W, et al. Effect of Rifampin on the Pharmacokinetics of Apixaban, an Oral Direct Inhibitor of Factor Xa. Am J Cardiovasc Drugs. 2016;16(2):119-27. DOI:10.1007/s40256-015-0157-9.
22. Frost CE, Byon W, Song Y, et al. Effect of ketoconazole and diltiazem on the pharmacokinetics of apixaban, an oral direct factor Xa inhibitor. Br J Clin Pharmacol. 2015;79(5):838-46. DOI:10.1111/bcp.12541.
23. Mikus G, Foerster KI, Schaumaeker M, et al. Application of a microdosed cocktail of 3 oral factor Xa inhibitors to study drug-drug interactions with different perpetrator drugs. Br J Clin Pharmacol. 2020;86(8):1632-41. DOI:10.1111/bcp.14277.
24. Mueck W, Kubitza D, Becka M. Co-administration of rivaroxaban with drugs that share its elimination pathways: pharmacokinetic effects in healthy subjects. Br J Clin Pharmacol. 2013;76(3):455-66. DOI:10.1111/bcp.12075.
25. Bartlett JW, Renner E, Mouland E, et al. Clinical Safety Outcomes in Patients With Nonvalvular Atrial Fibrillation on Rivaroxaban and Diltiazem. Ann Pharmacother. 2019;53(1):21-7. DOI:10.1177/1060028018795140.
26. Pham P, Schmidt S, Lesko L, et al. Association of Oral Anticoagulants and Verapamil or Diltiazem With Adverse Bleeding Events in Patients With Nonvalvular Atrial Fibrillation and Normal Kidney Function. JAMA Netw Open. 2020;3(4):e203593. DOI:10.1001/jamanetworkopen.2020.3593.
27. Mar PL, Gopinathannair R, Gengler BE, et al. Drug Interactions Affecting Oral Anticoagulant Use. Circ Arrhythm Electrophysiol. 2022;15(6):e007956. DOI:10.1161/CIRCEP.121.007956.
Об авторах
Л. В. ФединаРоссия
Федина Людмила Владимировна
Москва
eLibrary SPIN1961-7486
И. Н. Сычев
Россия
Сычев Игорь Николаевич
Москва
eLibrary SPIN 7282-6014
Т. Д. Растворова
Россия
Растворова Татьяна Дмитриевна
Москва
Е. В. Стригункова
Россия
Стригункова Евгения Владимировна
Москва
А. А. Качанова
Россия
Качанова Анастасия Алексеевна
Москва
eLibrary SPIN1214-8156
Ж. А. Созаева
Россия
Созаева Жаннет Алимовна
Москва
eLibrary SPIN 4138-4466
П. О. Бочков
Россия
Бочков Павел Олегович
Москва
eLibrary SPIN5576-8174
А. В. Варданян
Россия
Варданян Аршак Варданович
Москва
К. Б. Мирзаев
Россия
Мирзаев Карин Бадавиевич
Москва
eLibrary SPIN 8308-7599
Д. А. Сычев
Россия
Сычев Дмитрий Алексеевич
Москва
eLibrary SPIN4525-7556
Рецензия
Для цитирования:
Федина Л.В., Сычев И.Н., Растворова Т.Д., Стригункова Е.В., Качанова А.А., Созаева Ж.А., Бочков П.О., Варданян А.В., Мирзаев К.Б., Сычев Д.А. Влияние носительства гена ABCB1 и межлекарственных взаимодействий на фармакокинетику апиксабана и ривароксабана и клинические исходы у пациентов с фибрилляцией предсердий и тромбозом глубоких вен. Рациональная Фармакотерапия в Кардиологии. 2022;18(6):624-629. https://doi.org/10.20996/1819-6446-2022-12-02
For citation:
Fedina L.V., Sychev I.N., Rastvorova T.D., Strigunkova E.V., Kachanova A.A., Sozaeva Z.A., Bochkov P.O., Vardanyan A.V., Mirzayev K.B., Sychev D.A. Effect of ABCB1 Gene Carriage and Drug-Drug Interactions on Apixaban and Rivaroxaban Pharmacokinetics and Clinical Outcomes in Patients with Atrial Fibrillation and Deep Vein Thrombosis. Rational Pharmacotherapy in Cardiology. 2022;18(6):624-629. (In Russ.) https://doi.org/10.20996/1819-6446-2022-12-02

















































