Перейти к:
Активный дистанционный врачебный патронаж пациентов, перенесших инфаркт миокарда: есть ли преимущества перед стандартным амбулаторным наблюдением?
https://doi.org/10.20996/1819-6446-2024-3011
EDN: XKNPWA
Аннотация
Цель. Сравнить клиническую эффективность двух программ ведения пациентов в течение 12 мес. после инфаркта миокарда (ИМ) — стандартное амбулаторное наблюдение или ведение в комбинации с дополнительным активным дистанционным врачебным патронажем.
Материал и методы. В анализ вошли 150 пациентов с нефатальным ИМ в возрасте от 35 до 70 лет. К выписке пациенты рандомизированы в группы с разными программами дальнейшего наблюдения в течение 12 мес. после ИМ — группы стандартного амбулаторного наблюдения (n=75) или его комбинации с активным дистанционным врачебным патронажем (n=75). Через год после ИМ оценивались витальный статус; частота экстренных сердечно-с осудистых госпитализаций, обусловленных коронарной недостаточностью; фактическая приверженность к терапии и регулярному амбулаторному наблюдению; достижение целевых параметров сердечно- сосудистого здоровья; динамика поведенческих факторов риска.
Результаты. В группе пациентов с ИМ, находящихся в течение 12 мес. в программе с комбинированным стандартным амбулаторным наблюдением и дистанционным врачебным патронажем, по сравнению с пациентами со стандартным наблюдением, зарегистрировано в 4,8 раз меньше комбинированных ишемических событий (р<0,001); в 4,7 раз ниже была доля экстренных госпитализаций по сердечно-с осудистой причине (р<0,001). Было показано, что пациенты, наблюдавшиеся в программе с комбинированным стандартным амбулаторным наблюдением и дистанционным врачебным патронажем на протяжении года в 1,7 раз чаще осуществляли регулярные визиты в поликлинику (р<0,001). За год пациентами с активным наблюдением в большей степени были достигнуты поведенческие изменения — в 1,6 раз больше была доля пациентов, сообщивших об увеличении недельной физической активности (р=0,013) и об уменьшении количества периодов ежемесячного стресса или их полном отсутствии на работе и/или дома (р=0,020), в 1,8 раз чаще указавших на снижение частоты ежемесячного употребления алкоголя и уменьшение количества порций (p=0,001), а также изменения в структуре питания. Пациенты, подвергшиеся дополнительному дистанционному врачебному патронажу, в 1,2 раза чаще указали на снижение суточного употребления поваренной соли (р=0,011), в 1,3 раза чаще отметили добавление в рацион диетического мяса (р=0,003), в 1,1 раз чаще — свежих и приготовленных овощей (>300 г в неделю) (р=0,032), в 1,4 раза чаще — свежих фруктов и ягод (>300 г в неделю) (р=0,003), в 1,2 раза чаще сообщили о снижении употребления сложных углеводов до > ¼ части тарелки в сутки (р=0,036).
Заключение. Оригинальная программа комбинированного стандартного амбулаторного наблюдения пациентов и их активного дистанционного врачебного патронажа на протяжении 12 мес. после ИМ продемонстрировала преимущества в отношении эффективности вторичной профилактики сердечно-сосудистых событий и модификации факторов кардиоваскулярного риска.
Ключевые слова
Для цитирования:
Седых Д.Ю., Алхимова Т.С., Кашталап В.В., Барбараш О.Л. Активный дистанционный врачебный патронаж пациентов, перенесших инфаркт миокарда: есть ли преимущества перед стандартным амбулаторным наблюдением? Рациональная Фармакотерапия в Кардиологии. 2024;20(2):202-211. https://doi.org/10.20996/1819-6446-2024-3011. EDN: XKNPWA
For citation:
Sedykh D.Yu., Alkhimova T.S., Kashtalap V.V., Barbarash O.L. Remote active monitoring of patients after myocardial infarction: are there any advantages over standard outpatient monitoring? Rational Pharmacotherapy in Cardiology. 2024;20(2):202-211. (In Russ.) https://doi.org/10.20996/1819-6446-2024-3011. EDN: XKNPWA
Введение
Пациенты, перенесшие инфаркт миокарда (ИМ), несмотря на выполненную реваскуляризацию инфаркт-связанных коронарных артерий, сохраняют высокий риск повторных ишемических сердечно-сосудистых событий (инсультов и ИМ, смертей от них) в течение длительного времени после острой коронарной катастрофы. Доказано, что максимум реализации таких ишемических рисков приходится на первые 12 мес. и сохраняется в течение как минимум 5 последующих лет после первичной коронарной катастрофы [1]. Эффективному снижению заболеваемости и смертности (как общей, так и сердечно-сосудистой) в постинфарктный период в значительной степени способствуют ранние терапевтические интервенции, направленные на изменение образа жизни, агрессивную модификацию индивидуальных факторов кардиоваскулярного риска, долгосрочное сохранение приверженности лечению основными группами препаратов, улучшающими прогноз ишемической болезни сердца (ИБС) [так называемая болезнь-модифицирующая терапия: дезагреганты, статины, бета-адреноблокаторы, блокаторы ренин-ангиотензин-альдостероновой системы] [2]. В условиях клинической практики эффективность стандартного подхода ко вторичной профилактике после ИМ остается неоптимальной (наблюдение в амбулаторных условиях и диспансерное наблюдение врача-кардиолога, а затем врача-терапевта с консультациями необходимых специалистов по показаниям), что ассоциируется с сохранением высоких показателей заболеваемости и смертности от ИБС. Для оптимизации подходов ко вторичной профилактике после ИМ активно разрабатываются и внедряются доступные и воспроизводимые интервенционные программы [3] оптимизированного воздействия на факторы кардиоваскулярного риска. Подобные программы привлекают к работе квалифицированных специалистов для формирования мультидисциплинарных команд по работе с пациентами для диетологического консультирования, психосоциальной помощи, контролируемых тренировок и для ведения дополнительной информационно-образовательной и мотивационной активности [4]. Такие вмешательства могут осуществляться очно или дистанционно, могут разделяться на этапы, в конечном итоге позволяя инициировать необходимые поведенческие изменения среди большего количества пациентов после ИМ, снижая тяжесть постинфарктных осложнений и оптимизируя качество жизни больных [2][4-8]. Между тем доступность для пациентов интервенционных профилактических программ по модификации сердечно-сосудистого риска остается низкой, составляя не более 36,5% [7]. В самое ближайшее время задачей системы кардиологической реабилитации после ИМ будет формирование инновационных методик постинфарктной реабилитации пациентов с включением программ активной вторичной профилактики, в том числе с использованием цифровых и дистанционных технологий.
Цель исследования — сравнить клиническую эффективность двух программ ведения пациентов в течение 12 мес. после ИМ (стандартное амбулаторное наблюдение или ведение в комбинации с дополнительным активным дистанционным врачебным патронажем).
Материал и методы
Представляемое исследование соответствует стандартам надлежащей клинической практики и принципам Хельсинкской декларации, одобрено локальным этическим комитетом центра (протокол НИИ КПССЗ № 03/1 от 26 марта 2021 г.).
По дизайну исследование интервенционное, когортное, одноцентровое. Включение участников выполнено в период с марта по сентябрь 2021 г. из пациентов, находящихся на лечении в стационаре Кузбасского кардиологического диспансера имени академика Л. С. Барбараша по поводу ИМ, не являющегося перипроцедуральным осложнением согласно IV универсальному определению. Исходное установление диагноза ИМ в текущую госпитализацию проводилось на основании выявления повреждения миокарда в сочетании с клиническими доказательствами ишемии миокарда. Оценивалось нарастание и/или снижение уровня сердечного тропонина (при условии, что хотя бы одно значение было больше 99 перцентиля от верхней границы нормы) и наличие одного и более из следующих признаков: 1) симптомы ишемии миокарда; 2) вновь возникшие ишемических изменения на электрокардиограмме; 3) появление патологического зубца Q; 4) выявление по данным визуализирующих методик новых участков нежизнеспособного миокарда, либо новых участков нарушения локальной сократимости предположительно ишемической этиологии; 4) при ИМ 1 типа выявление тромба в коронарных артериях при коронароангиографии; при ИМ 2 типа — подтверждение наличия несоответствия между потребностью в кислороде и его доставкой.
Все вошедшие участники соответствовали следующим критериям: 1) возрастной диапазон от 35 до 70 лет; 2) постоянное проживание на территории города Кемерово или Кемеровского муниципального округа с удаленностью обособленного сельского поселения от города не менее 50 км и численностью не ниже 5000 человек, без планируемого переезда из домохозяйства в течение ближайших 5 лет; 3) индексный ИМ без летального исхода за период госпитализации; 4) "ожидаемая" продолжительность жизни пациента превышает 1 год за счет отсутствия тяжелой сопутствующей патологии (онкологических, ревматических, эндокринных заболеваний, исключая сахарный диабет; тяжелых заболеваний органов пищеварения и болезней крови; тяжелой хронической обструктивной болезни легких; сердечной недостаточности IV функционального класса; декомпенсированной патологии клапанного аппарата и сосудов; хронического алкоголизма и наркомании; синдрома длительной неподвижности); 5) подписано информированное добровольное согласие установленной формы. Всего по исходным критериям были отобраны 170 пациентов с ИМ, из которых для дальнейшего анализа до проведения рандомизации на группы были исключены 20 (11,8%) по причине обозначенных объективных сложностей с дальнейшей регулярной телефонной коммуникацией, а также в виду отсутствия постоянного доступа к мессенджеру Telegram через мобильное приложение или персональный компьютер. Таким образом, представляемые в статье результаты исследования основаны на данных 150 пациентов с ИМ.
К моменту выписки из стационара с использованием первичной медицинской документации (история болезни, выписной эпикриз) и личного опроса больных был проведен сбор основных социально-демографических показателей пациентов и их анамнеза, клинических характеристик ИМ (результаты лабораторных и инструментальных обследований), особенностей ведения (госпитальное лечение, рекомендации на амбулаторный этап).
Далее была проведена рандомизация пациентов исследования методом конвертов в группы с различной программой дальнейшего наблюдения в течение 12 мес. после ИМ (группа стандартного амбулаторного наблюдения (n=75) или группа стандартного амбулаторного наблюдения с дополнительным дистанционным активным врачебным патронажем (n=75)). Активный дистанционный врачебный патронаж подразумевал осуществление телефонных обзвонов пациентов (не реже 1 раза в месяц) и их ознакомление с информационными материалами по вторичной профилактике. Кроме того, в рамках авторской программы для осуществления таргетного информирования пациентов о факторах сердечно-сосудистого риска и методах их эффективной коррекции, а также для оптимизации приверженности пациентов к назначенной терапии был создан оригинальный информационно-профилактический Telegram-канал "Время сердцу", в который были приглашены все пациенты из группы активного ведения. Рассылка памяток посредством Telegram канала осуществлялась не менее 2-3 раз в неделю, включенные пациенты с ИМ имели возможность задать врачам любые интересующие их вопросы, касающиеся постинфарктного восстановления. Пациентам группы активного патронажа в каждой рассылке акцентировалась необходимость активного посещения кардиолога для совместного планирования программы вторичной профилактики.
Через год после ИМ на очном визите или при телефонном разговоре оценивались витальный статус пациента; частота экстренных сердечно-сосудистых госпитализаций, обусловленных коронарной недостаточностью; фактическая приверженность к терапии и амбулаторному наблюдению; достижение целевых параметров сердечно-сосудистого здоровья; динамика поведенческих факторов риска. В динамике через год, учитывая зарегистрированные случаи смерти, отклик наблюдающихся оставался высоким: 92% пациентов с ИМ из группы стандартного амбулаторного ведения, 97,3% — из группы его сочетания с дополнительным дистанционным активным врачебным патронажем.
Детальная исходная характеристика пациентов из исследования представлена в табл. 1. Следует отметить, что пациенты обеих групп не имели значимых различий по параметрам электрокардиограммы, эхокардиографии и лабораторным показателям. Всем пациентам при поступлении с ИМ была проведена коронароангиография, в 132 (88%) случаях закончившаяся выполнением чрескожного коронарного вмешательства со стентированием. В 123 (82%) случаях пациентам с ИМ был имплантирован стент с лекарственным покрытием. Реваскуляризация коронарного бассейна была полной у 81 (54%) пациента с ИМ, дальнейшая реваскуляризация была показана и технически возможна у 17 (11,3%). Медикаментозное лечение в стационаре осуществлялось согласно действующим клиническим рекомендациям. По ангиографическим характеристикам, выбранной стратегии хирургии, назначенной терапии при выписке с ИМ и частоте направления на 2 этап реабилитации в санаторий группы наблюдения были сопоставимы. Все пациенты в выписном эпикризе получили рекомендации по необходимости соблюдения психологического покоя, увеличению физической активности, особенностям питания после ИМ, были проинформированы о предстоящем амбулаторном наблюдении и возможности получения лекарственных средств по льготе.
Таблица 1. Характеристика пациентов с ИМ
|
Показатель |
Группы пациентов с ИМ |
р |
|
|
Стандартное амбулаторное наблюдение (n=75) |
Стандартное амбулаторное наблюдение и дистанционный врачебный патронаж (n=75) |
||
|
Социально-демографические характеристики |
|||
|
Возраст, лет |
60 (52; 66) |
58 (48; 64) |
0,162 |
|
Место жительства (село/ город), n (%) |
25 (33,3)/50 (66,7) |
18 (24,0)/57 (76,0) |
0,206 |
|
Пол (мужской/ женский), n (%) |
50 (66,7)/25 (33,3) |
53 (70,7)/22 (29,3) |
0,597 |
|
Анамнез до ИМ |
|||
|
Артериальная гипертензия, n (%) |
62 (82,7) |
67 (89,3) |
0,239 |
|
Предшествующая стенокардия, n (%) |
27 (36,0) |
20 (26,7) |
0,218 |
|
Постинфарктный кардиосклероз, n (%) |
14 (18,7) |
11 (14,7) |
0,511 |
|
Хроническая сердечная недостаточность, n (%) |
28 (37,3) |
23 (30,7) |
0,389 |
|
Инсульт и/или транзиторная ишемическая атака, n (%) |
5 (6,7) |
4 (5,3) |
0,730 |
|
Церебральный и/или периферический атеросклероз, n (%) |
17 (22,7) |
13 (17,3) |
0,414 |
|
Дислипидемия, n (%) |
41 (54,7) |
42 (56,0) |
0,869 |
|
Сахарный диабет, n (%) |
16 (21,3) |
19 (25,3) |
0,562 |
|
Ожирение, n (%) |
10 (13,3) |
11 (14,7) |
0,762 |
|
Хроническая болезнь почек, n (%) |
17 (22,7) |
11 (14,7) |
0,194 |
|
Хронические заболевания легких, n (%) |
4 (5,3) |
1 (1,3) |
0,172 |
|
Курение в настоящее время, n (%) |
32 (42,7) |
35 (46,7) |
0,622 |
|
Употребление алкоголя в настоящее время, n (%) |
45 (60,0) |
53 (70,7) |
0,170 |
|
Низкая физическая активность (ниже 2-3 занятий по 45 мин/нед), n (%) |
41 (54,7) |
36 (48,0) |
0,414 |
|
Стресс дома и/или на работе (1-2 периода в течение месяца), n (%) |
28 (37,3) |
20 (26,7) |
0,161 |
|
Клинические характеристики ИМ |
|||
|
ИМ (с подъемом ST/без подъема ST), n (%) |
53 (70,7)/22 (29,3) |
52 (69,3)/23 (30,7) |
0,858 |
|
ИМ, осложненный острой сердечной недостаточностью по Killip II-IV, n (%) |
3 (4,0) |
6 (8,0) |
0,302 |
|
ИМ рецидивирующее течение, n (%) |
5 (6,7) |
4 (5,3) |
0,730 |
|
ИМ, осложненный ранней постинфарктной стенокардией, n (%) |
6 (8,0) |
3 (4,0) |
0,302 |
|
ИМ, осложненный инсультом, n (%) |
1 (1,3) |
0 |
0,315 |
|
Направлен на 2 стационарный этап реабилитации, n (%) |
22 (29,3) |
28 (37,3) |
0,298 |
ИМ — инфаркт миокарда
Статистическая обработка результатов исследования выполнялась с помощью программы Statistica 10.0 (IBM, США). Для оценки и анализа полученных результатов применялся стандартный протокол описательной статистики. Проверка гипотезы о нормальности распределения количественных данных проводилась с помощью критерия Колмогорова-Смирнова. При отличном от нормального распределении количественные показатели были отражены в виде медианы (Ме) с указанием нижней 25% и верхней 75% квартилей (LQ; UQ), при нормальном — в виде средних значений (М) и стандартного отклонения (SD). Качественные переменные представлены в виде абсолютных значений (n) с выражением частоты встречаемости признака в %. Для сравнения двух независимых групп по количественному признаку использовался U-критерий Манна-Уитни, качественные признаки сравнивались с помощью построения таблиц сопряженности с применением критерия Хи² Пирсона. Различия показателей считались значимыми при уровне р<0,05.
Результаты
Через год после ИМ случаи смерти были зарегистрированы в группе стандартного амбулаторного наблюдения у 6 (8,0%) пациентов (все сердечно-сосудистого генеза), тогда как в группе комбинации стандартного амбулаторного наблюдения и дистанционного врачебного патронажа — у 2 (2,7%) (1 сердечно-сосудистая причина и 1 злокачественное новообразование) (p=0,053) (табл. 2).
Таблица 2. Достижение пациентами целевых параметров
сердечно-сосудистого благополучия и поведенческих изменений
в течение 12 мес. после ИМ
|
Показатель |
Группы пациентов с ИМ |
р |
|
|
Стандартное амбулаторное наблюдение (n=69) |
Стандартное амбулаторное наблюдение и дистанционный врачебный патронаж (n=73) |
||
|
Среднее систолическое артериальное давление в мм рт.ст., M±SD |
121,0±15,9 |
116,9±9,2 |
0,081 |
|
Среднее диастолическое артериальное давление в мм рт.ст., M±SD |
71,3±9,1 |
69,7±7,8 |
0,304 |
|
Достигли артериального давления <130/80 мм рт.ст., n (%)* |
48 из 56 (85,7) |
63 из 66 (95,5) |
0,061 |
|
Среднее ЧСС в покое в ударах/мин, M±SD |
65,9±10,6 |
63,2±10,4 |
0,223 |
|
Достигли ЧСС покоя 55-60/мин, n (%)* |
19 из 35 (54,3) |
49 из 70 (70,0) |
0,112 |
|
ХС ЛНП в ммоль/л, M±SD |
2,1±1,2 |
1,7±0,8 |
0,152 |
|
Достигли ХС ЛНП <1,4 ммоль/л, n (%)* |
17 из 37 (45,9) |
20 из 42 (47,6) |
0,881 |
|
Средний индекс массы тела в кг/м², M±SD |
32,1±4,6 |
31,4±4,1 |
0,734 |
|
Достигли снижения индекса массы тела <30,0 кг/м², n (%)* |
3 из 8 (37,5) |
5 из 11 (45,5) |
0,729 |
|
Достигли увеличения физической активности до 2-3 занятий по 45 минут в неделю и выше, n (%)* |
19 из 38 (50,0) |
28 из 36 (77,8) |
0,013 |
|
Уменьшили количество периодов ежемесячного стресса на работе и/или дома или полностью их нивелировали, n (%)* |
15 из 26 (57,7) |
17 из 19 (89,5) |
0,020 |
|
Полностью отказались от курения, n (%)* |
2 из 27 (7,4) |
9 из 35 (25,7) |
0,061 |
|
Снизили частоту употребления алкоголя в течение месяца и/или уменьшили количество порций до 1 стандартной дозы (40 мл крепких спиртных напитков, 120 мл вина, 330 мл пива), n (%)* |
18 из 41 (43,9) |
41 из 52 (78,8) |
0,001 |
* — все % рассчитаны от числа пациентов, исходно имевших фактор риска (избыточную массу тела или ожирение, гиподинамию, стресс на работе и/или дома, курение, употребление алкоголя) или отличный от целевого показатель (артериального давления, ЛНП, ЧСС в покое).
ИМ — инфаркт миокарда, ХС ЛНП — холестерин липопротеинов низкой плотности, ЧСС — частота сердечных сокращений, р — достоверность различий, M — среднее значение количественного признака, SD — стандартное отклонение количественного признака, n — абсолютное значение качественного признака.
Частота развившихся за период наблюдения комбинированных ишемических конечных точек (сердечно-сосудистой смертности + экстренных госпитализаций по ишемической причине) в группе с сочетанием стандартного амбулаторного и дистанционного врачебного наблюдения была в 4,8 раз реже относительно группы стандартного ведения [ 5 (6,7%) и 24 (32,0%); р<0,001]. Между группами выявлены различия по частоте экстренных сердечно-сосудистых госпитализаций в течение 12 мес. после ИМ: так пациенты в группе дополнительной интервенции в постинфарктном периоде, по сравнению с группой стандартного наблюдения группы в 4,7 раз реже поступали в стационар по поводу ишемических событий [ 4 (5,3%) и 19 (25,3%); р<0,001] (рис. 1). Причинами госпитализаций по поводу ишемических событий в группе стандартного амбулаторного наблюдения были повторный ИМ, нестабильная стенокардия, ишемический инсульт и прочие патологии, связанные с атеросклерозом коронарных или церебральных сосудов и их ишемией, тогда как в группе комбинации стандартного наблюдения и дистанционного врачебного патронажа зафиксированы 4 (5,3%) случая развития нестабильной стенокардии.
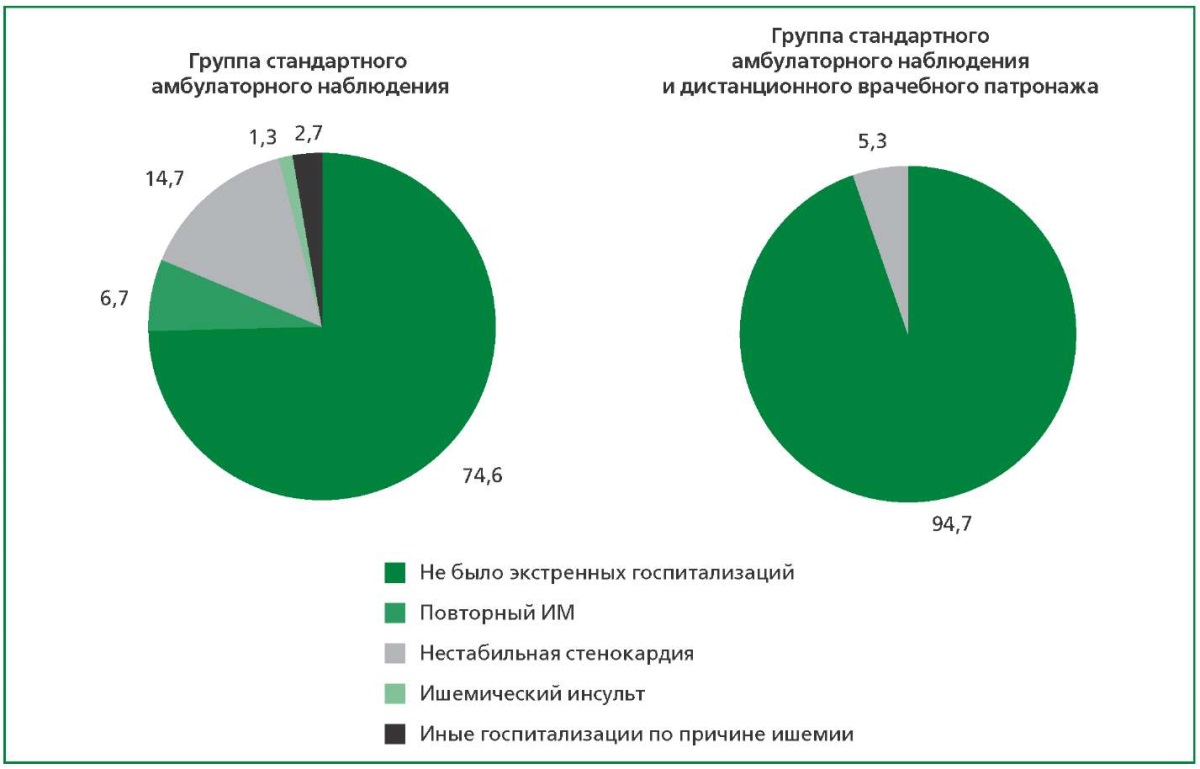
Рисунок 1. Структура госпитализаций по поводу ишемических событий
у пациентов с ИМ в течение года (%)
Все случаи госпитализаций с острым ИМ и нестабильной стенокардией сопровождались проведением новой диагностической коронарографии. Причины повторных ИМ: субокклюзии ранее имевшихся нереваскуляризированных стенозов коронарных артерий (n=3), в том числе гемодинамически значимых стенозов малого диаметра, не связанных с индексным ИМ; острый тромбоз (n=1), гемодинамически значимый рестеноз ранее установленных стентов при индексном ИМ (n=1). Нестабильная стенокардия была вызвана прогрессированием стенозов в ранее нереваскуляризированных коронарных артериях (n=7), в том числе малого диаметра; стойким вазоспастическим компонентом (n=2); гемодинамически незначимым рестенозом в ранее имплантированном стенте (n=2); не сопровождалась значимыми ангиографическими изменениями по сравнению с предшествующими результатами коронароангиографии (n=4).
Фактическая приверженность к приему основных групп препаратов, улучающих прогноз, в группе стандартного амбулаторного наблюдения и в группе его сочетания с дистанционным врачебным патронажем в течение 12 мес. после ИМ была сопоставимой. Дезагреганты принимали 68 (98,6%) и 72 (98,6%) пациентов (р=0,968), бета-адреноблокаторы — 66 (95,7%) и 69 (94,5%) (р=0,756), блокаторы ренин-ангиотензин-альдостероновой системы — 67 (97,1%) и 69 (94,5%) (р=0,445), статины — 66 (95,7%) и 70 (95,9%) (р=0,944), соответственно.
На протяжении года после ИМ пациенты из группы сочетания стандартного амбулаторного наблюдения и дистанционного врачебного патронажа, по сравнению с группой стандартного наблюдения, в 1,7 раз чаще сообщали, что регулярно посещают своего лечащего врача в поликлинике (61 (83,6%) и 33 (47,8%); p<0,001).
В группах пациентов с ИМ через 12 мес. также имелись значимые отличия в отношении достижения целевых параметров сердечно-сосудистого здоровья и поведенческих изменений (табл. 2). Необходимо обратить внимание, что в обеих группах больных было недостаточным достижение целевой частоты сердечных сокращений (ЧСС) покоя, уровня холестерина липопротеинов низкой плотности, снижение индекса массы тела и количества лиц, отказавшихся от курения.
Однако в группе комбинации стандартного амбулаторного наблюдения и дистанционного врачебного патронажа, по сравнению с группой стандартного наблюдения, пациенты по прошествии года в 1,6 раз чаще сообщили об увеличении уровня своей физической активности в течение недели и уменьшении количества периодов ежемесячного стресса или об их полном отсутствии на работе и/или дома; в 1,8 раз чаще указали на снижение частоты ежемесячного употребления алкоголя и уменьшение количества порций.
Через 12 мес. после индексного ИМ независимо от программы наблюдения равнозначны были доли пациентов, употребляющих в пищу диетическую молочную продукцию, рыбу, жареную, жирную пищу и фаст-фуд, готовящих с использованием растительного масла (табл. 3).
Таблица 3. Модификация пациентами питания в течение 12 месяцев после ИМ
|
Показатели |
Группы пациентов с ИМ |
р |
|
|
Стандартное амбулаторное наблюдение (n=69) |
Стандартное амбулаторное наблюдение и дистанционный врачебный патронаж (n=73) |
||
|
Снижение употребления поваренной соли <5 г/сут., n (%) |
54 (78,3) |
68 (93,2) |
0,011 |
|
Употребление диетической молочной продукции, n (%) |
52 (75,4) |
55 (75,3) |
0,998 |
|
Употребление в пищу диетического мяса, n (%) |
49 (71,0) |
66 (90,4) |
0,003 |
|
Употребление в пищу рыбы, n (%) |
49 (71,0) |
59 (80,8) |
0,171 |
|
Употребление свежих и/или приготовленных овощей >300 г/нед., n (%) |
56 (81,2) |
68 (93,2) |
0,032 |
|
Употребление свежих фруктов, ягод >300 г/нед., n (%) |
41 (59,4) |
60 (82,2) |
0,003 |
|
Приготовление пищи с использованием растительного масла, n (%) |
60 (87,0) |
66 (90,4) |
0,515 |
|
Употребление не > ¼ части тарелки сложных углеводов в сутки, n (%) |
45 (65,2) |
59 (80,8) |
0,036 |
|
Употребление жареной, жирной пищи, фаст-фуда, n (%) |
28 (40,6) |
28 (38,4) |
0,786 |
Между тем, пациенты, имевшие комбинацию стандартного амбулаторного наблюдения и дистанционного врачебного патронажа, по сравнению с группой стандартного наблюдения в 1,2 раза чаще указали на снижение суточного употребления поваренной соли, в 1,3 раза чаще на добавление в рацион диетического мяса, в 1,1 раз чаще — свежих и приготовленных овощей (>300 г/нед), в 1,4 раза чаще — свежих фруктов и ягод (>300 г/нед), в 1,2 раза чаще снизивших потребление сложных углеводов до > ¼ части тарелки в сутки.
На рис. 2 представлены различия по частоте присутствия в рационе пациентов отдельных продуктов питания или их компонентов через 12 месяцев после ИМ в группах стандартного наблюдения и его комбинации с дистанционным врачебным патронажем. Показано, что программа комбинации стандартного наблюдения и дистанционного врачебного патронажа обеспечивала более высокую частоту лиц, часто и иногда употребляющих свежие и приготовленные овощи (>300 г в неделю), чем программа стандартного наблюдения (р<0,001).
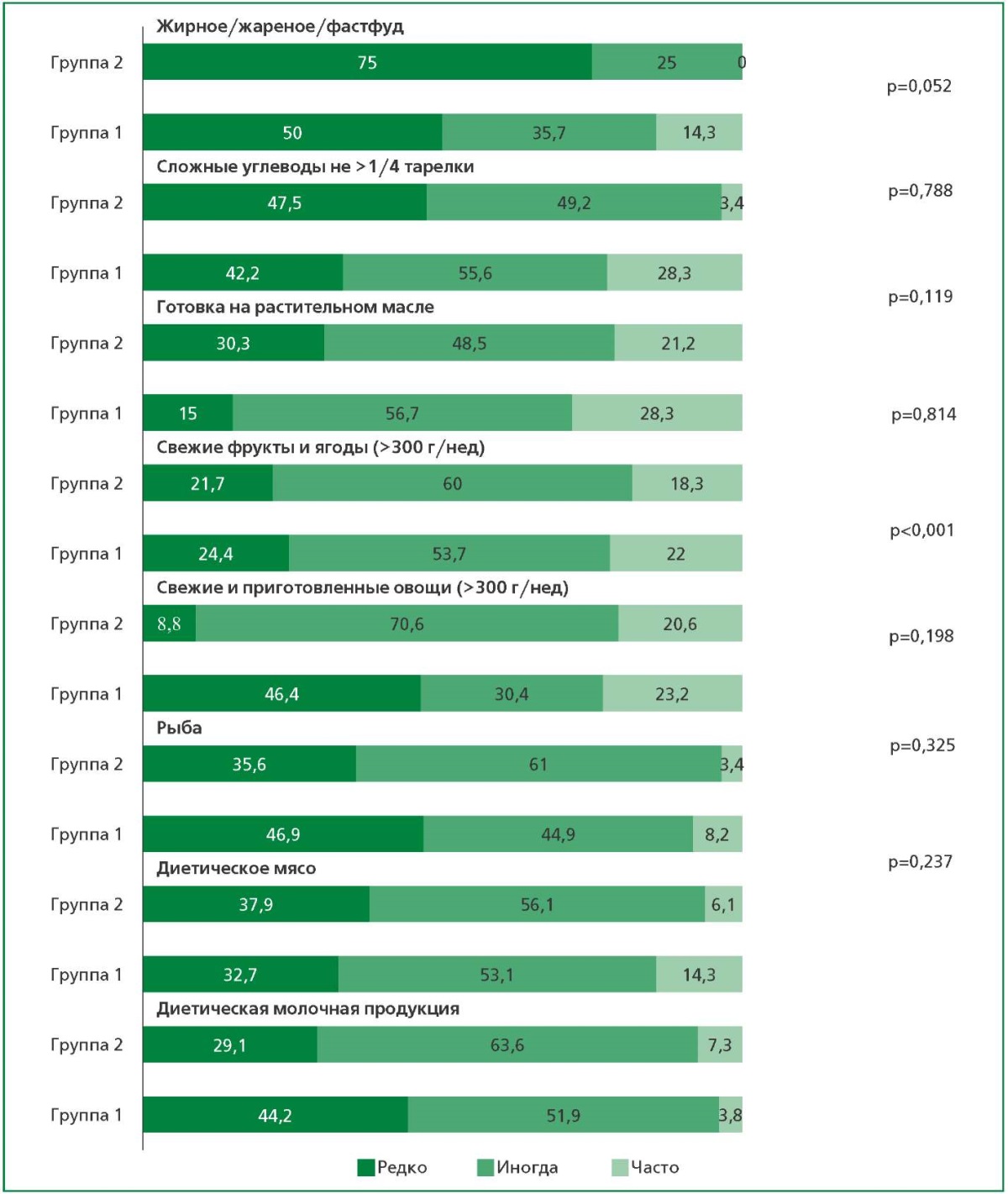
Рисунок 2. Частота присутствия в рационе пациентов отдельных продуктов питания
или их компонентов через 12 мес. после ИМ в группах стандартного наблюдения (группа 1)
и его комбинации с дистанционным врачебным патронажем (группа 2), в %
Таким образом, в ходе настоящего исследования были выявлены преимущества комбинации стандартного амбулаторного наблюдения с дистанционным врачебным патронажем пациентов перед стандартным в качестве опции для проведения профилактической программы и в достижении ее целей в течение года после ИМ.
Обсуждение
В настоящем исследовании продемонстрировано, что в группе пациентов с ИМ, находящихся в течение 12 мес. на комбинации стандартного амбулаторного наблюдения с дистанционным активным врачебным патронажем, по сравнению с группой стандартного наблюдения были зарегистрированы меньшее число комбинированных ишемических событий и меньшая частота экстренных госпитализаций по сердечно-сосудистым причинам. Было показано, что пациенты, наблюдавшиеся по авторской программе, на протяжении года чаще осуществляли регулярное амбулаторное наблюдение. За год пациентами с комбинированным наблюдением значимо чаще были достигнуты поведенческие изменения — увеличение физической активности, минимизация стресса и употребления алкоголя, а также изменения в структуре питания. Пациенты, подвергшиеся дополнительному дистанционному врачебному патронажу, чаще пациентов на стандартном диспансерном учете после ИМ, указывали на уменьшение употребления в течение суток поваренной соли (менее 5 г), а также на снижение порции сложных углеводов до ¼ части тарелки, кроме того большее число пациентов этой группы отметили факт употребления диетического мяса, овощей и фруктов (>300 г/нед.), большая доля пациентов сообщили об увеличении в рационе частоты питания свежими и/или приготовленными овощами. Между тем в обеих группах обращает на себя внимание недостаточный процент достижения целевых показателей качества жизни после ИМ (артериального давления, ЧСС в покое, снижение индекса массы тела, отказов от курения), что следует рассматривать в качестве потенциальных мишеней, требующих дальнейшей лечебно-профилактической работы.
В противовес нашим результатам в рандомизированном контролируемом исследовании Rehabilitation after myocardial infarction trial и метаанализе The Cardiac Rehabilitation Outcome Study, напротив, в эффектах от предложенных программ по кардиореабилитации у пациентов с ИМ не выявлено влияния на смертность, сердечно-сосудистую заболеваемость и модификацию факторов риска [2][9][10], что говорит о гетерогенности влияния различных инструментов интервенции в рамках вторичной профилактики. По данным G. Van Halewijn и соавт., подобные интервенционные вмешательства наиболее показательны с позиций эффективности только тогда, когда включают наибольшее количество компонентов кардиореабилитации в программу [11]. Аналогично нашей работе в одной из рандомизированных проспективных программ, акцентированной на усилении образовательной составляющей при наблюдении после ИМ, также были выявлены положительные прогностические эффекты в виде снижения числа ишемических событий (отношение шансов 0,46, 95% доверительный интервал 0,28-0,74; р=0,002) [12]. Чтобы предсказать клиническую эффективность программ модификации образа жизни активно разрабатываются прогностические инструменты, в частности шкала MANIPAL, связующая выявленный уровень приверженности с изменениями факторов риска и частотой развития последующих неблагоприятных исходов [13].
Доказано, что любая дополнительная информационная интервенция по вопросам профилактики (не менее 15 мин) у пациентов с ИМ улучшает психологический настрой и в 85,7% случаев ассоциируется с дальнейшей реализацией поведенческих изменений (р<0,001) [14]. Согласно действующим клиническим рекомендациям, для пациентов с ИМ участие в обучающих и информационных программах научно обосновано и является необходимым компонентом вторичной профилактики. Между тем, часть таких пациентов исходно остается "потерянной" для программ дополнительного наблюдения, что обусловлено не столько существующими организационно-финансовыми барьерами кардиореабилитации при ИМ, но скорее, результатом внутренней конкуренции терапевтических потребностей пациента и его религиозных, культурных и семейных убеждений [15]. Такие пациенты с ИМ, как правило, даже в ситуации высокой приверженности к лечению, не достигают целевых показателей липидограммы и уровня артериального давления в постинфарктном периоде, что связывают с недостаточной титрацией доз лекарственных препаратов или с отсутствием регулярного амбулаторного диспансерного наблюдения у кардиолога [16][17].
Аналогично эффектам представленной нами авторской программы, программа мобильной кардиореабилитации MCard также положительно повлияла на поведение участников в течение 6 месяцев после острого коронарного события с точки зрения улучшения питания, ограничения поваренной соли, увеличения физической активности [5]. В другой программе наблюдения после ИМ также были показаны преимущества дополнительного консультирования по вопросам образа жизни в виде значимого снижения потребления насыщенных жиров (F=22,48 (где F — вариация между средними значениями выборки к вариация внутри выборок в дисперсионном анализе), p<0,001), соленых/консервированных продуктов (F=13,58, p<0,001), увеличения потребления овощей, фруктов, орехов и цельнозерновых продуктов (F=40,88, p<0,001), повышения уровня липопротеинов высокой плотности (F=8,982, p=0,001) [18]. В исследовании пациентов в провинции Хамадан (Иран) продемонстрировали, что в группе более длительной (8-недельной) очной интервенционной программы наблюдения постинфарктные пациенты не только значимо поменяли рацион своего питания на более здоровый, но и увеличили физические нагрузки (p<0,001) [19]. 15-месячная программа по модификации образа жизни после коронарной реваскуляризации при ИБС, показала не только изменения профиля традиционных факторов риска, но и значимое улучшение психологического статуса больных [20]. В нашей работе также отражен факт минимизации психологического стресса через 12 мес. Формированию и распространению региональных программ вторичной профилактики после ИМ, включающих образовательные аспекты в отношении модификации образа жизни, значимо может способствовать популяризация и финансирование на уровне государства, именно такой положительный опыт представлен в публикациях исследователями из Бразилии [17].
Дополнительные программы модификации факторов риска после ИМ не менее эффективны в случае доминирующей роли патронажа медицинской сестры, а не врача. В одном из исследований при сравнении пациентов стандартного постинфарктного наблюдения у врача и его комбинации с информирующим сестринским вмешательством в течение 12 нед. после выписки после ИМ выявлено значительное улучшение систолического (р=0,001) и диастолического артериального давления (р=0,016), снижение индекса массы тела (р=0,004), а также улучшение качества жизни по всем субшкалам — физическому, эмоциональному и социальному (р<0,001) благополучию именно в группе дополнительного патронажа [21]. Усиление диспансерного наблюдения пациентов после ИМ, не менее эффективным дополнительным наблюдением медицинской сестры, может быть полезно с точки зрения оптимизации производительности труда врача при сопоставимой клинической "выгоде" для пациентов.
Таким образом, дополнение к стандартному наблюдению после ИМ дистанционного врачебного патронажа, является эффективным с позиции достижений целей вторичной профилактики и реабилитации у пациентов.
Ограничения исследования: в качестве ограничений следует отметить сбор части данных в исследовании посредством опроса пациента или его родственников, что может вносить субъективизм в предоставленные ответы.
Заключение
В настоящем исследовании у пациентов после перенесенного ИМ оригинальная программа, комбинирующая стандартное амбулаторное наблюдение и дистанционный активный врачебный патронаж в течение 12 мес., продемонстрировала преимущества в отношении эффективной вторичной профилактики сердечно-сосудистых событий и модификации факторов сердечно-сосудистого риска.
Отношения и Деятельность. Нет.
Relationships and Activities. None.
Финансирование. Исследование проведено при поддержке Научно-исследовательского института комплексных проблем сердечно-сосудистых заболеваний.
Funding. The study was performed with the support of Research Institute for Complex Issues of Cardiovascular Diseases.
Список литературы
1. Барбараш О. Л., Седых Д. Ю., Горбунова Е. В. Основные факторы, определяющие риск развития повторного инфаркта миокарда. Сердце: журнал для практикующих врачей. 2017;16(1):10-50]. DOI:10.18087/rhj.2017.1.2280.
2. Murphy BE, Card PD, Ramirez-Kelly L, et al. Effects of the Strong Hearts program after a major cardiovascular event in patients with cardiovascular disease. J Osteopath Med. 2023;123(6):279-285. DOI:10.1515/jom-2022-0141.
3. Thuthinal AS, Bhade NS, Khirade AJ, et al. Assessment of Prescription Adherence to Secondary Prevention Guideline Recommendations and Patient Adherence to Pharmacotherapy and Lifestyle Modifications in Acute Coronary Syndrome and Chronic Coronary Syndrome Patients. J Assoc Physicians India. 2022;70(12):11-2. DOI:10.5005/japi-11001-0159.
4. Ларина В. Н., Ахматова Ф. Д., Аракелов С. Э., и др. Cовременные стратегии кардиореабилитации после инфаркта миокарда и чрескожного коронарного вмешательства. Кардиология. 2020;60(3):111-8. DOI:10.18087/cardio.2020.3.n546.
5. Manzoor S, Hisam A, Aziz S, et al. Effectiveness of Mobile Health Augmented Cardiac Rehabilitation on Behavioural Outcomes among Post-acute Coronary Syndrome Patients: A Randomised Controlled Trial. J Coll Physicians Surg Pak. 2021;31(10):1148-53. DOI:10.29271/jcpsp.2021.10.1148.
6. Sagar VA, Davies EJ, Briscoe S, et al. Exercise-based rehabilitation for heart failure: systematic review and meta-analysis. Open Heart. 2015;2(1):e000163. DOI:10.1136/openhrt-2014-000163.
7. Kotseva K, Wood D, De Backer G, et al; EUROASPIRE Study Group. EUROASPIRE III: a survey on the lifestyle, risk factors and use of cardioprotective drug therapies in coronary patients from 22 European countries. Eur J Cardiovasc Prev Rehabil. 2009;16(2):121-37. DOI:10.1097/HJR.0b013e3283294b1d.
8. Lavie CJ, Arena R, Franklin BA. Cardiac Rehabilitation and Healthy Life-S tyle Interventions: Rectifying Program Deficiencies to Improve Patient Outcomes. J Am Coll Cardiol. 2016;67(1):13-5. DOI:10.1016/j.jacc.2015.09.103.
9. West RR, Jones DA, Henderson AH. Rehabilitation after myocardial infarction trial (RAMIT): multi-centre randomised controlled trial of comprehensive cardiac rehabilitation in patients following acute myocardial infarction. Heart. 2012;98(8):637-44. DOI:10.1136/heartjnl-2011-300302.
10. Rauch B, Davos CH, Doherty P, et al; ‘Cardiac Rehabilitation Section’, European Association of Preventive Cardiology (EAPC), in cooperation with the Institute of Medical Biometry and Informatics (IMBI), Department of Medical Biometry, University of Heidelberg, and the Cochrane Metabolic and Endocrine Disorders Group, Institute of General Practice, Heinrich-H eine University, Düsseldorf, Germany. The prognostic effect of cardiac rehabilitation in the era of acute revascularisation and statin therapy: A systematic review and meta-analysis of randomized and non-randomized studies — The Cardiac Rehabilitation Outcome Study (CROS). Eur J Prev Cardiol. 2016;23(18):1914-39. DOI:10.1177/2047487316671181.
11. van Halewijn G, Deckers J, Tay HY, et al. Lessons from contemporary trials of cardiovascular prevention and rehabilitation: A systematic review and meta-analysis. Int J Cardiol. 2017;232:294-303. DOI:10.1016/j.ijcard.2016.12.125.
12. Giannopoulos G, Karageorgiou S, Vrachatis D, et al. A stand-a lone structured educational programme after myocardial infarction: a randomised study. Heart. 2021;107(13):1047-53. DOI:10.1136/heartjnl-2020-318414.
13. Devasia T, Shetty PN, Kareem H, et al. Manipal lifestyle modification score to predict major adverse cardiac events in postcoronary angioplasty patients. Indian Heart J. 2018;70 Suppl 3(Suppl 3):S353-S358. DOI:10.1016/j.ihj.2018.10.411.
14. Hisam A, Khan A, Zahid B, et al. Health related quality of life in post-acute coronary patient. J Pak Med Assoc. 2022;72(10):2069-73. DOI:10.47391/JPMA.3461.
15. Dilla D, Ian J, Martin J, et al. "I don’t do it for myself, I do it for them": A grounded theory study of South Asians’ experiences of making lifestyle change after myocardial infarction. J Clin Nurs. 2020;29(19-20):3687-700. DOI:10.1111/jocn.15395.
16. Гарганеева А. А., Кужелева Е. А., Тукиш О. В. Роль приверженности лечению в клиническом течении постинфарктного периода (по данным регистра острого инфаркта миокарда). Комплексные проблемы сердечно-сосудистых заболеваний. 2019;8(4):56-64]. DOI:10.17802/2306-1278-20198-4-56-64.
17. Cедых Д. Ю., Барбараш О. Л. Факторы, влияющие на приверженность к лечению пациентов трудоспособного возраста с инфарктом миокарда. Атеросклероз. 2023;19(2):93-106]. DOI:10.52727/2078-256X-2023-19-2-93-106.
18. Mok VK, Sit JW, Tsang AS, et al. A controlled trial of a nurse follow-up dietary intervention on maintaining a heart-h ealthy dietary pattern among patients after myocardial infarction. J Cardiovasc Nurs. 2013;28(3):256-66. DOI:10.1097/JCN.0b013e31824a37b7.
19. Amini R, Rajabi M, Azami H, Soltanian A. The effect of self-management intervention program on the lifestyle of postmyocardial infarction patients. J Educ Health Promot. 2021;10:145. DOI:10.4103/jehp.jehp_902_20.
20. Arzet A, Sibanda W, Naidoo DP, Somalingum P. The effect of lifestyle modification on depression among myocardial infarction patients after revascularisation. Cardiovasc J Afr. 2021;32(2):70-7. DOI:10.5830/CVJA-2020030.
21. Yadav S, Kalal N, Sharma SK, Deora S. The development and randomised feasibility trial of a Nurse-led lifestyle modification follow-up programme among post-myocardial infarction patients. J Res Nurs. 2023;28(3):230-46. DOI:10.1177/17449871231163983.
Об авторах
Д. Ю. СедыхРоссия
Седых Дарья Юрьевна
Кемерово
Т. С. Алхимова
Россия
Алхимова Татьяна Сергеевна
Кемерово
В. В. Кашталап
Россия
Кашталап Василий Васильевич
Кемерово
О. Л. Барбараш
Россия
Барбараш Ольга Леонидовна
Кемерово
Дополнительные файлы
Рецензия
Для цитирования:
Седых Д.Ю., Алхимова Т.С., Кашталап В.В., Барбараш О.Л. Активный дистанционный врачебный патронаж пациентов, перенесших инфаркт миокарда: есть ли преимущества перед стандартным амбулаторным наблюдением? Рациональная Фармакотерапия в Кардиологии. 2024;20(2):202-211. https://doi.org/10.20996/1819-6446-2024-3011. EDN: XKNPWA
For citation:
Sedykh D.Yu., Alkhimova T.S., Kashtalap V.V., Barbarash O.L. Remote active monitoring of patients after myocardial infarction: are there any advantages over standard outpatient monitoring? Rational Pharmacotherapy in Cardiology. 2024;20(2):202-211. (In Russ.) https://doi.org/10.20996/1819-6446-2024-3011. EDN: XKNPWA

















































