Перейти к:
Какие данные клинического и лабораторно-инструментального обследования ассоциированы с развитием феномена невосстановленного коронарного кровотока у пациентов с острым коронарным синдромом?
https://doi.org/10.20996/1819-6446-2025-3190
EDN: ZRIATV
Аннотация
Цель. Изучить клинические и лабораторно-инструментальные факторы, ассоциированные с развитием феномена невосстановленного коронарного кровотока, у пациентов с инфарктом миокарда в работе кардиологической службы скоропомощного стационара.
Материал и методы. Для проведения исследования была сформирована база данных 2090 пациентов с диагнозом «Острый коронарный синдром», последовательно госпитализированных в региональный сосудистый центр. После проведения чрескожного коронарного вмешательства и оценки коронарного кровотока по шкале TIMI, у 59 пациентов отмечался феномен невосстановленного коронарного кровотока, эти пациенты составили 1-ю группу. 2-я группа (n=149) была сформирована случайным образом из оставшихся 2031 пациентов с финальным коронарным кровотоком TIMI 3. Между группами проводилось сравнение клинико-демографических, лабораторных и инструментальных данных; факторов, влияющих на развитие феномена «no-slow-reflow». Статистическую обработку данных выполняли в программе STATISTICA, с использованием методов параметрического и непараметрического анализа.
Результаты. В 1-й группе пациентов сахарный диабет встречался с частотой 42,4%, во 2-й — 22,8%, p=0,003. По данным лабораторных исследований у пациентов 1-й и 2-й групп средний уровень лейкоцитов крови составил 10,9×109/л и 9,5×109/л, соответственно, p=0,0015; абсолютное содержание нейтрофилов 8,4×109/л и 6,6×109/л, p=0,0003. В 1-й и 2-й группах пациентов фракция выброса (ФВ) левого желудочка (ЛЖ) составила в среднем 42% и 45% соответственно, p=0,0015. В 1-й группе выявлялись изменения по передней стенке ЛЖ на электрокардиограмме в 59% случаев, во 2-й — в 50%, p=0,018. Проксимальное поражение инфаркт-связанной артерии в 1-й группе наблюдалось в 88%, во 2-й — в 40%, p<0,0001. По данным бинарной логистической регрессии независимыми факторами риска развития феномена «no-/slow-reflow» являются: уровень поражения инфаркт-связанной артерии [OR=3,33; 95% CI: 1,67-6,57; p<0,001], ФВ ЛЖ [OR=1,1; 95% CI: 1,04-1,17; p<0,001], время от начала болевого синдрома до реваскуляризации [OR=1,03; 95% CI: 0,95-0,996; p=0,02].
Заключение. Длительное общее время ишемии миокарда, наличие сахарного диабета, более низкая ФВ ЛЖ, повышенное содержание лейкоцитов и нейтрофилов крови, передняя локализация инфаркта миокарда, более проксимальный уровень окклюзии коронарной артерии, ассоциированы с развитием «no-/slow-reflow» у пациентов с инфарктом миокарда в реальной клинической практике.
Ключевые слова
Для цитирования:
Константинова Е.В., Ильин Ю.С., Великоцкий А.А., Черников А.О., Жданова М.С., Площенков Е.В. Какие данные клинического и лабораторно-инструментального обследования ассоциированы с развитием феномена невосстановленного коронарного кровотока у пациентов с острым коронарным синдромом? Рациональная Фармакотерапия в Кардиологии. 2025;21(3):200-208. https://doi.org/10.20996/1819-6446-2025-3190. EDN: ZRIATV
For citation:
Konstantinova E.V., Ilin Yu.S., Velikotskiy A.A., Chernikov A.O., Zhdanova M.S., Ploshchenkov E.V. Which сlinical, laboratory, and instrumental factors are associated with the development of the no-reflow phenomenon in patients with acute coronary syndrome? Rational Pharmacotherapy in Cardiology. 2025;21(3):200-208. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3190. EDN: ZRIATV
Введение
Проведение чрескожного коронарного вмешательства (ЧКВ) у пациентов с инфарктом миокарда (ИМ) в большинстве случаев необходимо, эффективно, безопасно, и все более широко применяется в реальной клинической практике [1]. Однако в ряде случаев ЧКВ сопряжено с возможным развитием осложнений, одним из которых является феномен невосстановленного/замедленного коронарного кровотока («no-/slow-reflow») [2]. Этот феномен может встречаться от 2 до 50% всех случаев ИМ с подъёмом сегмента ST электрокардиограммы (ЭКГ) [3-7]. Разброс данных, вероятно, обусловлен отсутствием общепризнанного эффективного метода диагностики. Предлагались разнообразные диагностические методы: динамика изменений ЭКГ, контрастная эхокардиография (ЭхоКГ), контрастная магнитно-резонансная томография (МРТ), данные коронароангиографии (КАГ). Динамика изменений сегмента SТ на ЭКГ может коррелировать с восстановлением кровотока в инфаркт-связанной артерии (ИСА) но обладает низкой чувствительностью [8]. Контрастная ЭхоКГ позволяет диагностировать нарушения перфузии миокарда на уровне микроциркуляторного русла существенно более точно [9]. Ограничением метода могут быть возможности аппарата, оператора и доступность контраста.
МРТ сердца с контрастированием является наиболее чувствительным методом для выявления феномена «no-/slow-reflow» [10]. Однако проведение метода в подавляющем большинстве случаев невозможно сразу после ЧКВ у пациента с ИМ.
В литературе можно встретить несколько названий и несколько определений феномена невосстановленного/замедленного коронарного кровотока. В контексте проведенной работы имеется в виду то определение, которое соответствует термину «феномен no-reflow» и подразумевает ангиографическую оценку [11]. В повседневной работе ЧКВ-центра феномен невосстановленного коронарного кровотока устанавливается на основании кровотока по шкале ТIMI (Thrombolysis In Myocardial Infarction) при проведении контрольной КАГ [12].
Несмотря на длительное изучение феномена невосстановленного коронарного кровотока, значительный объём литературных данных, по-прежнему требуют уточнения вопросы, связанные с механизмами его развития, распространенностью, факторами, ассоциированными с его возникновением. Таким образом, цель исследования — изучить клинические и лабораторно-инструментальные факторы, ассоциированные с развитием феномена невосстановленного коронарного кровотока, у пациентов с ИМ в работе кардиологической службы скоропомощного стационара.
Материал и методы
В исследование было включено 2090 пациентов с диагнозом «Острый коронарный синдром» (ОКС), последовательно госпитализированных в ГКБ №1 им. Н. И. Пирогова г. Москвы в период с 1 января 2017 по 1 ноября 2022 гг. по каналу скорой медицинской помощи или обратившихся самостоятельно. Критерии исключения: проведенная тромболитическая терапия, отказ от КАГ или ЧКВ, отсутствие обструктивного поражения коронарных артерий, многососудистое поражение коронарных артерий, требующее операции коронарного шунтирования, агональное состояние больного.
У всех пациентов анализировали демографические, анамнестические, клинические, лабораторные, инструментальные, прицельно — ангиографические показатели. Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI. При КАГ оценивали стандартные показатели, включая тип коронарного кровоснабжения миокарда, локализацию и уровень поражения ИСА. При выполнении КАГ у всех больных была проанализирована степень коронарного кровотока в ИСА по шкале TIMI как до, так и после ЧКВ. ИСА идентифицировалась на основании совокупности данных, включая: ЭКГ критерии топической локализации ишемических изменений, оценку коронарного кровотока по шкале TIMI от 0 до 3, ангиографические признаки осложнённой атеросклеротической бляшки, а именно, наличие пристеночных тромбов, подрытых краёв и нестабильной морфологии поражения.
Феномен «no-reflow» определялся как отсутствие антероградного поступления контрастного вещества или минимальный кровоток дистальнее места окклюзии и имплантации стента (TIMI 0 и TIMI 1, соответственно). Феномен «slow-reflow» определялся как степень кровотока TIMI 2 по данной шкале. Все пациенты были разделены на 2 группы: с невосстановленным/замедленным кровотоком (TIMI 0-2) (59 пациентов — они составили 1-ю группу) и с нормальным кровотоком (TIMI 3) (2031 пациент).
Из 2031 пациента (с финальным антероградным кровотоком TIMI 3 и отсутствием значимых различий в характере поражения коронарного русла, в сравнении с 1-й группой пациентов с невосстановленным кровотоком), случайным образом было отобрано 149 пациентов, составивших 2-ю группу [13].
Все больные перед ЧКВ получали перорально нагрузочные дозы ацетилсалициловой кислоты (150-325 мг) и тикагрелора (180 мг). При проведении ЧКВ интракоронарно болюсно вводился нефракционированный гепарин в дозе 7500-12500 МЕ в зависимости от массы тела. При диагностировании оператором ангиографического феномена «no-/slow-reflow» внутривенно болюсно вводился эптифибатид (180 мкг/кг), далее внутривенно через дозатор.
Статистическую обработку данных выполняли в программе Statistica 10 (StatSoft Inc, США), с использованием методов параметрического и непараметрического анализа. Все количественные данные проверяли на предмет нормальности распределения. В случае нормального распределения количественные данные представляли в виде среднего и стандартного отклонения (М±SD). Ненормально распределенные количественные величины описывали при помощи медианы (Me) с указанием нижнего и верхнего квартилей (Q1; Q3). Для номинальных данных указывали абсолютные и относительные значения. При сравнительном статистическом анализе для средних величин в нормально распределенных совокупностях количественных данных рассчитывали t-критерий Стьюдента для независимых выборок, в случае ассиметричного распределения данных использовали U-критерий Манна–Уитни. Для оценки всех статистически значимых количественных величин был проведён ROC-анализ с расчетом площади под кривой (AUC) и 95% доверительного интервала (ДИ), и построены характеристические кривые. Для сравнения номинальных данных в изучаемых группах использовался критерий χ2 Пирсона. В случае анализа четырехпольных таблиц при ожидаемом явлении хотя бы в одной ячейке менее 10, нами рассчитывался критерий χ2 с поправкой на непрерывность по Йейтсу (Yates’s correction), или использовался точный критерий Фишера при значении менее 5. В качестве количественной меры эффекта при сравнении относительных показателей нами использовался показатель отношения шансов (ОШ). Определение предикторов развития феномена «no-/slow-reflow» осуществляли с помощью метода пошаговой бинарной логистической регрессии. В модель были включены все показатели, которые имели статистические значимые различия при межгрупповом сравнении. Различия считали статистически значимыми при p<0,05.
Результаты
Клинико-демографические характеристики всех пациентов, вошедших в окончательный анализ и составивших 1-ю и 2-ю группу представлены в табл. 1.
Выделенные для анализа 1-я и 2-я группы пациентов значимо не различались по возрасту (66±12 лет и 64±11,5 лет, p=0,398), полу (59% мужчин и 70,5% мужчин, p=0,122), индексу массы тела (27,3 кг/м2 vs 27,6 кг/м2, p=0,842), курению (42,6% и 48,6%, p=0,486), наличию хронической болезни почек C3a-C5 (45,8% и 28,9%, p=0,229), гипертонической болезни (89,7% и 92%, p=0,599), ИМ в анамнезе (12,1% и 17,45%, p=0,342), фибрилляция предсердий (8,6% и 9,4%, p=0,862), ЧКВ в анамнезе (8,6% vs 11,4%, p=0,559).
При этом, статистически значимые различия наблюдались по частоте сахарного диабета (СД) (рис. 2). В 1-й группе пациентов СД встречался с частотой 42,4%, во 2-й — с частотой 22,8%, p=0,003. При этом СД встречается в 2,6 раза чаще в группе с невосстановленным/замедленным кровотоком, чем в группе без феномена «no-/slow-reflow» [OШ 2,642±0,331; 95% ДИ: 1,382-5,052; p<0,05].
Пациенты 1-й и 2-й групп значимо различались по содержанию лейкоцитов в крови (10,9×109/л vs 9,5×109/л, p=0,0015), по абсолютному содержанию нейтрофилов (8,4×109/л vs 6,6×109/л в 1 и 2 группе, соответственно, p=0,0003), по относительному содержанию нейтрофилов/лейкоцитам (77,5% vs 70,8% в 1 и 2 группе, соответственно, p=0,01) (табл. 2) Другие проанализированные лабораторные показатели среди пациентов 1-й и 2-й групп значимо не различались и составили, соответственно: гематокрит (43,4% vs 41,9%, p=0,087), креатинин при поступлении (98,9 мкмоль/л vs 91,2 мкмоль/л, p=0,216), мочевина (6,2 ммоль/л vs 5,9 ммоль/л в 1 и 2 группе, соответственно, p=0,119), СКФ (63 мл/мин/1,73 м2 vs 70,4 мл/мин/1,73 м2 в 1-й и 2-й группе, p=0,09), общий холестерин (5,02±1,3 ммоль/л vs 5,07±1,39 ммоль/л, p=0,819), холестерин липопротеидов низкой плотности (2,92±1,18 ммоль/л vs 3,18±1,3 ммоль/л, p=0,266), глюкоза (8,3 ммоль/л vs 8,1 ммоль/л, p=0,278).
По данным ЭКГ при поступлении в стационар элевация сегмента ST относительно изолинии была зарегистрирована в 83,1% случаев (у 49 человек) в 1-й группе пациентов и у 73,2% (у 109 человек) во 2-й группе (p=0,132). Изменения передней стенки левого желудочка (ЛЖ) по данным ЭКГ наблюдались в 59% (у 35 человек) в 1-й группе и 50% случаев — во 2-й (p=0,018).
Фракция выброса (ФВ) ЛЖ по данным ЭхоКГ, выполненной в 1-е сутки госпитализации, в среднем составила в 1-й группе пациентов 42%, во 2-й — 45%, p=0,0015.
По данным КАГ уровень поражения ИСА в 1-й группе в 88% случаев был проксимальный (у 52 пациентов), во 2-й группе — в 40% (у 59 пациентов (p<0,0001). ИСА была окклюзирована в среднем сегменте в 10% случаев в 1-й группе и 52% случаев во 2-й (p<0,0001).
При анализе времени от момента начала заболевания до открытия ИСА оказалось, что время «боль-баллон» составило 7,0 (3,0; 16,0) ч в 1-й группе и 4,0 (2,3; 8,3) ч во 2-й группе, p=0,004. Пациентам 1-й группы реваскуляризация в целом выполнялась на 3 ч позже, чем у пациентов 2-й группы.
Построение характеристических кривых подтвердило зависимость возникновения феномена невосстановленного/замедленного кровотока от содержания лейкоцитов и нейтрофилов в крови больных с ИМ при поступлении, а также от времени от начала боли до реваскуляризации, ассоциацию с величиной ФВ ЛЖ. Все ROC-кривые вышеперечисленных параметров не пресекали линию нулевой прогностической значимости и их площадь под кривой (AUC) оказалась достаточно велика.
При помощи бинарной логистической регрессии было определено, что основными независимыми факторами риска развития феномена «no-/slow-reflow» являются: уровень поражения ИСА [OШ 3,33; 95% ДИ: 1,67-6,57; p<0,001], исходный кровоток по TIMI [OШ 1,83; 95% ДИ: 1,24-2,72; p=0,003], ФВ ЛЖ [OШ 1,1; 95% ДИ: 1,04-1,17; p<0,001], время от начала болевого синдрома до реваскуляризации [OШ 1,03; 95% ДИ: 0,95-0,996; p=0,02].
Таблица 1. Клинико-демографические характеристики пациентов, включённых в исследование
Параметр | 1-я группа (n=59) | 2-я группа (n=149) | p |
Возраст, лет (M±SD) | 66±12 | 64±11,5 | 0,398 |
Пол: муж./жен., n (%) | 35 (59,3)/24 (40,7) | 105 (70,5)/44 (29,5) | 0,122 |
ИМТ, кг/м² (Me [Q1; Q3]) | 27,3 [ 25; 32] | 27,6 [ 24,8; 31,5] | 0,842 |
Курение, n (%) | 20 (42,6) | 53 (48,6) | 0,486 |
Пациенты с ГБ, n (%) | 52 (89,7) | 137 (92) | 0,599 |
ХБП C3a-C5, n (%) | 27 (45,8) | 43 (28,9) | 0,229 |
Сахарный диабет, n (%) | 25 (42,4) | 34 (22,8) | 0,003 |
Фибрилляция предсердий, n (%) | 5 (8,6) | 14 (9,4) | 0,862 |
Пациенты с ИМ в анамнезе, n (%) | 7 (12,1) | 26 (17,45) | 0,342 |
Пациенты с ЧКВ в анамнезе, n (%) | 5 (8,6) | 17 (11,4) | 0,559 |
Данные представлены в виде M±SD или Me [Q1; Q3], если не указано иное ИМТ — индекс массы тела, ГБ — гипертоническая болезнь, ХПБ – хроническая болезнь почек, С1 — скорость клубочковой фильтрации (СКФ) ≥90 мл/мин, С2 — СКФ 60-89 мл/мин, С3а — СКФ 45-59 мл/мин, С3b — СКФ 30-44 мл/мин, С4 — СКФ 15-29 мл/мин, С5 — СКФ <15 мл/мин | |||
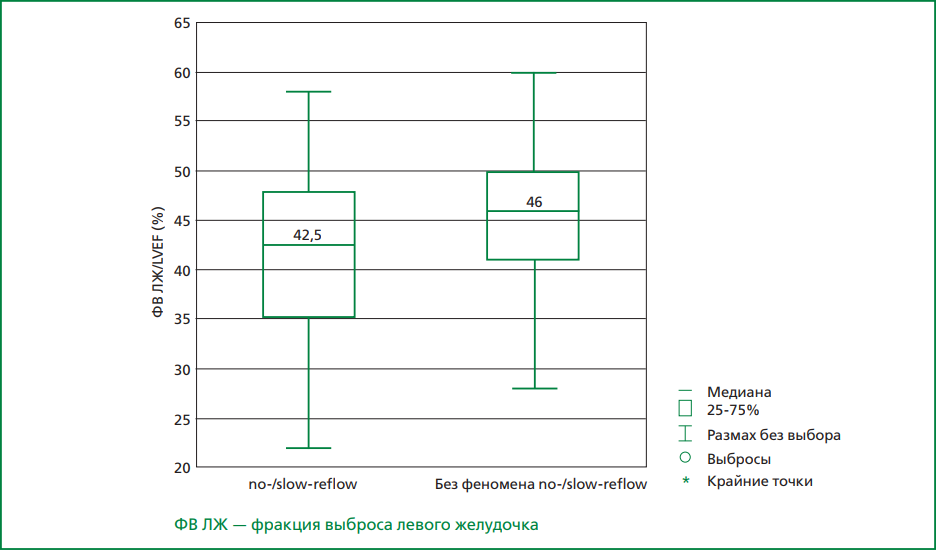
Рисунок 1. Среднее значение ФВ ЛЖ (%) в зависимости от наличия/отсутствия феномена «no-/slow-reflow».
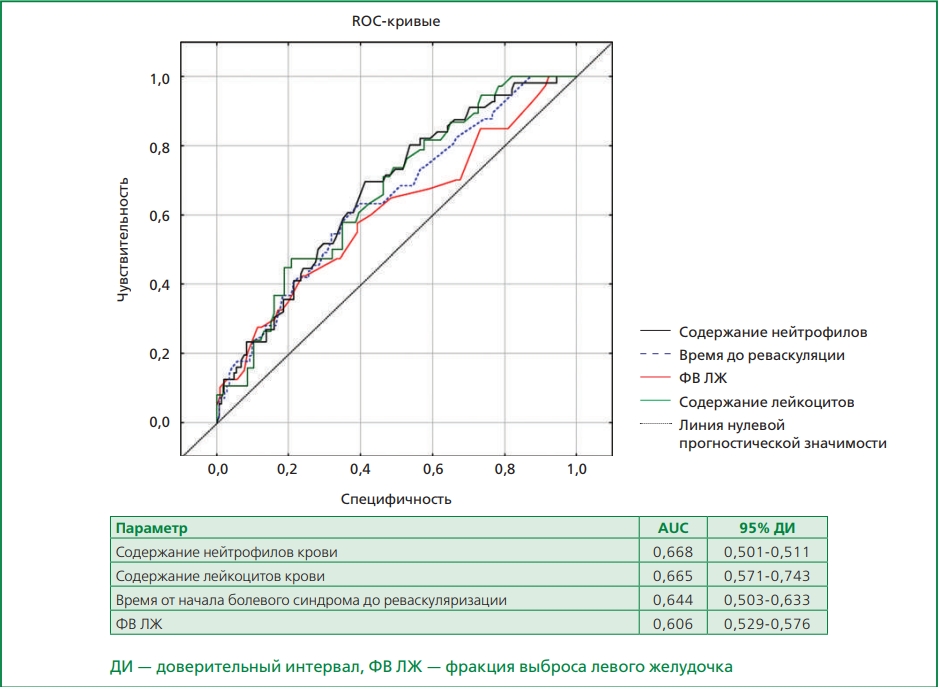
Рисунок 2. ROC-анализ факторов, ассоциированных с развитием «no-/slow-reflow».
Таблица 2. Лабораторные показатели пациентов с ОКС при поступлении в стационар в группах
Параметр | 1-я группа (n=59) | 2-я группа (n=149) | p |
Лейкоциты крови, ×109/л (Me [Q1; Q3]) | 10,9 [ 9,1; 13,2] | 9,5 [ 7,4; 11,6] | 0,0015 |
Нейтрофилы крови, ×109/л (Me [Q1; Q3]) | 8,4 [ 6,9; 15,7] | 6,6 [ 5,2; 7,6] | 0,0003 |
Отношение нейтрофилы/лейкоциты, % (Me [Q1; Q3]) | 77,5 [ 66; 82,2] | 70,8 [ 62,1; 79,6] | 0,01 |
Глюкоза крови, ммоль/л (Me [Q1; Q3]) | 8,3 [ 6,8; 10,9] | 8,1 [ 6,8; 9,9] | 0,278 |
Мочевина плазмы крови, ммоль/л (Me [Q1; Q3]) | 6,2 [ 5,3; 7,7] | 5,9 [ 4,8; 7,5] | 0,119 |
Креатинин, ммоль/л (Me [Q1; Q3]) | 98,9 [ 82,7; 115,3] | 91,2 [ 82,6; 106,6] | 0,216 |
СКФ по CKD-EPI, мл/мин/1,73 м2 (Me [Q1; Q3]) | 63 [ 47; 83] | 70,4 [ 57; 82] | 0,09 |
Холестерин, ммоль/л (M±SD) | 5,02±1,3 | 5,07±1,39 | 0,819 |
ЛНП, ммоль/л (M±SD) | 2,92±1,18 | 3,18±1,3 | 0,266 |
ОКС — острый коронарный синдром, СКФ — скорость клубочковой фильтрации, ЛНП — липопротеиды низкой плотности | |||
Таблица 3. Локализация очага ишемического повреждения по данным ЭКГ в исследуемых группах
Локализация ИМ, n (٪) | 1-я группа, n=59 | 2-я группа, n= 149 | p |
Передний | 35 (59,3) | 75 (50,3) | 0,018 |
Нижний | 17 (28,8) | 60 (40,2) | |
Нижне-боковой | 1 (1,7) | 0 (0) | |
Нижне-боковой, ПЖ | 1 (1,7) | 0 0) | |
Нижний, ПЖ | 2 (3,4) | 0 (0) | |
Передне-боковой | 1 (1,7) | 3 (2,0) | |
Передне-нижний | 2 (3,4) | 1 (0,7) | |
Распространённый передний | 0 (0) | 6 (4,0) | |
Задне-боковой | 0 (0) | 4 (2,68) | |
ЭКГ – электрокардиография, ПЖ – правый желудочек | |||
Таблица 4. ИСА у пациентов в изучаемых группах
ИСА, n (٪) | 1-я группа | 2-я группа | p |
Передняя межжелудочковая артерия | 33 (55,93) | 62 (41,61) | 0,657 |
Правая коронарная артерия | 17 (28,81) | 55 (36,91) | |
Ветви тупого края | 1 (1,69) | 2 (1,34) | |
Огибающая ветвь левой коронарной артерии | 4 (6,78) | 19 (12,75) | |
Диагональные ветви | 1 (1,69) | 2 (1,34) | |
Интермедиарная артерия | 0 (0) | 2 (1,34) | |
Ствол левой коронарной артерии | 1 (1,69) | 3 (2,01) | |
Многососудистое поражение | 2 (3,39) | 4 (2,68) | |
ИСА — инфаркт-связанная артерия | |||
Обсуждение
В проведенном исследовании авторы определили лабораторно-инструментальные факторы, ассоциированные с развитием феномена невосстановленного коронарного кровотока после выполнения ЧКВ у пациентов с ИМ в повседневной работе кардиологической службы стационара.
Обращало на себя внимание, что группы пациентов, выделенные в зависимости от наличия или отсутствия феномена «no-/slow-reflow» не различались по полу и возрасту, поэтому не представляется возможным выделить какую-то гендерную группу или возраст пациентов, ассоциированных с возникновением данного феномена.
Среди проанализированной коморбидной патологии наличие СД было значимо ассоциировано с развитием феномена невосстановленного коронарного кровотока. Эти данные находят подтверждение и в работах других авторов [14-18]. Механизмы, лежащие в основе патогенеза феномена невосстановленного кровотока — это не только процессы дистальной эмболии и микроваскулярной обструкции, но, прежде всего, процесс реперфузионного и продолжающегося ишемического повреждения [19]. При длительном ишемическом повреждении и, особенно, при реперфузии миокарда имеют большое значение процессы воспаления и иммунного ответа, составляющие звенья которых представляют собой сложную сеть взаимопереплетающихся каскадов. Многие иммунные реакции, наблюдаемые при ишемии/реперфузионном повреждении, по-видимому, имеют тенденцию к эскалации на фоне имеющегося у пациента СД [15].
Закономерным отражением более значительной активации системной воспалительной реакции и реакции в очаге ишемического повреждения миокарда является обнаруженный в настоящем исследовании в крови пациентов с феноменом невосстановленного кровотока более высокий уровень лейкоцитов и нейтрофилов крови. Эти клетки играют значительную роль не только в развитии воспалительных реакций, но принимают участие в регуляции функции эндотелия, выраженности окислительного стресса и выработке цитокинов, включая провоспалительные [20, 21]. Нейтрофилы продуцируют многочисленные вазоактивные вещества, что может приводить к дополнительной вазоконстрикции и формированию отека ткани, что способствует развитию феномена «no-reflow» [17][22].
Ассоциация между феноменом невосстановленного коронарного кровотока и снижением ФВ ЛЖ, вероятно, может быть обусловлена тем, что, несмотря на открытый просвет сосуда, фактически продолжается повреждение миокарда. Миокард повреждается как за счет продолжающейся ишемии (дополнительный вклад в который вносят и дистальная микроэмболия и дисфункция эндотелия и т.д.), так и за счёт реперфузионного повреждения, что приводит к увеличению размеров некроза миокарда [7][18][23]. При этом, по-видимому, снижение ФВ ЛЖ может быть не только следствием, но и условием для развития микроциркуляторной дисфункции. Пациенты с исходно сниженной ФВ ЛЖ могут быть более чувствительны к реперфузионному стрессу, что усиливает риск невосстановленного кровотока.
Оценка ЭКГ является рутинным, простым и дешёвым методом, поэтому многие авторы изучали возможность его применения для суждения о наличии и степени выраженности феномена невосстановленного коронарного кровотока. Так F. Dindas и соавт. установлена возможность прогнозирования развития феномена «no-/slow-reflow» при помощи QRS-индекса Сильвестра и оценки QRS-T паттерна у пациентов с ОКС без элевации сегмента ST [24]. В проведенной работе не проводился такой специфический анализ ЭКГ, однако необходимо отметить интересную особенность исследования F. Dindas и соавт.: исследуемую группу составили пациенты с ИМ без подъёма сегмента ST [24]. В представленном исследовании не у всех включенных пациентов, вошедших в окончательный анализ данных и у которых наблюдалось развитие «no-/slow-reflow» на контрольной КАГ, наблюдался подъём сегмента ST ЭКГ. Изменения передней стенки ЛЖ на ЭКГ в группе больных с развитием феномена «slow-/no-reflow» авторы наблюдали значимо чаще, что, возможно, объясняется большим размером очага ишемического повреждения при передней локализации ИМ и, следовательно, более активным местным и системным воспалительным и иммунным ответом на повреждение при такой локализации ишемического очага.
При этом, по данным исходной КАГ — выполненной до ЧКВ — не установлено различий по частоте поражения той или иной ИСА в 1-й и 2-й группах пациентов. Все указанное может отражать в некоторой степени несоответствия между топической ЭКГ диагностикой очага ишемического повреждения и данными по поражению той или иной ИСА по данным КАГ. Похожие результаты описали китайские исследователи [16]. В настоящем исследовании наблюдалась взаимосвязь между проксимальным повреждением ИСА и частотой развития невосстановленного коронарного кровотока. По-видимому, при проксимальном поражении ИСА бóльшая масса миокарда вовлекается в ишемическое повреждение, что в свою очередь увеличивает выраженность воспалительных реакций в очаге ишемического повреждения, дисфункции эндотелия и тромбозом микроваскулярного русла. Кроме того, увеличивается масса миокарда, вовлечённая в реперфузионное повреждение [6]. Несмотря на то, что анатомическая локализация поражения ИСА (в том числе проксимальная окклюзия) не является, очевидно, модифицируемым фактором риска, клиническое значение этого фактора, по мнению авторов, заключается в возможности ранней стратификации риска и, соответственно, индивидуализации стратегии реперфузии. Так, возможно рассматривать пациента с ОКС при ангиографической верификации проксимального поражения ИСА уже на начальном этапе интервенционного вмешательства, как находящегося в группе высокого риска развития феномена «no-/slow-reflow» и иметь в виду возможность применении агрессивной антитромботической терапии (включая, например, ингибиторы IIb/IIIa рецепторов), использования интракоронарного введения вазоактивных препаратов. С точки зрения техники проведения вмешательства, по-видимому, целесообразно избегать у таких пациентов повторной и агрессивной пред- и постдилатации, ограничивая механическую травматизацию интимы сосуда.
Время ишемии миокарда (от возникновения симптомов, до проведения ЧКВ) как в проведенном исследовании, так и в работах других авторов, являлось значимым фактором, влияющим на возникновение феномена невосстановленного коронарного кровотока [16][23][25][26].
Ограничения исследования
Проанализированные в исследовании факторы не являются исчерпывающими с точки зрения патогенеза рассмотренного феномена и возможных мишеней для коррекции, но они доступны для выявления в реальной клинической практике. Данная публикация предоставляет часть результатов регистра стационара по пациентам с ОКС и не включала анализ других параметров КАГ, кроме указанных в данной статье.
Работа представляет собой одноцентровое исследование, что могло отражаться в формировании единого мнения в диагностике; в заключительный анализ включена выборка сравнительно небольшого размера.
Заключение
Феномен невосстановленного/замедленного кровотока, диагностирующийся по данным контрольной КАГ при выполнении первичного ЧКВ у пациентов с ИМ, изучается многие годы и даже десятки лет, но многие вопросы по-прежнему остаются открытыми. Авторы проанализировали ряд клинических факторов и результатов лабораторно-инструментального обследования, ассоциированных с развитием феномена «no-/slow-reflow» в реальной клинической практике. Такие факторы, как общее время ишемии миокарда, наличие СД, низкая ФВ ЛЖ, повышенное содержание лейкоцитов и нейтрофилов крови, передняя локализация ИМ, проксимальный уровень окклюзии коронарной артерии, были ассоциированы с развитием
«no-/slow-reflow». По данным логистической регрессии независимыми предикторами невосстановленного кровотока служили: проксимальный уровень поражения коронарной артерии, сниженная ФВ ЛЖ, а также увеличение времени до реваскуляризации. Для того, чтобы влиять на частоту развития феномена невосстановленного коронарного кровотока, необходимо принимать во внимание возможности коррекции указанных факторов. С учетом неизменяемых факторов, таких, как анатомический уровень поражения ИСА, представляется возможной выработка корректной тактики ведения каждого пациента с ОКС в зависимости от предикторов и факторов риска, ассоциированных с развитием феномена невосстановленного коронарного кровотока, в частности, с теми факторами, которые были получены в проведённом исследовании.
Список литературы
1. Бойцов С.А., Шахнович Р.М., Терещенко С.Н. и др. Особенности реперфузионной стратегии лечения пациентов с инфарктом миокарда с подъемом сегмента ST по данным Российского регистра острого инфаркта миокарда — РЕГИОН-ИМ. Кардиология. 2024;64(2):3-17. DOI:10.18087/cardio.2024.2.n2601.
2. Мазнев Д.С., Болдуева С.А., Леонова И.А. и др. Осложнения первичного чрескожного коронарного вмешательства в сочетании с мануальной тромбоаспирацией у пациентов с инфарктом миокарда с подъемом сегмента ST. Скорая медицинская помощь. 2020;21(4):43-7. DOI:10.24884/2072-6716-2020-21-4-43-47.
3. Papapostolou S, Andrianopoulos N, Duffy SJ, et al. Long-term clinical outcomes of transient and persistent noreflow following percutaneous coronary intervention (PCI): a multicentre Australian registry. EuroIntervention. 2018;14(2):185-93. DOI:10.4244/ EIJ-D-17-00269.
4. Li H, Fu DG, Liu FY, et al. Evaluation of related factors, prediction and treatment drugs of no-reflow phenomenon in patients with acute ST-segment elevation myocardial infarction after direct PCI. Exp Ther Med. 2018;15(4):3940-6. DOI:10.3892/etm.2018.5900.
5. Namazi M, Mahmoudi E, Safi M, et al. The No-reflow Phenomenon: Is it Predictable by Demographic factors and Routine Laboratory Data? Acta Biomed. 2021;92(5):e2021297. DOI:10.23750/abm.v92i5.10053.
6. Ndrepepa G, Kastrati A. Coronary No-Reflow after Primary Percutaneous Coronary Intervention-Current Knowledge on Pathophysiology, Diagnosis, Clinical Impact and Therapy. J Clin Med. 2023;12(17):5592. DOI:10.3390/jcm12175592.
7. Bamarinejad F, Kermani-Alghoraishi M, Soleimani A, et al. Clinical, laboratory, and procedural predictors of slow flow/no reflow phenomenon after emergency percutaneous coronary interventions in ST-elevated myocardial infarction. Egypt Heart J. 2024;76(1):146. DOI:10.1186/s43044-024-00577-0.
8. Stensjøen AL, Hommerstad A, Halvorsen S, et al. Worst lead ST deviation and resolution of ST elevation at one hour for prediction of myocardial salvage, infarct size, and microvascular obstruction in patients with ST-elevation myocardial infarction treated with primary percutaneous coronary intervention. Ann Noninvasive Electrocardiol. 2020;25(6):e12784. DOI:10.1111/anec.12784.
9. Криночкин Д.В., Бессонов И.С., Кузнецов В.А. и др. Контрастная эхокардиография с оценкой миокардиальной перфузии в диагностике феномена «no-reflow» у пациента с острым инфарктом миокарда. Атеросклероз. 2019;15(2):52-8. DOI:10.15372/ATER20190208.
10. Arcari L, Cimino S, De Luca L, et al. Impact of Heart Rate on Myocardial Salvage in Timely Reperfused Patients with ST-Segment Elevation Myocardial Infarction: New Insights from Cardiovascular Magnetic Resonance. PLoS ONE 2015 10(12):e0145495. DOI:10.1371/journal.pone.0145495.
11. Староверов И.И., Шахнович Р.М., Гиляров М.Ю. и др. Евразийские клинические рекомендации по диагностике и лечению острого коронарного синдрома с подъемом сегмента ST (ОКСпST). Евразийский кардиологический журнал. 2020;(1):4-77. DOI:10.38109/2225-1685-2020-1-4-77.
12. Константинова Е.В., Муксинова М.Д., Гиляров М.Ю. и др. Клиническое значение феномена невосстановленного коронарного кровотока в работе регионального сосудистого центра. Кардиология. 2020;60(4):146-50. DOI:10.18087/cardio.2020.4.n976.
13. Константинова Е.В., Ильин Ю.С., Великоцкий А.А. и др. Клинические факторы, ассоциированные с развитием феномена невосстановленного коронарного кровотока у пациентов с острым коронарным синдромом. Рациональная Фармакотерапия в Кардиологии. 2024;20(1):27-34. DOI:10.20996/1819-6446-2024-2994.
14. Sun Y, Ren J, Li L, et el. RDW as A Predictor for No-Reflow Phenomenon in DM Patients with ST-Segment Elevation Myocardial Infarction Undergoing Primary Percutaneous Coronary Intervention. J Clin Med. 2023;12(3):807. DOI:10.3390/jcm12030807.
15. Zhao SR, Huang R, Liu F, et al. Study on Correlation between Type 2 Diabetes and No-Reflow after PCI. Dis Markers. 2022;2022:7319277. DOI:10.1155/2022/7319277.
16. Yu Y, Wu Y, Wu X, et al. Risk Factors for No-Reflow in Patients with STElevation Myocardial Infarction Who Underwent Percutaneous Coronary Intervention: A Case-Control Study. Cardiol Res Pract. 2022;2022:3482518. DOI:10.1155/2022/3482518.
17. Журавлев А.С., Азаров А.В., Семитко С.П., Иоселиани Д.Г. Феномен no-reflow во время первичного чрескожного коронарного вмешательства у пациентов с острым инфарктом миокарда с подъемом сегмента ST, обусловленным массивным коронарным тромбозом. Патогенез и предикторы noreflow. Кардиология. 2021;61(2):99-105. DOI:10.18087/cardio.2021.2.n1175.
18. Хубулава Г.Г., Козлов К.Л., Шишкевич А.Н. и др. Предикторы реперфузионного синдрома миокарда: современный взгляд на вопрос и актуальные проблемы. Часть 2: феномен невосстановленного коронарного кровотока, или феномен no-reflow (обзор литературы). Регионарное кровообращение и микроциркуляция. 2021;20(3):4–10. DOI:10.24884/1682-6655-2021-20-3-4-10.
19. Гиляров М.Ю., Иванов И.И., Константинова Е.В. и др. Феномен no-reflow и реперфузионное повреждение миокарда: механизмы и методы лечения. Клиницист. 2021;15(1-4):10-9. DOI:10.17650/1818-8338-2021-15-1-4-K645.
20. Wang J., Zhang F., Gao M. et al. The Systemic Immune Inflammatory Index Predicts No-Reflow Phenomenon after Primary Percutaneous Coronary Intervention in Older Patients with STEMI. Cardiovascular Innovations and Applications. 2023;7(1):10.15212/CVIA.2023.0005. DOI:10.15212/CVIA.2023.0005.
21. Bağcı A, Aksoy F. Systemic immune-inflammation index predicts new-onset atrial fibrillation after ST elevation myocardial infarction. Biomark Med. 2021;15(10):731-9. DOI:10.2217/bmm-2020-0838.
22. Durante A, Camici PG. Novel insights into an "old" phenomenon: the no reflow. Int J Cardiol. 2015;187:273-80. DOI:10.1016/j.ijcard.2015.03.359.
23. Nair Rajesh G, Jayaprasad N, Madhavan S, et al. Predictors and prognosis of no-reflow during primary percutaneous coronary intervention. Proc (Bayl Univ Med Cent). 2018;32(1):30-3. DOI:10.1080/08998280.2018.1509577.
24. Dindas F, Koyuncu I, Candan O, et al. Predictive role of Frontal QRS-T angle and Selvester QRS Score in determining angiographic slow flow phenomenon following percutaneous coronary intervention in patients with Non-ST elevation myocardial infarction. J Electrocardiol. 2021;69:20-6. DOI:10.1016/j.jelectrocard.2021.09.001.
25. Liu Y, Ye T, Chen K, et al. A nomogram risk prediction model for no-reflow after primary percutaneous coronary intervention based on rapidly accessible patient data among patients with ST-segment elevation myocardial infarction and its relationship with prognosis. Front Cardiovasc Med. 2022;9:966299. DOI:10.3389/fcvm.2022.966299. Erratum in: Front Cardiovasc Med. 2023;10:1229889. DOI:10.3389/fcvm.2023.1229889.
26. Frolov АА, Pochinka IG, Shakhov BЕ, et al. Using an artificial neural network to predict coronary microvascular obstruction (no-reflow phenomenon) during percutaneous coronary interventions in patients with myocardial infarction. Sovrem Tekhnologii Med. 2021;13(6):6-14. DOI:10.17691/stm2021.13.6.01.
Об авторах
Е. В. КонстантиноваРоссия
Константинова Екатерина Владимировна
Москва
Ю. С. Ильин
Россия
Ильин Юрий Сергеевич
Москва
А. А. Великоцкий
Россия
Великоцкий Антон Александрович
Москва
А. О. Черников
Россия
Черников Артем Олегович
Москва
М. С. Жданова
Россия
Жданова Мария Сергеевна
Москва
Е. В. Площенков
Россия
Площенков Евгений Валерьевич
Москва
Дополнительные файлы
Рецензия
Для цитирования:
Константинова Е.В., Ильин Ю.С., Великоцкий А.А., Черников А.О., Жданова М.С., Площенков Е.В. Какие данные клинического и лабораторно-инструментального обследования ассоциированы с развитием феномена невосстановленного коронарного кровотока у пациентов с острым коронарным синдромом? Рациональная Фармакотерапия в Кардиологии. 2025;21(3):200-208. https://doi.org/10.20996/1819-6446-2025-3190. EDN: ZRIATV
For citation:
Konstantinova E.V., Ilin Yu.S., Velikotskiy A.A., Chernikov A.O., Zhdanova M.S., Ploshchenkov E.V. Which сlinical, laboratory, and instrumental factors are associated with the development of the no-reflow phenomenon in patients with acute coronary syndrome? Rational Pharmacotherapy in Cardiology. 2025;21(3):200-208. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3190. EDN: ZRIATV

















































