Перейти к:
Прямые методы оценки приверженности к антигипертензивной терапии: контролируемый прием препаратов и терапевтический лекарственный мониторинг
https://doi.org/10.20996/1819-6446-2025-3192
EDN: TCNCNG
Аннотация
Низкая приверженность к терапии – одна из основных причин псевдорезистентной артериальной гипертензии (АГ), сопряжена с повышением риска сердечно-сосудистых осложнений и увеличением прямых и непрямых медицинских затрат. Оценка приверженности является важным элементом в ведении пациентов с неконтролируемой АГ, особенно при подозрении на устойчивость к терапии. «Золотого стандарта» оценки приверженности к терапии нет и поэтому, кроме непрямых методов, хотя и простых, но довольно ненадежных, в последнее время все чаще используются прямые способы — контроль приема препаратов в присутствии медперсонала, которые проводятся на фоне повторного мониторирования артериального давления при помощи портативных устройств или повторных его измерений специалистом, а также терапевтический мониторинг лекарственных препаратов или метаболитов в биологических жидкостях с использованием ультра-высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией. В данном описательном обзоре представлены ключевые результаты исследований по применению этих методов, рассмотрены их ограничения и преимущества, а также даны практические рекомендации по внедрению этих подходов в повседневную клиническую практику. Симультанное и как можно более раннее их применение позволяет исключить в ряде случаев необходимость в дополнительных сложных и затратных лечебно-диагностических процедурах, а также более точно и надежно выделить группу пациентов с истинно резистентной АГ — когорту, которая представляет наибольший научно-практический интерес. Использование рассмотренных подходов повышает клинико-экономическую эффективность лечения, помогает выявить парамедицинские проблемы и укрепляет взаимодействие между врачом и пациентом.
Ключевые слова
Для цитирования:
Ионов М.В., Емельянов И.В., Конради А.О. Прямые методы оценки приверженности к антигипертензивной терапии: контролируемый прием препаратов и терапевтический лекарственный мониторинг. Рациональная Фармакотерапия в Кардиологии. 2025;21(3):234-243. https://doi.org/10.20996/1819-6446-2025-3192. EDN: TCNCNG
For citation:
Ionov M.V., Emelyanov I.V., Konradi A.O. Direct methods for assessing adherence to antihypertensive therapy: witnessed intake and therapeutic drug monitoring. Rational Pharmacotherapy in Cardiology. 2025;21(3):234-243. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3192. EDN: TCNCNG
Введение
Артериальная гипертензия (АГ) остается главным, самым распространенным фактором риска сердечно-сосудистой заболеваемости и смертности [1], явно или косвенно приводящим к 10,8 млн фатальных исходов ежегодно [2]. Особое положение в ряду больных АГ занимают пациенты, у которых артериальное давление (АД) систематически определяется выше целевого диапазона, прежде всего в силу более серьезного их прогноза в отношении развития сердечно-сосудистых осложнений [3][4]. Среди лиц с неконтролируемой или предположительно резистентной АГ (отсутствие контроля АГ на фоне приема 3 и более антигипертензивных препаратов (АГП), в том числе диуретик) чаще всего встречаются больные, которые частично или даже полностью не соблюдают врачебные рекомендации. Недостаточная приверженность — одна из отличительных черт пациентов с хроническими неинфекционными заболеваниями [5], в том числе и с АГ [6]. Известно, что среди всех лиц с установленным диагнозом АГ, приверженность к антигипертензивной терапии (АГТ) составляет в целом около 50% [7][8], несколько ниже в Российской Федерации [9] и уменьшается еще примерно вдвое от исходного уровня в течение первого года лечения [10]. Приблизительно 12% лиц с АГ даже не начинают лечение [11]. Снижение приверженности у пациентов с АГ приводит к повышению сердечно-сосудистого риска per se [12]. Экономические потери вследствие неприверженности огромны [13], 90% дополнительных расходов возникают вследствие повторных госпитализаций [14]. Показано, что повышение приверженности приводит к существенному снижению рисков [15] и, по мнению некоторых экспертов, эффективнее, нежели разработка новых лекарственных препаратов [16].
Приверженность определяется как степень, в которой поведение пациента соответствует рекомендациям врача, и включает также персистенцию — длительность непрерывного следования рекомендациям [17]. В большинстве случаев недостаточная приверженность к лечению является непреднамеренной (забывчивость, невнимательность) [18]. В отличие от этого, преднамеренная неприверженность — это сознательное решение отойти от предписанной схемы лечения [19].
Диагностика неприверженности может проводиться непрямыми и прямыми методами. Первые дают лишь косвенное представление без верификации факта приема препарата: беседа с пациентами, заполнение специальных опросников [20-22], учет количества принятых препаратов, устройства для детекции открытия упаковок [23], мобильные приложения, сверка рецептурных листов, а также электронные таблетки-сенсоры, которые принимаются вместе с настоящим препаратом [24]. Простые интервью являются наименее точными и надежными [25]. Биоразлагаемые таблетки-сенсоры экономически невыгодны [26] и не отражают истинного поведения пациента [27]. Учет рецептурных листов невозможен в России, — почти все АГП отпускаются без рецепта; мобильные приложения для отслеживания приема препаратов в России редко используются пациентами [28].
Прямыми методами подтверждается прием препарата либо на момент проведения этой процедуры, либо накануне, что повышает их чувствительность [29]. Такими методами являются прием препаратов в присутствии медицинского персонала, а также терапевтический лекарственный мониторинг. Цель настоящего обзора — проанализировать возможности и ограничения этих прямых методов в контексте оценки приверженности к АГТ.
Прием препаратов под контролем медицинского персонала
Метод приема препаратов под контролем медицинского персонала, известный в англоязычной литературе как directly observed therapy (DOT) или witnessed drug intake, довольно давно применяется у пациентов с АГ [30] и заимствован из других областей медицины — используется у больных с легочным туберкулезом [31], ВИЧ [32], а также в психиатрической практике [33], однако чаще с целью эффективного и безопасного лечения.
При переносе этой методики в гипертензиологию она была усложнена одновременным выполнением суточного мониторирования АД (СМАД) и/или продолжительным медицинским наблюдением после приема АГП. Тем самым, DOT относится не только к определению факта приверженности к АГТ, но и к методам оценки ее эффективности, что выгодно отличает его от других непрямых и прямых вариантов оценки приверженности (рис. 1).
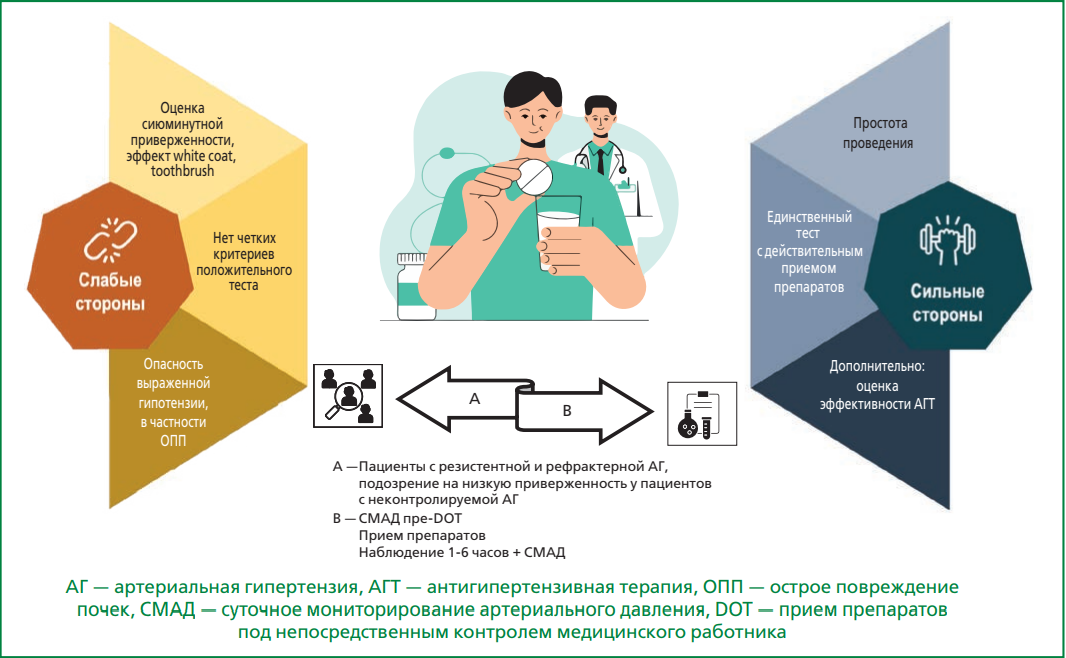
Рисунок 1. Прием препаратов под непосредственным контролем медицинского работника. Преимущества, недостатки и практические рекомендации.
Одни из первых сообщений о применимости, выполнимости и эффективности DOT появились в начале 2010-х. M. Ruzicka и соавт. в 2013 г. опубликовали описание клинического случая DOT у 53-летней пациентки с морбидным ожирением и рефрактерной АГ (определяемой как отсутствие контроля АГ на фоне приема 5 и более АГП), показав выраженное снижение систолического АД (САД) по данным СМАД с 177 мм рт.ст. до 97 мм рт.ст. в течение первого часа после приема утренних доз рекомендованных ранее 7 АГП. Установленная таким образом низкая приверженность к АГТ позволила редуцировать схему лечения до трех базовых АГП при удовлетворительном контроле суточного АД через 2 мес. [30][34].
Затем, как минимум две группы исследователей из Норвегии активно использовали DOT в рамках региональных пилотных проектов по симпатической денервации почечных артерий (ренальной денервации (РДН)) — Oslo-RDN (Effect of Renal Sympathetic Denervation on Resistant Hypertension and Cardiovascular Hemodynamic in Comparison to Intensive Medical Therapy Utilizing Impedance Cardiography) и DOT-HTN (Directly observed therapy prior to ambulatory blood pressure measurement) [35-37]. В публикациях F. E. M. Fadl Elmula и соавт. 6 из 18 участников, направленных на процедуру РДН, были исключены из числа потенциальных кандидатов после того, как у них при DOT на фоне ранее рекомендованной АГТ фиксировались целевые мониторные показатели АД [35]. Увеличив выборку до 65 пациентов с резистентной АГ, те же авторы выявили 20 неприверженных участников [36]. U. Hameed и соавт. в 2016 г. обследовали 50 пациентов с предполагаемой резистентной АГ и показали статистически незначимое снижение мониторного САД при DOT по сравнению с исходными показателями. Даже такие незначительные со статистической точки зрения различия позволили установить «истинность» резистентной АГ лишь у половины участников. Напротив, у 20% больных (как позже выяснилось, неприверженных к АГТ) была зафиксирована системная гипотензия во время DOT [37, 38]. U. Hjørnholm и соавт. в качественном анализе небольшой группы пациентов с неконтролируемой АГ без серьезной коморбидности, принимающих 2 и более АГП (n=16) не выявили значимых нежелательных явлений при DOT [39]. S. Heimark и соавт. в 2016 г. провели детальный скрининг направленных для РДН 83 больных, у 53 из которых диагноз резистентной АГ не подтвердился по большей части из-за низкой приверженности (32%), второй по частоте причиной исключения оказалась ранее не выявленная вторичная АГ (30%) [40].
М. Ruzicka и соавт. провели DOT у 48 амбулаторных пациентов с предполагаемой резистентной АГ, высоко приверженных к лечению по данным непрямых методов (анкетный опрос, подсчет таблеток). При этом среднее дневное САД у них снизилось в среднем на 10 мм рт.ст. непосредственно после DOT, и на 11 мм рт.ст. через 1 мес.; у 14 обследуемых была исключена устойчивость к АГТ [30]. Этот пример подчеркивает низкую диагностическую точность непрямых методов оценки приверженности.
Первый опыт применения DOT авторами данной статьи был описан в 2022 г. у 62-летнего пациента с предполагаемой рефрактерной АГ. Спустя 4 ч после приема большей части из назначенных ему ранее 7 АГП было отмечено значимое снижение САД с исходных 166 мм рт.ст. до 94 мм рт.ст. После получения результатов СМАД количество АГП сократили до четырех, с удовлетворительным контролем офисного АД спустя полгода [41]. В настоящее время авторы с успехом применяют DOT и у стационарных пациентов. Выполнение DOT в стационаре действительно оправдано: в исследовании А. Pio-Abreu и соавт. с участием 83 пациентов (69% с признаками рефрактерной АГ) истинная резистентная АГ была после DOT подтверждена у 77% из них, а истинная рефрактерность — лишь у 32,5%. Количество АГП и показатели мониторного САД снизились, и оставались в рамках целевого диапазона в течение 7 мес. после выписки [42].
Один из недостатков классического варианта DOT — необходимость прибыть и находиться в медицинском центре на протяжении определенного времени. Однако появившаяся недавно практика видео-DOT, апробированная у пациентов с различными формами туберкулеза [43], была недавно успешно использована авторами в исследовании телемедицинского сопровождения пациентов с неконтролируемой АГ [44].
Терапевтический мониторинг лекарственных препаратов
Изначально методика терапевтического лекарственного мониторинга (ТЛМ) была направлена на определение эффективных или токсических уровней препаратов, но оценка приверженности к АГТ требует обнаружения минимальных концентраций действующих веществ или их метаболитов [45]. Методы количественного анализа АГП были разработаны в конце 2000-х гг. [46-48].
Довольно быстро появились первые сообщения об истинном уровне неприверженности среди лиц с предполагаемой резистентной АГ: J. Ceral и соавт. выяснили, что более 65% из 84 амбулаторных пациентов были не привержены назначенной АГТ (половина из них — полностью не привержены) [49]. Схожая картина продемонстрирована О. Jung и соавт. при анализе образцов мочи в группе 76 больных — 50% из них оказались неприверженными [50]. Пилотные исследования способствовали распространению использования прямых методов оценки приверженности, которые используется сейчас в крупных международных многоцентровых рандомизированных клинических исследованиях — в большинстве современных исследований применяются DOT и/или ТЛМ [51]. В 2013 г. В. Štrauch и соавт. провели анализ содержания АГП в сыворотке у 339 пациентов с резистентной АГ (176 госпитализированных и 163 амбулаторных), в результате которого выяснилось, что около 47% амбулаторных пациентов были в той или иной степени не привержены терапии. Среди госпитализированных больных уровень неприверженности был значительно ниже (19%) [52]. В дальнейшем были разработаны различные модификации аналитических методов на основе плазмы крови, при использовании которых частота выявления низкого приверженности также была довольно высокой — от 42% до 86% [53][54].
В настоящее время установленной методикой ТЛМ является определение АГП и/или их метаболитов с использованием ультра-высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (ВЭЖХ-МС) (рис. 2). Основными биологическими жидкостями для ТЛМ являются кровь (цельная, плазма, сыворотка) и моча. Хотя предложены и другие источники обнаружения АГП, такие как «сухая капля» крови [55], слюна [56] и даже волосы [57], пока что они не получили широкого распространения. Несмотря на то, что еще 10 лет назад некоторые авторы высказывали предположения о непрактичности ТЛМ, в первую очередь ввиду высокой стоимости проведения анализа [15, 58], проведенные впоследствии клинико-экономические исследования свидетельствуют, что ТЛМ экономически эффективен в разных популяциях [48][59], намного дешевле РДН, а также применения таблеток-сенсоров [60], поэтому широко доступен в западных странах и включен в большинство медицинских страховых пакетов [61]. Основные первоначальные затраты — приобретение оборудования, обучение персонала и пробоподготовка [62], в дальнейшем же ТЛМ быстро окупается. С 2014 по 2021 гг. в Великобритании возникло 35 ТЛМ-центров, в континентальной Европе по данным на 2022 г. было уже 50 таких учреждений [63].
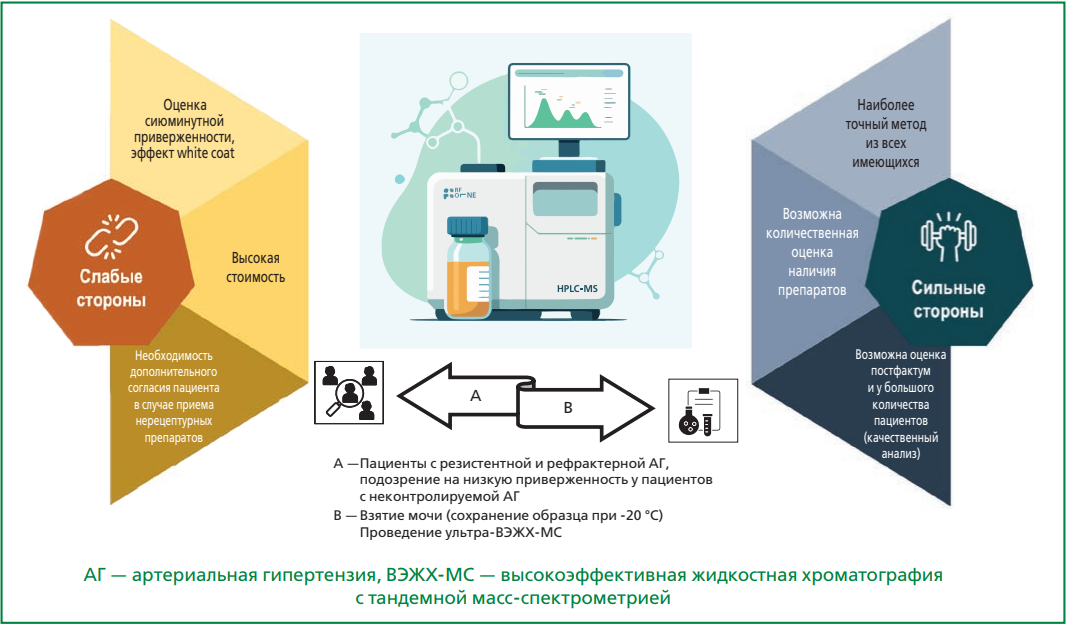
Рисунок 2. Терапевтический лекарственный мониторинг. Преимущества, недостатки и практические рекомендации.
Вместе со снижением стоимости ВЭЖХ-МС с начала 2010-х гг. количество публикаций стало расти. В исследовании М. Tomaszewski и соавт. в 2014 г. с участием более 200 пациентов (в том числе 17 кандидатов для выполнения РДН) и качественной оценкой в моче 40 наиболее часто назначаемых АГП была показана 25%-я частота неприверженности, 4 потенциальных кандидата для РДН были полностью не привержены [27]. Объединенный анализ 9 исследований из 5 стран (747 участников с трудно контролируемой или резистентной АГ) с применением ВЭЖХ-МС плазмы или мочи показал, что уровень низкой приверженности варьировал от 23 до 63% [15].
Вторая половина 2010-х и начало 2020-х гг. обозначились значительно более крупными исследованиями. Во французском одноцентровом проекте среди 386 пациентов с резистентной АГ было выявлено, что у 25% фиксировалась низкая приверженность, у 47% — частичная и только 28% больных полностью соблюдали предписанный режим лечения [64]. Отметим также исследование RHYME-RCT (Resistant HYpertension: MEasure to ReaCh Targets), включавшее 100 пациентов с резистентной АГ с применением ВЭЖХ-МС, в котором было показано повышение приверженности к АГТ в долгосрочной перспективе после ТЛМ [65]. Сохраняется выраженная гетерогенность результатов исследований с применением ТЛМ. В исследовании 2019 г. (n=91) было показано, что при качественном анализе доля неприверженных лиц составляла лишь 7%, тогда как количественный анализ увеличивает ее до 20% [66]. Еще один пример — работа J.P. Sheppard и соавт., в которой среди 191 пациента с АГ (в том числе 62% с контролируемой АГ) доля неприверженных составила около 5%, что может указывать на тот факт, что применение ТЛМ не должно рассматриваться в качестве облигатного метода среди всех гипертензивных больных [67]. В исследовании А. J. Lawson и соавт. были проанализированы данные 300 пациентов, из которых 166 участников не придерживались назначенной схемы АГТ, а 20% из них полностью игнорировали прием препаратов. Отличительной особенностью этого исследования стала неожиданность — обследуемые хотя и давали (вербальное) согласие на проведение ТЛМ, но не были заранее предупреждены, на каком из визитов он действительно будет предпринят [68].
Интересным является не только сам факт обозначения неприверженности, но и сравнительный анализ неприверженных пациентов и больных с симптоматическими формами АГ или с другими вариантами псевдорезистентности. В исследовании О. Jung и соавт. из 108 пациентов с предполагаемой резистентной АГ у 15 была выявлена вторичная АГ, и у 40 — недостаточная приверженность к назначенной АГТ (12 из них были полностью непривержены). Таким образом, втрое чаще причиной устойчивости к АГТ становилась именно неприверженность, а не вторичная АГ [50]. В работе S. L. Daugherty и соавт. частота выявления вторичной АГ составила <1%, оказавшись существенно ниже доли неприверженных больных (12,8%) [69]. Наиболее демонстративным можно назвать исследование Р. Patel и соавт., в котором приняли участие 34 пациента, направленных на РДН [70]. Подтверждённая качественным ТЛМ-анализом мочи низкая приверженность оказалась наиболее частой причиной несоответствия критериям отбора для РДН (24%). Без биохимического скрининга приверженности терапии показатель соответствия составил бы 38%. Полученные данные о распространенности низкой приверженности, важности проведения ТЛМ вновь поднимают вопрос этапности скрининговых методик исключения псевдорезистентности. По мнению А. Velasco и соавт., скрининг первичного альдостеронизма до или после ТЛМ, тактика с первоначальным ТЛМ намного более диагностически точна и экономически выгодна [71].
ТЛМ также активно используется с целью фармакокинетической оценки определенных классов АГП. Несколько из них метаболизируются при участии различных изоформ цитохрома P-450. Вследствие полиморфизма генов, различий CYP-зависимого метаболизма наблюдается значительная межиндивидуальная вариабельность сывороточных концентраций АГП. У ряда больных также может различаться абсорбция этих препаратов в желудочно-кишечном тракте. Более того, такие факторы, как старение, нарушение функции печени, лекарственные взаимодействия, состояния, влияющие на печеночный кровоток вносят вклад в изменения клиренса АГП [72]. В исследовании Т. А. Родиной и соавт. на основе выборки из 42 пациентов была продемонстрирована возможность применения ВЭЖХ-МС для индивидуальной оценки фармакокинетических параметров АГП и контроля приверженности на основании измерения концентраций препарата в плазме крови. Больные получали различные дозы нифедипина, авторы смогли определить фенотип пациента по скорости метаболизма АГП и скорректировать его дозировку исходя из полученных данных [73]. С. В. Селезнев и соавт. в небольшом пилотном проекте у 56 пациентов (n=39 с контролируемой АГ) показали, что у большой доли пациентов концентрации назначенных АГП в плазме при стабильном приеме не достигают требуемого целевого диапазона [74]. В перспективе необходимы дальнейшие исследования оценки количества и характера требуемых тестов, в зависимости от фармакокинетических параметров, а также влияния применения этих аналитических методов для коррекции низкой приверженности к лечению и их связи с долгосрочными результатами.
Практические рекомендации по использованию прямых методов оценки приверженности
Для получения достоверных результатов применения прямых методов оценки приверженности, важны практические аспекты их внедрения. Уже упомянутые авторы из Канадского центра компетенций предлагают использовать короткий скрининговый протокол DOT с 4-6-часовым наблюдением в клинике [75]. Исследователи из Норвегии в своих работах наблюдали амбулаторных пациентов в течение всего лишь 2 ч и не выявили значимых нежелательных реакций [36, 39]. Остается не вполне ясным диагностический порог ∆ АД «до-после» DOT. М. А. Hameed и соавт., в отсутствие такового использовали произвольный критерий разницы среднесуточного САД в ≥5 мм рт.ст. [38]. Можно подвергнуть сомнению обоснованность столь низкого граничного значения, поскольку выводы о недостаточной приверженности могут иметь серьезные терапевтические последствия, повлиять на взаимоотношения между врачом и пациентом.
Имея целью стандартизировать ТЛМ и повысить его эффективность, в 2022 г. экспертами в этой области был подготовлен структурированный рекомендательный документ [63]. Авторы обзора не будут останавливаться на каждом из упомянутых в нем аспектов и коснутся лишь основных положений: а) в рамках подготовительной работы требуется создание матрицы наиболее часто назначаемых АГП, б) целесообразно использовать качественную, а не количественную оценочную шкалу, в) формировать простой и понятный для пациентов отчет с результатами оценки АГП, и г) обсуждать результаты ТЛМ c пациентом вне зависимости от итога анализа.
Отличительной чертой DOT и ТЛМ является феномен «белого халата» — приверженность часто улучшается непосредственно перед и после визита к врачу, создавая ложное впечатление об удовлетворительной приверженности [76]. Миновать это ограничение зачастую трудно из-за этических соображений: пациент должен быть информирован о проводимых вмешательствах и диагностических манипуляциях. Повысить достоверность их результатов при соблюдении этических норм можно, получив информированное согласие на проведение описанных процедур во время последующих визитов исходно и однократно [77]. Даже при полной информированности пациента оба метода можно использовать как минимум для определения эффективности АГТ.
По мнению авторов настоящего обзора, не стоит отдавать предпочтение какому-то отдельному методу и использовать их по возможности симультанно. Такой подход обоснован и проанализирован в обзорах проблемы приверженности [45][78]. Ярким примером служит и клинический случай 59-летнего пациента с отсутствием контроля АГ, несмотря на ранее проведенную РДН. При ТЛМ был найден лишь один из назначенных 10 АГП, а затем проведён DOT, в процессе которого у пациента развилась выраженная симптомная системная гипотензия и острое повреждение почек, потребовавшей симптоматической терапии. При сокращении АГТ до 4 АГП у пациента была достигнута стойкая нормотензия [79]. Другим подтверждением служит прямое сравнительное исследование DOT и ТЛМ, в котором L. V. Halvorsen и соавт. на протяжении 7 лет наблюдали 19 пациентов с резистентной АГ, чья приверженность была подтверждена изначально DOT. C течением времени 7 пациентов были повторно расценены как неприверженные на основании результатов ТЛМ. Неприверженные пациенты при заполнении специального опросника Beliefs about Medicines Questionnaire выражали сомнения по поводу самой необходимости АГТ, хотя активно не обсуждали свои опасения с врачом [80]. Как показывает недавний обзор причин неприверженности, пациенты редко сообщают врачу о пропусках или полной остановке приема текущей АГТ [81]. Отечественное исследование Л. Б. Лазебника и соавт. демонстрирует и низкую базовую осведомленность пациентов — 54% больных признаются, что лишь отчасти информированы о важности назначенной АГТ и ее предполагаемой продолжительности [82], а в опросе 200 врачей европейских клиник продемонстрированы более чем скромные временные затраты врача на обсуждение вопросов, связанных с АГТ [83].
Учитывая тот факт, что в России обе прямые методики пока еще не получили широкого распространения, авторы обзора предлагают открыть дискуссию на тему практического их внедрения. Ниже приводится разработанная авторами схема ведения амбулаторных пациентов с предполагаемой резистентной АГ, значительные роли в которой отданы обсуждаемым прямым методам оценки приверженности (рис. 3). Точка зрения авторов — следует в первую очередь подтвердить факт приема АГП, и затем переходить к другим более сложным и затратным процедурам, использование валидированных опросников при первом контакте с пациентом остается важным шагом, так как это во-первых, хотя бы частично помогает дифференцировать пациентов с низкой приверженностью, а во-вторых может выявить её причины [77].
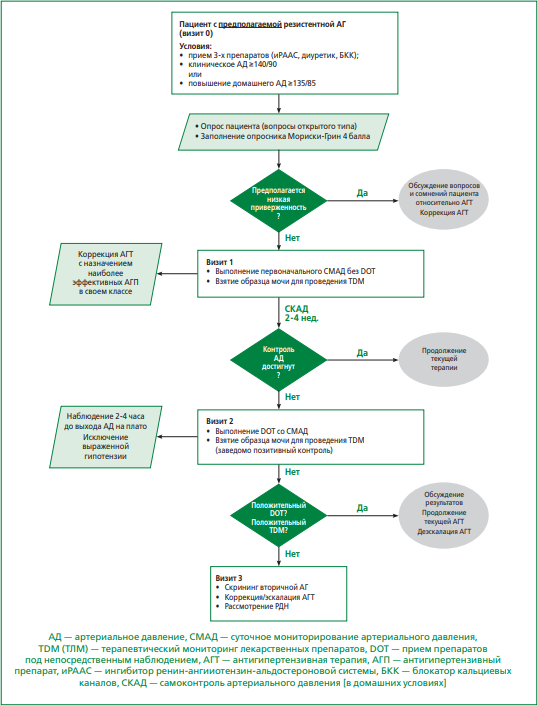
Рисунок 3. Интеграция прямых методов оценки приверженности к АГТ в амбулаторных и стационарных условиях.
Заключение
Оценка приверженности — важный элемент в лечении пациентов с неконтролируемой АГ, особенно при подозрении на устойчивость к АГТ. Прямые методы оценки приверженности характеризуются высокой точностью, но имеют определенные недостатки — частый феномен «белого халата», высокая изначальная стоимость. Тем не менее, при должной подготовке персонала вполне возможно внедрение обеих методик в амбулаторную практику. Использование данных подходов повышает клиническую и экономическую эффективность лечения, помогает выявить парамедицинские проблемы и укрепляет взаимодействие между врачом и пациентом.
Список литературы
1. NCD Risk Factor Collaboration (NCD-RisC). Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. Lancet. 2021;398(10304):957-80. DOI:10.1016/S0140-6736(21)01330-1. Erratum in: Lancet. 2022;399(10324):520. DOI:10.1016/S0140-6736(22)00061-7.
2. Egan BM, Kjeldsen SE, Grassi G, et al. The global burden of hypertension exceeds 1.4 billion people: should a systolic blood pressure target below 130 become the universal standard? J Hypertens. 2019;37(6):1148-53. DOI:10.1097/HJH.0000000000002021.
3. de la Sierra A, Ruilope LM, Staplin N, et al. Resistant Hypertension and Mortality: An Observational Cohort Study. Hypertension. 2024;81(11):2350-6. DOI:10.1161/HYPERTENSIONAHA.124.23276.
4. Buhnerkempe MG, Prakash V, Botchway A, et al. Adverse Health Outcomes Associated With Refractory and Treatment-Resistant Hypertension in the Chronic Renal Insufficiency Cohort. Hypertension. 2021:77(1):72-81. DOI:10.1161/HYPERTENSIONAHA.120.15064.
5. Nieuwlaat R, Wilczynski N, Navarro T, et al. Interventions for enhancing medication adherence. Cochrane Database Syst Rev. 2014;2014(11):CD000011. DOI:10.1002/14651858.CD000011.pub4.
6. Tajeu GS, Kent ST, Huang L, et al. Antihypertensive Medication Nonpersistence and Low Adherence for Adults <65 Years Initiating Treatment in 2007-2014. Hypertension. 2019;74(1):35-46. DOI:10.1161/HYPERTENSIONAHA.118.12495.
7. Burnier M, Egan BM. Adherence in Hypertension. Circ Res. 2019;124(1):1124-40. DOI:10.1161/CIRCRESAHA.118.313220.
8. Mazzaglia G, Ambrosioni E, Alacqua M, et al. Adherence to antihypertensive medications and cardiovascular morbidity among newly diagnosed hypertensive patients. Circulation 2009;120(16):1598-605. DOI:10.1161/CIRCULATIONAHA.108.830299.
9. Bochkareva EV, Butina EK, Kim IV, et al. Adherence to antihypertensive medication in Russia: a scoping review of studies on levels, determinants and intervention strategies published between 2000 and 2017. Arch Public Health. 2019;77:43. DOI:10.1186/s13690-019-0366-9.
10. Vrijens B, Vincze G, Kristanto P, et al. Adherence to prescribed antihypertensive drug treatments: longitudinal study of electronically compiled dosing histories. BMJ. 2008;336(7653):1114-7. DOI:10.1136/bmj.39553.670231.25.
11. Lemstra M, Nwankwo C, Bird Y, Moraros J. Primary nonadherence to chronic disease medications: a meta-analysis. Patient Prefer Adherence. 2018;12:721-31. DOI:10.2147/PPA.S161151.
12. Lee H, Yano Y, Cho SMJ, et al. Adherence to Antihypertensive Medication and Incident Cardiovascular Events in Young Adults With Hypertension. Hypertension. 2021;77(4):1341-9. DOI:10.1161/HYPERTENSIONAHA.120.16784.
13. Cutler RL, Fernandez-Llimos F, Frommer M, et al. Economic impact of medication non-adherence by disease groups: a systematic review. BMJ Open. 2018;8(1):e016982. DOI:10.1136/bmjopen-2017-016982.
14. Parekh N, Ali K, Stevenson JM, et al. Incidence and cost of medication harm in older adults following hospital discharge: a multicentre prospective study in the UK. Br J Clin Pharmacol. 2018;84(8):1789-97. DOI:10.1111/bcp.13613.
15. Berra E, Azizi M, Capron A, et al. Evaluation of Adherence Should Become an Integral Part of Assessment of Patients With Apparently TreatmentResistant Hypertension. Hypertension. 2016;68(2):297-306. DOI:10.1161/HYPERTENSIONAHA.116.07464.
16. Haynes RB, McDonald H, Garg AX, Montague P. Interventions for helping patients to follow prescriptions for medications. Cochrane Database Syst Rev. 2002;(2):D000011. DOI:10.1002/14651858.CD000011.
17. Burnier M. Medication adherence and persistence as the cornerstone of effective antihypertensive therapy. Am J Hypertens. 2006;19(11):1190-6. DOI:10.1016/j.amjhyper.2006.04.006.
18. Лукина Ю.В., Кутишенко Н.П., Марцевич С.Ю., Драпкина О.М. Проблемные вопросы и разработка классификаций основных параметров качества и приверженности фармакотерапии. Часть I: приверженность пациентов к лечению. Кардиоваскулярная терапия и профилактика. 2023;22(6):3603] DOI:10.15829/17288800-2024-4268.
19. Mukhtar O, Weinman J, Jackson SH. Intentional non-adherence to medications by older adults. Drugs Aging. 2014;31(3):149-57. DOI:10.1007/s40266-014-0153-9.
20. Morisky DE, Green LW, Levine DM. Concurrent and Predictive Validity of a SelfReported Measure of Medication Adherence. Medical Care. 1986;24(1):67-74. DOI:10.1097/00005650-198601000-00007.
21. Николаев Н.А., Скирденко Ю.П. Российский универсальный опросник количественной оценки приверженности к лечению (КОП-25). Клиническая фармакология и терапия. 2018;27(1):74-8]
22. Kim MT, Hill MN, Bone LR, Levine DM. Development and testing of the HillBone Compliance to High Blood Pressure Therapy Scale. Prog Cardiovasc Nurs. 2000;15(3):90-6. DOI:10.1111/j.1751-7117.2000.tb00211.x.
23. El Alili M, Vrijens B, Demonceau J, et al. A scoping review of studies comparing the medication event monitoring system (MEMS) with alternative methods for measuring medication adherence. Br J Clin Pharmacol. 2016;82(1):268-79. DOI:10.1111/bcp.12942.
24. Sideri K, Cockbain J, Van Biesen W, et al. Digital pills for the remote monitoring of medication intake: a stakeholder analysis and assessment of marketing approval and patent granting policies. J Law Biosci. 2022;9(2):lsac029. DOI:10.1093/jlb/lsac029.
25. Meddings J, Kerr EA, Heisler M, Hofer TP. Physician assessments of medication adherence and decisions to intensify medications for patients with uncontrolled blood pressure: still no better than a coin toss. BMC Health Serv Res. 2012;12:270. DOI:10.1186/1472-6963-12-270.
26. Park LG, Howie-Esquivel J, Dracup K. Electronic measurement of medication adherence. West J Nurs Res. 2015;37(1):28-49. DOI:10.1177/0193945914524492.
27. Tomaszewski M, White C, Patel P, et al. High rates of non-adherence to antihypertensive treatment revealed by high-performance liquid chromatography-tan dem mass spectrometry (HP LC-MS/MS) urine analysis. Heart. 2014;100(11):855- 61. DOI:10.1136/heartjnl-2013-305063.
28. Polukhin NV, Nikolic TR, Ekkert NV, et al. The Analysis of the Context of Digital Access to Healthcare in Russia. Sustainability. 2023;15(3):2271. DOI:10.3390/su15032271.
29. Bourque G, Ilin JV, Ruzicka M, et al. Nonadherence Is Common in Patients With Apparent Resistant Hypertension: A Systematic Review and Meta-analysis. Am J Hypertens. 2023;36(7):394-403. DOI:10.1093/ajh/hpad013.
30. Ruzicka M, Leenen FHH, Ramsay T, et al. Use of Directly Observed Therapy to Assess Treatment Adherence in Patients With Apparent Treatment-Resistant Hypertension. JAMA Intern Med. 2019;179(10):1433-4. DOI:10.1001/jamainternmed.2019.1455.
31. Tian JH, Lu ZX, Bachmann MO, Song FJ. Effectiveness of directly observed treatment of tuberculosis: a systematic review of controlled studies. Int J Tuberc Lung Dis. 2014;18(9):1092-8. DOI:10.5588/ijtld.13.0867.
32. Hart JE, Jeon CY, Ivers LC, et al. Effect of directly observed therapy for highly active antiretroviral therapy on virologic, immunologic, and adherence outcomes: a meta-analysis and systematic review. J Acquir Immune Defic Syndr. 2010;54(2):167-79. DOI:10.1097/QAI.0b013e3181d9a330. Erratum in: J Acquir Immune Defic Syndr. 2011;56(1):e37-8.
33. Ducroix C, Choudey M, Cornic F, et al. Directly observed therapy (DOT) in a psychiatric consulting dispensary, long term practice and retrospective study of patients coming every day [abstract]. European Psychiatry. 2007;22(1):S207. DOI:10.1016/j.eurpsy.2007.01.688.
34. Ruzicka M, McCormick B, Leenen FHH, et al. Adherence to blood pressure-lowering drugs and resistant hypertension: should trial of direct observation therapy be part of preassessment for renal denervation? Can J Cardiol. 2013;29(12):1741. e1-3. DOI:10.1016/j.cjca.2013.07.678.
35. Fadl Elmula FE, Hoffmann P, Fossum E, et al. Renal Sympathetic Denervation in Patients With Treatment-Resistant Hypertension After Witnessed Intake of Medication Before Qualifying Ambulatory Blood Pressure. Hypertension. 2013;62(3):526-32. DOI:10.1161/HYPERTENSIONAHA.113.01452.
36. Fadl Elmula FE, Hoffmann P, Larstorp AC, et al. Adjusted drug treatment is superior to renal sympathetic denervation in patients with true treatment-resistant hypertension. Hypertension 2014;63(5):991-9. DOI:10.1161/HYPERTENSIONAHA.114.03246.
37. Hjørnholm U, Aamodt M, Larstorp AC, et al. Directly Observed Therapy in Hypertension (DOT-HTN). In: Burnier M, editor. Drug Adherence in Hypertension and Cardiovascular Protection, Cham: Springer International Publishing; 2018, p. 57-85. DOI:10.1007/978-3-319-76593-8_6.
38. Hameed MA, Tebbit L, Jacques N, et al. Non-adherence to antihypertensive medication is very common among resistant hypertensives: results of a directly observed therapy clinic. J Hum Hypertens. 2016;30(2):83-9. DOI:10.1038/jhh.2015.38.
39. Hjørnholm U, Larstorp ACK, Andersen MH, Høieggen A. Directly observed therapy prior to ambulatory blood pressure measurement (DOT-HTN) in uncontrolled hypertensive patients — Effect on blood pressure, safety and patient perception. Blood Press. 2019;28(5):327-35. DOI:10.1080/08037051.2019.1633907.
40. Heimark S, Eskås PA, Mariampillai JE, et al. Tertiary work-up of apparent treatment-resistant hypertension. Blood Press. 2016;25(5):312-8. DOI:10.3109/08037051.2016.1172865.
41. Ионов М.В., Емельянов И.В., Вахрушев А.Д. и др. Опыт применения многоконтактных катетерных систем для проведения радиочастотной симпатической денервации почечных артерий у пациентов с резистентной артериальной гипертензией: непосредственные результаты вмешательства. Российский кардиологический журнал. 2022;27(2):4794. DOI:10.15829/1560-4071-2022-4794.
42. Pio-Abreu A, Trani-Ferreira F, Silva GV, et al. Directly observed therapy for resistant/refractory hypertension diagnosis and blood pressure control. Heart. 2022;108(24):1952-6. DOI:10.1136/heartjnl-2022-320802.
43. Browne SH, Umlauf A, Tucker AJ, et al. Wirelessly observed therapy compared to directly observed therapy to confirm and support tuberculosis treatment adherence: A randomized controlled trial. PLoS Med. 2019;16(10):e1002891. DOI:10.1371/journal.pmed.1002891.
44. Ionov MV, Zhukova OV, Yudina YS, et al. Value-based approach to blood pressure telemonitoring and remote counseling in hypertensive patients. Blood Press. 2021;30(1):20-30. DOI:10.1080/08037051.2020.1813015.
45. Versmissen J, van Steenkiste J, Koch BCP, Peeters LEJ. “Under pressure”: The role of therapeutic drug monitoring in the treatment of hypertension. Br J Clin Pharmacol. 2024;90(8):1884-91. DOI:10.1111/bcp.16125.
46. Iriarte G, Gonzalez O, Ferreirós N, et al. Validation of a fast liquid chromatography-UV method for the analysis of drugs used in combined cardiovascular therapy in human plasma. J Chromatogr B Analyt Technol Biomed Life Sci. 2009;877(27):3045-53. DOI:10.1016/j.jchromb.2009.07.018.
47. Gonzalez O, Iriarte G, Rico E, et al. LC-MS/MS method for the determination of several drugs used in combined cardiovascular therapy in human plasma. J Chromatogr B Analyt Technol Biomed Life Sci. 2010;878(28):2685-92. DOI:10.1016/j.jchromb.2010.07.026.
48. Brinker S, Pandey A, Ayers C, et al. Therapeutic drug monitoring facilitates blood pressure control in resistant hypertension. J Am Coll Cardiol. 2014;63(8):834-5. DOI:10.1016/j.jacc.2013.10.067.
49. Ceral J, Habrdova V, Vorisek V, et al. Difficult-to-control arterial hypertension or uncooperative patients? The assessment of serum antihypertensive drug levels to differentiate non-responsiveness from non-adherence to recommended therapy. Hypertens Res. 2011;34(1):87-90. DOI:10.1038/hr.2010.183.
50. Jung O, Gechter JL, Wunder C, et al. Resistant hypertension? Assessment of adherence by toxicological urine analysis. J Hypertens. 2013;31(4):766-74. DOI:10.1097/HJH.0b013e32835e2286.
51. Schlaich MP, Bellet M, Weber MA, et al. Dual endothelin antagonist aprocitentan for resistant hypertension (PRECISION): a multicentre, blinded, randomised, parallel-group, phase 3 trial. Lancet. 2022;400(10367):1927-37. DOI:10.1016/S0140-6736(22)02034-7. Erratum in: Lancet. 2023;401(10373):268. DOI:10.1016/S0140-6736(23)00119-8.
52. Strauch B, Petrák O, Zelinka T, et al. Precise assessment of noncompliance with the antihypertensive therapy in patients with resistant hypertension using toxicological serum analysis. J Hypertens. 2013;31(12):2455-61. DOI:10.1097/HJH.0b013e3283652c61.
53. Peeters LEJ, Feyz L, Boersma E, et al. Clinical Applicability of Monitoring Antihypertensive Drug Levels in Blood. Hypertension. 2020;76(1):80-6. DOI:10.1161/HYPERTENSIONAHA.120.15038.
54. de Jager RL, Maarseveen EM van, Bots ML, Blankestijn PJ.; SYMPATHY investigators. Medication adherence in patients with apparent resistant hypertension: findings from the SYMPATHY trial. Br J Clin Pharmacol. 2018;84(1):18-24. DOI:10.1111/bcp.13402.
55. Bernieh D, Lawson G, Tanna S. Quantitative LC-HRMS determination of selected cardiovascular drugs, in dried blood spots, as an indicator of adherence to medication. J Pharm Biomed Anal. 2017;142:232-43. DOI:10.1016/j.jpba.2017.04.045.
56. Avataneo V, Fanelli E, De Nicolò A, et al. A Non-Invasive Method for Detection of Antihypertensive Drugs in Biological Fluids: The Salivary Therapeutic Drug Monitoring. Front Pharmacol. 2022;12:755184. DOI:10.3389/fphar.2021.755184.
57. Sharma JR, Dludla PV, Dwivedi G, Johnson R. Measurement Tools and Utility of Hair Analysis for Screening Adherence to Antihypertensive Medication. Glob Heart. 2023;18(1):17. DOI:10.5334/gh.1191.
58. Osterberg L, Blaschke T. Adherence to medication. N Engl J Med. 2005;353(5):487- 97. DOI:10.1056/NEJMra050100.
59. Chung O, Vongpatanasin W, Bonaventura K, et al. Potential cost-effectiveness of therapeutic drug monitoring in patients with resistant hypertension. J Hypertens. 2014;32(12):2411-21; discussion 2421. DOI:10.1097/HJH.0000000000000346.
60. Nomura A, Tanigawa T, Kario K, Igarashi A. Cost-effectiveness of digital therapeutics for essential hypertension. Hypertens Res. 2022;45(10):1538-48. DOI:10.1038/s41440-022-00952-x.
61. Gupta P, Patel P, Štrauch B, et al. Biochemical Screening for Nonadherence Is Associated With Blood Pressure Reduction and Improvement in Adherence. Hypertension. 2017;70(5):1042-8. DOI:10.1161/HYPERTENSIONAHA.117.09631.
62. Lane D, Patel P, Khunti K, Gupta P. Objective measures of non-adherence in cardiometabolic diseases: a review focused on urine biochemical screening. Patient Prefer Adherence. 2019;13:537-47. DOI:10.2147/PPA.S162215.
63. Lane D, Lawson A, Burns A, et al.; Endorsed by the European Society of Hypertension (ESH) Working Group on Cardiovascular Pharmacotherapy and Adherence. Nonadherence in Hypertension: How to Develop and Implement Chemical Adherence Testing. Hypertension. 2022;79(1):12-23. DOI:10.1161/HYPERTENSIONAHA.121.17596.
64. Kichou B, Henine N, Himeur Y, et al. [Assessment of adherence to antihypertensive drugs in patients with resistant hypertension receiving optimal treatment]. Ann Cardiol Angeiol (Paris). 2019;68(4):264-8. (In French). DOI:10.1016/j.ancard.2019.07.002.
65. Zeijen VJM, Peeters LEJ, Asman A, et al. Quality-of-life and beliefs about medication in relation to a therapy adherence intervention in resistant hypertension: the Resistant HYpertension: MEasure to ReaCh Targets trial. J Hypertens. 2024;42(10):1687-94. DOI:10.1097/HJH.0000000000003780.
66. Punt AM, Stienstra NA, van Kleef MEA, et al. Screening of cardiovascular agents in plasma with LC-MS/MS: A valuable tool for objective drug adherence assessment. J Chromatogr B Analyt Technol Biomed Life Sci. 2019;1121:103-10. DOI:10.1016/j.jchromb.2019.05.013.
67. Sheppard JP, Albasri A, Gupta P, et al. Measuring adherence to antihypertensive medication using an objective test in older adults attending primary care: cross-sectional study. J Hum Hypertens. 2022;36(12):1106-12. DOI:10.1038/s41371-021-00646-w.
68. Lawson AJ, Hameed MA, Brown R, et al. Nonadherence to antihypertensive medications is related to pill burden in apparent treatment-resistant hypertensive individuals. J Hypertens. 2020;38(6):1165-73. DOI:10.1097/HJH.0000000000002398.
69. Daugherty SL, Powers JD, Magid DJ, et al. Incidence and prognosis of resistant hypertension in hypertensive patients. Circulation. 2012;125(13):1635-42. DOI:10.1161/CIRCULATIONAHA.111.068064.
70. Patel P, Gupta PK, White CM, et al. Screening for non-adherence to antihypertensive treatment as a part of the diagnostic pathway to renal denervation. J Hum Hypertens. 2016;30(6):368-73. DOI:10.1038/jhh.2015.103.
71. Velasco A, Chung O, Raza F, et al. Cost-Effectiveness of Therapeutic Drug Monitoring in Diagnosing Primary Aldosteronism in Patients With Resistant Hypertension. J Clin Hypertens (Greenwich). 2015;17(9):713-9. DOI:10.1111/jch.12570.
72. Höcht C, Bertera FM, Mayer MA, Taira CA. Issues in drug metabolism of major antihypertensive drugs: beta-blockers, calcium channel antagonists and angiotensin receptor blockers. Expert Opin Drug Metab Toxicol. 2010;6(2):199-211. DOI:10.1517/17425250903397381.
73. Родина Т.А., Мельников Е.С., Белков С.А. и др. Терапевтический лекарственный мониторинг нифедипина методом ВЭЖХ-МС/МС при лечении артериальной гипертензии. Биомедицина. 2017;(4):53-69]
74. Селезнев С.В., Якушин С.С., Мыльников П.Ю. и др. Терапевтический лекарственный мониторинг при неконтролируемой артериальной гипертензии: результаты пилотной части исследования. Российский медико-биологический вестник им. академика И.П. Павлова. 2023;31(2):195-202. DOI:10.17816/PAVLOVJ119880.
75. Choudhry NK, Kronish IM, Vongpatanasin W, et al.; American Heart Association Council on Hypertension; Council on Cardiovascular and Stroke Nursing; and Council on Clinical Cardiology. Medication Adherence and Blood Pressure Control: A Scientific Statement From the American Heart Association. Hypertension. 2022;79(1):e1-14. DOI:10.1161/HYP.0000000000000203.
76. Cramer JA, Scheyer RD, Mattson RH. Compliance declines between clinic visits. Arch Intern Med. 1990;150(7):1509-10. DOI:10.1001/archinte.1990.00390190143023.
77. Eskås PA, Heimark S, Eek Mariampillai J, et al. Adherence to medication and drug monitoring in apparent treatment-resistant hypertension. Blood Press. 2016;25(4):199-205. DOI:10.3109/08037051.2015.1121706.
78. Durand H, Hayes P, Harhen B, et al. Medication adherence for resistant hypertension: Assessing theoretical predictors of adherence using direct and indirect adherence measures. Br J Health Psychol. 2018;23(4):949-66. DOI:10.1111/bjhp.12332.
79. Linicus Y, Kindermann I, Helfer AG, et al. Witnessed drug intake before planned denervation--always harmless? Int J Cardiol. 2015;179:125-6. DOI:10.1016/j.ijcard.2014.10.162.
80. Halvorsen LV, Bergland OU, Søraas CL, et al. Nonadherence by Serum Drug Analyses in Resistant Hypertension: 7‐Year Follow‐Up of Patients Considered Adherent by Directly Observed Therapy. J Am Heart Assoc. 2022;11(18):e025879. DOI:10.1161/JAHA.121.025879.
81. Burnier M, Persu A, Azizi M, Prejbisz А. Patient perspectives on treatment adherence in hypertension: preliminary results of an ESH survey in five countries [abstract]. J Hypertens. 2022;40(Suppl 1):e61. DOI:10.1097/01.hjh.0000835756.15202.e5.
82. Лазебник Л.Б., Подкопаев Д.В., Комиссаренко И.А., Михеева О.М. Как повысить приверженность больных артериальной гипертензией к лечению? Артериальная гипертензия 2011;17(3):240-5] DOI: 10.18705/1607-419X-2011-17-3-240-245.
83. Burnier M, Prejbisz A, Weber T, et al. Hypertension healthcare professional beliefs and behaviour regarding patient medication adherence: a survey conducted among European Society of Hypertension Centres of Excellence. Blood Press. 2021;30(5):282-90. DOI:10.1080/08037051.2021.1963209.
Об авторах
М. В. ИоновРоссия
Ионов Михаил Васильевич
Санкт-Петербург
И. В. Емельянов
Россия
Емельянов Игорь Витальевич
Санкт-Петербург
А. О. Конради
Россия
Конради Александра Олеговна
Санкт-Петербург
Дополнительные файлы
Рецензия
Для цитирования:
Ионов М.В., Емельянов И.В., Конради А.О. Прямые методы оценки приверженности к антигипертензивной терапии: контролируемый прием препаратов и терапевтический лекарственный мониторинг. Рациональная Фармакотерапия в Кардиологии. 2025;21(3):234-243. https://doi.org/10.20996/1819-6446-2025-3192. EDN: TCNCNG
For citation:
Ionov M.V., Emelyanov I.V., Konradi A.O. Direct methods for assessing adherence to antihypertensive therapy: witnessed intake and therapeutic drug monitoring. Rational Pharmacotherapy in Cardiology. 2025;21(3):234-243. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3192. EDN: TCNCNG

















































