Перейти к:
Практика применения чрескожных коронарных вмешательств при остром коронарном синдроме без подъема сегмента ST (по данным регистра CONTRAST)
https://doi.org/10.20996/1819-6446-2025-3196
EDN: MUCPZC
Аннотация
Цель. Оценить реальную практику использования инвазивных методов диагностики и лечения у больных с острым коронарным синдромом без подъема сегмента ST(ОКСбпST) в рамках регистра регионального сосудистого центра.
Материал и методы. В исследование включены 136 пациентов, последовательно поступавших в сосудистый центр г. Сергиева Посада в экстренном порядке с октября 2018 г. по март 2019 г., с диагнозом ОКСбпST. Средний возраст составил 63±11 года, доля мужчин — 61%.
Результаты. Всем пациентам была выполнена коронарная ангиография (КАГ) в ближайшие сроки после поступления в стационар (<2 ч). Ни у одного из больных не выявлено абсолютных противопоказаний для проведения чрескожного коронарного вмешательства (ЧКВ). Все 136 пациентов в зависимости от выбранной тактики инвазивного лечения были разделены на 3 группы: пациенты, которым не было проведено ЧКВ на стационарном этапе лечения и при отдаленном наблюдении — 69 человек (50,7%; 1-я группа); пациенты, которым проведено ЧКВ во время текущей госпитализации — 50 человек (36,8%; 2-я группа); пациенты, которым проведено отсроченное ЧКВ после текущей госпитализации — 17 человек (12,5%; 3-я группа). На принятие решения о проведении ЧКВ не влияли клиническая картина заболевания и риск по шкале GRACE. У больных 3-й группы трехсосудистое поражение коронарных артерий (КА) по результатам КАГ встречалось существенно чаще, чем в 1 и 2 группах (59% vs 22% и 34%, р=0,001). Согласно результатам регрессионного анализа выявление поражения только одной КА многократно повышало вероятность выполнения ЧКВ. Эта вероятность прогрессивно уменьшалась по мере увеличения степени поражения КА.
Заключение. В региональном сосудистом центре у пациентов с диагнозом ОКСбпST ЧКВ в стационаре была проведена лишь 36% больных. При решении вопроса о проведении ЧКВ в первую очередь врачи руководствовались не столько степенью риска сердечно-сосудистых осложнений, как того требуют клинические рекомендации, сколько техническими возможностями процедуры и ее безопасностью.
Ключевые слова
Для цитирования:
Марцевич С.Ю., Калайджян Е.П., Загребельный А.В., Бородин А.Н., Кутишенко Н.П., Драпкина О.М. Практика применения чрескожных коронарных вмешательств при остром коронарном синдроме без подъема сегмента ST (по данным регистра CONTRAST). Рациональная Фармакотерапия в Кардиологии. 2025;21(3):226-233. https://doi.org/10.20996/1819-6446-2025-3196. EDN: MUCPZC
For citation:
Martsevich S.Yu., Кalaydzhyan E.P., Zagrebelnyi A.V., Borodin A.N., Kutishenko N.P., Drapkina O.M. Practice of percutaneous coronary interventions in non-ST-elevation acute coronary syndrome (based on the CONTRAST registry data). Rational Pharmacotherapy in Cardiology. 2025;21(3):226-233. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3196. EDN: MUCPZC
Введение
С конца ХХ века острый инфаркт миокарда (ИМ) стали подразделять на два типа — ИМ с подъемом сегмента ST (ИМпST) и ИМ без подъема сегмента ST (ИМбпST). Одновременно было введено понятие острого коронарного синдрома (ОКС) — промежуточного диагноза, устанавливающегося при поступлении больных, который также подразделялся на ОКС с подъемом сегмента ST (ОКСпST) и ОКС без подъема сегмента ST (ОКСбпST). Считается, что в основе двух этих видов ИМ лежат разные патологические механизмы. Поэтому и тактика их лечения существенно различается. В первую очередь это касаается проведения реперфузионной терапии и, в частности, чрескожного коронарного вмешательства (ЧКВ). Если в отношении ОКСпST необходимость немедленного проведения ЧКВ была очевидна с самого начала [1][2], то в отношении необходимости проведения ЧКВ (не только немедленного, но и отсроченного) при ОКСбпST долгое время ясности не было [3]. Начиная с начала 10-х гг. ХХI века, согласно клиническим рекомендациям для больных очень высокого и высокого риска, проведение ЧКВ однозначно показано, причем первым — в первые 2 ч после госпитализации, а последним — в течение 24 ч после госпитализации [4][5] Реальная клиническая практика демонстрирует, однако, что эти рекомендации соблюдаются далеко не всегда, а частота проведения ЧКВ при ОКСбпST значительно варьирует по данным разных исследований. Так, по данным федерального регистра ОКС, реваскуляризация миокарда не проводилась 63,7% больных с ОКСбпST. При этом противопоказания к проведению ЧКВ были указаны только в 9,5% историй болезни [6].
По данным Юго-Западного китайского регистра ЧКВ проводились у 61,3% больных ОКСбпST [7]. По данным когортного исследования, основанного на регистре, проводившегося в Норвегии в 2013-2018 гг., частота выполнения ЧКВ у больных нестабильной стенокардией составила 30%, а у больных с ИМбпST — 69% [8]. По данным регистра ОКСбпST, проводившегося в г. Кемерово, частота выполнения ЧКВ в стационаре составила 46,4% [9]. При этом во многих исследованиях не указывались конкретные сроки проведения ЧКВ. Ни в одной из названных выше работ не определяли основные мотивы выполнения или невыполнения ЧКВ при ОКСбпST.
Цель исследования — оценить реальную практику применения ЧКВ у больных, поступающих в региональный сосудистый центр с диагнозом ОКСбпST.
Материал и методы
В рамках проспективного исследования был проведен анализ выбора тактики инвазивного лечения у 136 пациентов, поступивших в сосудистый центр г. Сергиев Посад в экстренном порядке с октября 2018 по март 2019 гг., с диагнозом ОКСбпST (регистр CONTRAST). В исследование были включены мужчины и женщины любого возраста, поступившие в стационар с диагнозом ОКСбпST и подписавшие информированное согласие на обработку персональных данных и согласие на телефонный контакт при проспективном наблюдении, проживающие на территории Московской области или в г. Москве. Протокол исследования был утвержден независимым этическим комитетом Национального медицинского исследовательского центра терапии и профилактической медицины. Исследование было зарегистрировано на сайте ClinicalTrials.gov под номером NCT04490928.
У всех пациентов, кроме обычно выполняемых анализов (общий анализ крови, общий анализ мочи, биохимический анализ крови), был определен уровень кардиоспецифического маркера — тропонина I. Несмотря на это, результаты определения тропонина далеко не всегда оказывали влияние на принятие решения об инвазивной стратегии лечения, поскольку нередко они становились доступными лишь после осуществления ЧКВ. Оценка риска неблагоприятного исхода определялась при помощи шкалы GRACE (Global Registry of Acute Coronary Events). Окончательный диагноз (ИМбпST или нестабильная стенокардия) устанавливался после проведения КАГ и ЧКВ при выписке из стационара. Данные о заключительном диагнозе получали из историй болезни. Ни один из авторов исследования не принимал участие в постановке диагноза.
Степень поражения коронарных артерий (КА) определялась количеством пораженных сосудов: однососудистое, двухсосудистое или трехсосудистое поражение и степенью поражения >50%. Решение о необходимости и возможности проведения ЧКВ, а также об определении инфаркт-зависимой артерии и позиционировании стента принималось совместно врачом рентгеноваскулярной диагностики и кардиологом. Была возможность применять как непокрытые металлические стенты (BMS — Bare-Metal Stents), так и стенты, выделяющие лекарственный препарат (DES — Drug Eluting Stent). Была проанализирована лекарственная терапия, назначенная пациентам на стационарном этапе. Все 136 пациентов в зависимости от выбранной тактики инвазивного лечения были разделены на 3 группы.
Спустя пять лет после выписки пациентов из стационара проводилась оценка их жизненного статуса и анализ развития основных осложнений за прошедший период. Сбор информации осуществлялся посредством единой информационно-аналитической системы (ЕМИАС) или путем телефонного интервью с пациентом или его представителями (при летальном исходе). За указанный период времени показатель отклика достиг 100%. В ходе исследования фиксировались следующие события, произошедшие за пятилетний период: нефатальный ИМ, острое нарушение мозгового кровообращения, повторные госпитализации из-за сердечно-сосудистых заболеваний, повторные ЧКВ, аортокоронарное шунтирование, сердечно-сосудистая смертность, общая смертность и совокупность всех указанных событий. За первичную конечную точку принята общая смертность
Статистический анализ
Обработка данных проводилась при помощи статистического пакета IBM SPSS Statistics 26. Для качественных показателей определялись частоты (%). Различия по качественным признакам оценивались с помощью критерия χ2 Пирсона. При описании количественных показателей, имеющих нормальное распределение, проводился расчет средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ). В качестве количественной меры эффекта при сравнении относительных показателей использовался показатель отношения шансов (ОШ). Количественные показатели оценивались на предмет соответствия нормальному распределению, для этого использовался критерий Шапиро–Уилка (при числе исследуемых <50) или критерий Колмогорова–Смирнова (при числе исследуемых >50). При сравнении средних величин в нормально распределенных совокупностях количественных данных рассчитывался t-критерий Стьюдента. Статистически значимыми считались различия при уровне р <0,05. Построение прогностической модели вероятности проведения ЧКВ выполнялось при помощи метода бинарной логистической регрессии. Мерой определенности, указывающей на ту часть дисперсии, которая может быть объяснена с помощью логистической регрессии, в исследовании служил показатель Найджелкерка.
Результаты
Из 136 человек, включенных в регистр, 83 (61%) были мужчины, женщин было 53 (39%). Возраст пациентов — от 37 до 93 лет, среднее значение 63±11 года. Всем пациентам, включенным в исследование, была выполнена КАГ в ближайшие сроки после поступления в стационар (<2 ч). Ни у одного из больных, по данным медицинской документации, абсолютных противопоказаний для проведения ЧКВ выявлено не было. Если принималось решение о проведении ЧКВ во время текущей госпитализации, то у всех больных эта процедура была проведена непосредственно после КАГ, кроме одного, которому ЧКВ было выполнено на следующий день.
ЧКВ во время текущей госпитализации было проведено 50 больным (36,8%). Некоторым пациентам было рекомендовано проведение ЧКВ после выписки из стационара. Все 136 пациентов в зависимости от выбранной тактики инвазивного лечения были разделены на 3 группы: пациенты, которым не было проведено ЧКВ на стационарном этапе лечения и при отдаленном наблюдении — 69 человек (50,7%; 1-я группа); пациенты, которым проведено ЧКВ во время текущей госпитализации — 50 человек (36,8%; 2-я группа); пациенты, которым проведено отсроченное ЧКВ после текущей госпитализации — 17 человек (12,5%; 3-я группа) (рис. 1).
Показатели риска, оцененные по шкале GRACE, где низкий риск соответствует сумме баллов 108 и менее, умеренный риск соответствует диапазону от 109-140 баллов и высокий риск — 141 и более баллов, значимо не различались между выделенными группами (рис. 2). Основные клинико-демографические показатели, такие как пол, возраст, наличие сопутствующих заболеваний и прочие, сопоставленные между тремя группами больных, отражены в табл. 1.
При поступлении в стационар частота болевого синдрома в грудной клетке была сопоставимой у пациентов всех трех исследуемых групп, хотя несколько чаще она встречалась у больных 1-й группы (94,2% vs 82%,88/2%, р=0,11). Периферические отеки реже наблюдались у больных 2-й и 3-й групп, чем у пациентов 1-й группы (4% и 5,9% vs 21,7%, р=0,012). Анализ ЭКГ не выявил значимых различий между группами. Умеренное снижение фракции выброса левого желудочка статистически значимо чаще отмечалось у пациентов 2-й группы в сравнении с 1-й и 3-й группами (14% vs 1,4% и 11,8%, р=0,027). Повышение уровня тропонина I было зафиксировано практически у половины пациентов всех групп, однако чаще наблюдалось у пациентов 2-й группы (табл. 2). При выявлении периферических отеков, ЧКВ как правило не выполняли. В случае обнаружения зон гипокинезии, процедуру ЧКВ старались перенести на более поздний срок.
В табл. 3 представлена информация, отражающая назначение лекарственной терапии пациентам в условиях стационара. Следует отметить, что почти все пациенты трех групп получали двойную антиагрегантную терапию (91,3%, 100%, 88,2%, р=0,075), ингибиторы ренин-ангиотензин-альдостероновой системы (71%, 78%, 86,5%, р=0,674), бета-адреноблокаторы (92,8%, 86%, 76,5%, р=0,674) и статины (88,4%,94%,88,2%, р=0,56). Около трети пациентов получали блокаторы кальциевых каналов и непрямые оральные антикоагулянты. Примерно половине пациентов всех групп были назначены нитраты. По результатам КАГ у больных 3-й группы трехсосудистое поражение КА встречалось статистически значимо чаще, чем в 1-й и 2-й группах (59% vs 22% vs 34%, р=0,001). Во 2-й группе пациентов чаще встречалось однососудистое поражение. Отсутствие поражения КА было наиболее характерно для больных 1-й группы (рис. 3). Тем не менее в 1-й группе было 14% больных с одно- и двухсосудистым поражением КА и 22% больных с трехсосудистым поражением КА.
При выписке из стационара диагноз ИМбпST был установлен у 10,1% больных 1-й группы, 32% больных 2-й группы и 5,9% больных 3-й группы. Остальным больным при выписке из стационара был установлен диагноз нестабильной стенокардии. Чаще всего с диагнозом ИМбпST были выписаны пациенты из 2-й группы, а с диагнозом нестабильная стенокардия пациенты 1-й и 2-й групп (р=0,003).
При проведении регрессионного анализа с учетом поправки на пол и возраст пациентов было продемонстрировано, что перенесенный ранее ИМ (р=0,041), патологический зубец Т на ЭКГ (р=0,042), окклюзия инфаркт-зависимой КА (р=0,005) увеличивали шанс принятия решения о проведении ЧКВ (рис. 4). Однако в наибольшей степени выполнение ЧКВ ассоциировалось с поражением одной КА, по мере увеличения числа пораженных КА вероятность проведения ЧКВ значительно снижалась. Несмотря на то, что изолированно боль за грудиной не являлась определяющим условием для выполнения ЧКВ, ее наличие несколько уменьшало шанс проведения ЧКВ (р=0,042).
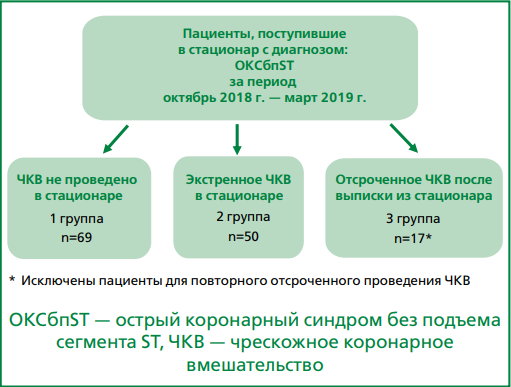
Рисунок 1. Схема по выбору тактики ведения пациентов, поступивших с диагнозом ОКСбпST.
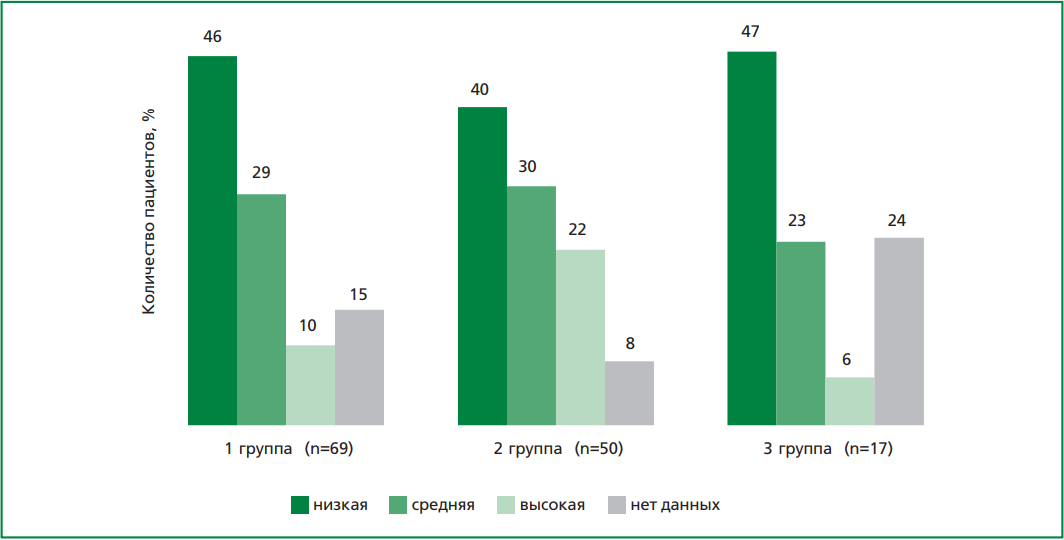
Рисунок 2. Сравнение пациентов трех групп по степени риска по шкале GRACE.
Таблица 1. Сравнительная характеристика пациентов трех групп по основным демографическим, клиническим и анамнестическим характеристикам и факторам риска
Фактор | 1-я группа n=69 | 2-я группа n=50 | 3-я группа n=17 | р-value |
Мужчины, n (%) Женщины, n (%) | 37 (53,6) 32 (46,4) | 33 (66) 17(34) | 13 (76,5) 4 (23,5) | 0,1481 |
Возраст, лет (M±SD) | 62,3±11,2 | 64±11 | 61,8±10,2 | 0,3992 |
Инвалидность, n (%) | 7 (10,1) | 1 (2) | 5 (29,4) | 0,0141 |
Курящие, n (%) | 8 (11,6) | 6 (12) | 1 (5,9) | 0,7671 |
АГ в анамнезе, n (%) | 68 (98,6) | 49 (98) | 17 (100) | 0,8391 |
СД 2 типа в анамнезе, n (%) | 7 (10,1) | 4 (8) | 2 (11,8) | 0,8761 |
ПИКС, n (%) | 18 (26,1) | 22 (44) | 10 (58,8) | 0,0181 |
ОНМК в анамнезе, n (%) | 8 (11,6) | 7 (14) | 2 (11,8) | 0,9221 |
КАГ в анамнезе, n (%) | 8 (11,6) | 17 (34) | 10 (58,8) | <0,0011 |
ЧКВ в анамнезе, n (%) | 6 (8,7) | 11 (22) | 6 (35,3) | 0,0161 |
ФП в анамнезе, n (%) | 9 (13) | 8 (16) | 3 (17,6) | 0,8451 |
АКШ в анамнезе, n (%) | 1 (1,4) | 2 (4) | 0 | 0,5191 |
1 χ² квадрат Пирсона, 2 t-критерий Стьюдента АГ — артериальная гипертензия, АКШ — аортокоронарное шунтирование, ДИ — доверительный интервал, КАГ — коронароангиография, ОНМК — острое нарушение мозгового кровообращения, ПИКС — постинфарктный кардиосклероз, СД — сахарный диабет, ФП — фибрилляция предсердий, ЧКВ — чрескожное коронарное вмешательство | ||||
Таблица 2. Сравнительная характеристика пациентов трех групп по данным, полученным при поступлении в стационар
Фактор | 1-я группа n=69 | 2-я группа n=50 | 3-я группа n=17 | р-value1 |
Боль за грудиной при поступлении, n (%) | 65 (94,2) | 41 (82) | 15 (88,2) | 0,11 |
Наличие одышки, n (%) | 32 (46,4) | 22 (44) | 7 (41,2) | 0,917 |
Отеки периферические, n (%) | 15 (21,7) | 2 (4) | 1 (5,9) | 0,012 |
Депрессия сегмента ST по ЭКГ, n (%) | 16 (23,2) | 16 (32) | 1 (5,9) | 0,091 |
Патологический зубец Т по ЭКГ, n (%) | 10 (14,5) | 12 (24) | 3 (17,6) | 0,416 |
Наличие зон гипокинеза, n (%) | 24 (34,8) | 20 (40) | 12 (70,6) | 0,026 |
Наличие зон акинеза, n (%) | 1 (1,4) | 3 (6) | 0 | 0,26 |
Сохранная ФВ (>50%), n (%) | 63 (91,3) | 39 (78) | 14 (82,4) | 0,121 |
Промежуточная ФВ (40-49٪), n (%) | 1 (1,4) | 7 (14) | 2 (11,8) | 0,027 |
Низкая ФВ (<40%), n (%) | 3 (4,3) | 3 (6) | 1 (5,9) | 0,912 |
Повышение тропонина I, n (%) | 36 (52,2) | 32 (64) | 8 (47,1) | 0,026 |
1 χ² Пирсона ФВ — фракция выброса, ЭКГ — электрокардиограмма | ||||
Таблица 3. Основные группы медикаментозной терапии, проводимой в стационаре для пациентов трех групп
Фактор | 1-я группа n=69 | 2-я группа n=50 | 3-я группа n=17 | р-value1 |
Двойная антиагрегантная терапия, n (%) | 63 (91,3) | 50 (100) | 15 (88,2) | 0,0751 |
АСК, n (%) | 67 (97,1) | 50 (100) | 15 (88,2) | 0,0461 |
Тикагрелор, n (%) | 8 (11,6) | 14 (28) | 2 (11,8) | 0,0541 |
Клопидогрел, n (%) | 61 (88,4) | 36 (72) | 15 (88,2) | 0,2851 |
Бета-адреноблокаторы, n (%) | 64 (92,8) | 43 (86) | 14 (82,4) | 0,331 |
иАПФ, n (%) | 49 (71) | 39 (78) | 13 (76,5) | 0,6741 |
Сартаны, n (%) | 5 (7,2) | 9 (18) | 4 (23,5) | 0,0951 |
БКК, n (%) | 31 (44,9) | 22 (44) | 5 (29,4) | 0,4961 |
Нитраты, n (%) | 44 (63,8) | 26 (52) | 10 (58,8) | 0,4371 |
Статины, n (%) | 61 (88,4) | 47 (94) | 15 (88,2) | 0,561 |
НОАК, n (%) | 32 (46,4) | 21 (42) | 7 (41,2) | 0,8641 |
1 χ² квадрат Пирсона АСК — ацетилсалициловая кислота, БКК — блокаторы кальциевых каналов, иАПФ — ингибиторы ангиотензинпревращающего фермента, НОАК — непрямые оральные антикоагулянты | ||||
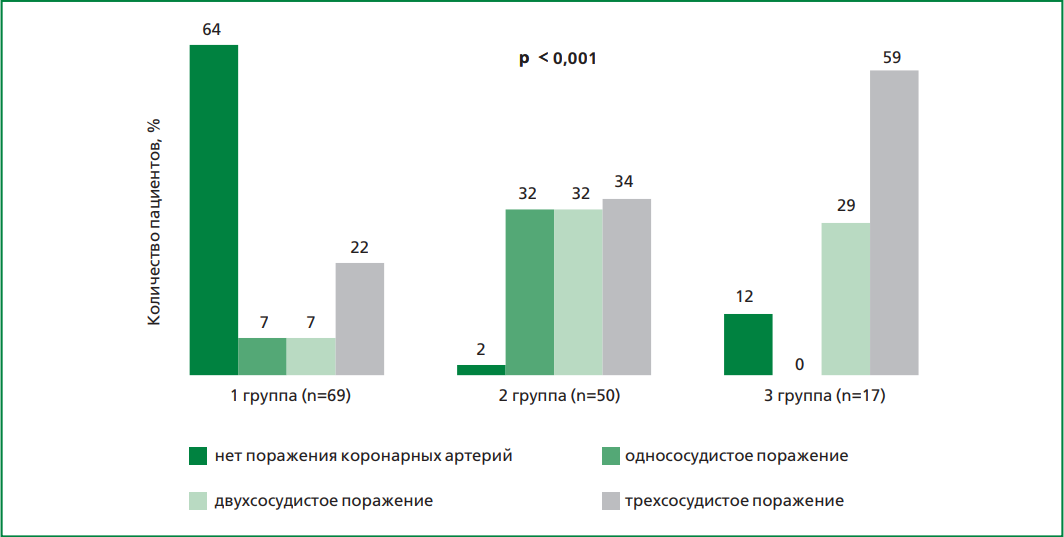
Рисунок 3. Сравнительная характеристика пациентов трех групп по типу поражения коронарного русла.
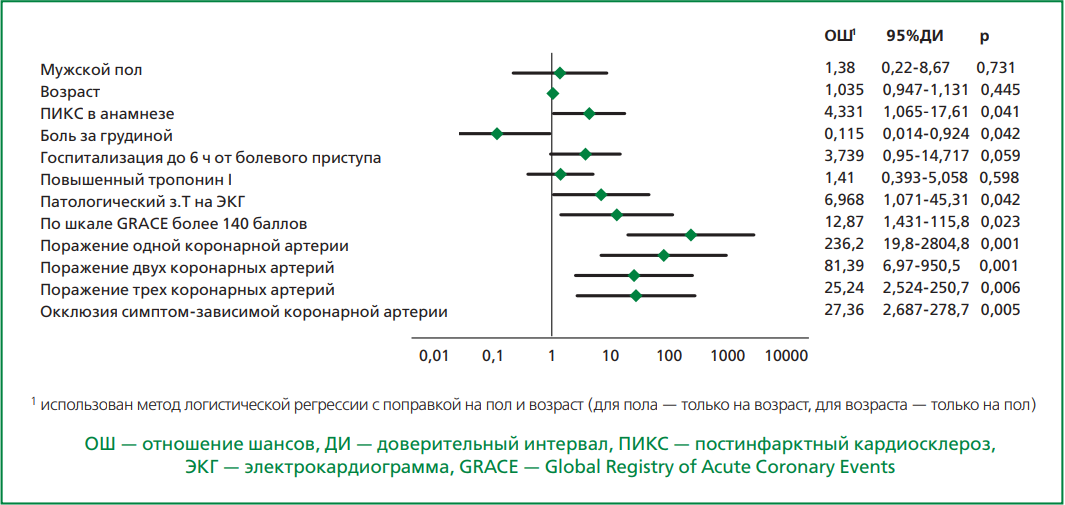
Рисунок 4. Факторы, ассоциированные с принятием решения о проведении ЧКВ.
Обсуждение
Настоящее исследование проводилось с соблюдением всех требований клинического регистра [10]. Для выполнения исследования был выбран типичный региональный сосудистый центр. Поэтому, несмотря на относительно небольшой объем выборки, полученные данные можно считать репрезентативными, по крайней мере, для Московской области. Примечательно, что всем без исключения больным в самое ближайшее время после поступления была проведена КАГ, хотя некоторым пациентам с низким риском осложнений, согласно современным клиническим рекомендациям, ее выполнение не было обязательным.
ЧКВ было проведено в общей сложности 36,8% больных. Примерно такая же частота выполнения ЧКВ при ИМбST приводится в современных клинических рекомендациях (37%) [11] и в ряде регистров ОКСбпST, о чем упоминалось выше. Обращает на себя внимание, что в регистре CONTRAST ЧКВ выполнено практически всем больным в самые ближайшие сроки после поступления, хотя в клинических рекомендациях, действовавших на момент проведения исследования, указана необходимость немедленного проведения ЧКВ только у больных с высоким риском сердечно-сосудистых осложнений, в частности у больных с риском по шкале GRACE >140 баллов [4]. Следует подчеркнуть, что у пациентов 3-й группы (с отсроченным проведением ЧКВ) в анамнезе статистически значимо чаще был ранее перенесённый ИМ (р=0,018) и выполненное ранее ЧКВ (р=0,016).
Работы по изучению факторов, влияющих на принятие решения о проведении ЧКВ при ОКСбпST, малочисленны. По данным недавно опубликованного исследования, основными предикторами выполнения ЧКВ у больных с нестабильной стенокардией были: выраженная ангинозная боль (отношение шансов 2,7, 95% ДИ 1,9-3,7), мужской пол (отношение шансов 1,4, 95% ДИ 1,1-1,7), и гиперлипидемия. При этом у многих больных очень высокого и высокого риска ЧКВ не было проведено [12]. Похожая ситуация выявлена и в настоящем исследовании. Парадоксально, но вопреки уже действовавшим на момент проведения исследования клиническим рекомендациям, риск, оцененный по шкале GRACE, оказывал минимальное влияние на решение о выполнении ЧКВ. Клиническая картина заболевания также практически не влияла на проведение ЧКВ, более того, сохраняющийся болевой синдром в настоящем исследовании оказался признаком в пользу невыполнения ЧКВ.
Решающую роль в принятии решения о проведении/непроведении ЧКВ играла ангиографическая картина, полученная в период текущей госпитализации. Выявление поражения только одной КА многократно повышало вероятность выполнения ЧКВ. Эта вероятность прогрессивно уменьшалась по мере увеличения степени поражения КА.
Пациентам всех трех групп назначались основные классы препаратов, необходимые, согласно современным клиническим рекомендациям, для улучшения отдаленных исходов заболевания. При этом соотношение назначения этих классов лекарств было приблизительно равнозначным в каждой группе.
Таким образом, значительной части больных с самым высоким риском сердечно-сосудистых осложнений, по данным настоящего исследования, ЧКВ не было проведено. Выше уже было отмечено, что меньшая вероятность проведения ЧКВ при ОКСбпST у больных высокого риска была отмечена и в ряде зарубежных исследований. Так, B.S. Case и соавт. отметили, что наличие ранее перенесенного ИМ, ранее проведенная реваскуляризация и ряд других прогностически неблагоприятных факторов снижали вероятность проведения ЧКВ при ОКСбпST [13]. Похожие данные были выявлены и в исследовании H. С. Wijeysundera и соавт. [14]. Дальнейшее проспективное наблюдение включенных в регистр CONTRAST больных позволит оценить, как подобная тактика повлияла на отдаленные исходы заболевания.
Ограничения исследования
Обследованная когорта больных являлась относительно небольшой. Однако это компенсируется высоким уровнем соблюдения протокола, соответствием всем стандартам ведения регистра, а также репрезентативностью выбранного специализированного сосудистого центра. Данные были получены в начале функционирования сосудистого центра, поэтому представляется крайне необходимым проводить аналогичные исследования в настоящее время.
Заключение
В региональном сосудистом центре при поступлении в стационар больных с диагнозом ОКСбпST всем без исключения больным в ближайшие сроки была проведена КАГ. Однако ЧКВ в стационаре была проведена лишь 36% больных. Проведенный анализ позволяет предположить, что врачи, решая вопрос о проведении ЧКВ, в первую очередь руководствовались не столько степенью риска сердечно-сосудистых осложнений, как того требуют клинические рекомендации, сколько техническими возможностями процедуры и ее безопасностью. В результате достаточно большой доле больных с очень высоким и высоким риском ЧКВ не была проведена в надлежащие сроки, либо была отсрочена.
Список литературы
1. Grines CL, Browne KF, Marco J, et al. A comparison of immediate angioplasty with thrombolytic therapy for acute myocardial infarction. The Primary Angioplasty in Myocardial Infarction Study Group. N Engl J Med. 1993;328(10):673-9. DOI:10.1056/NEJM199303113281001.
2. Huynh T, Perron S, O’Loughlin J, et al. Comparison of primary percutaneous coronary intervention and fibrinolytic therapy in ST-segment-elevation myocardial infarction: bayesian hierarchical meta-analyses of randomized controlled trials and observational studies. Circulation. 2009;119(24):3101-9. DOI:10.1161/CIRCULATIONAHA.108.793745.
3. Hall M, Dondo TB, Yan AT, et al. Association of Clinical Factors and Therapeutic Strategies With Improvements in Survival Following Non-ST-Elevation Myocardial Infarction, 2003-2013. JAMA. 2016;316(10):1073-82. DOI:10.1001/jama.2016.10766.
4. Roffi M, Patrono C, Collet JP, et al.; ESC Scientific Document Group. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). Eur Heart J. 2016;37(3):267-315. DOI:10.1093/eurheartj/ehv320.
5. Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC Guideline for the Management of Patients with Non-ST-Elevation Acute Coronary Syndromes: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2014;64(24):e139-228. DOI:10.1016/j.jacc.2014.09.017. Erratum in: J Am Coll Cardiol. 2014;64(24):2713- 4. Dosage error in article text.
6. Сагайдак О.В., Ощепкова Е.В., Попова Ю.В. и др. Анализ оказания медицинской помощи больным с острым коронарным синдромом в 2019 году (по данным федерального регистра острого коронарного синдрома). Кардиологический вестник. 2020;(3):37-45. DOI:10.36396/MS.2020.16.3.005
7. Li SY, Zhou MG, Ye T. Frequency of ST-segment elevation myocardial infarction, non-ST-segment myocardial infarction, and unstable angina: Results from a Southwest Chinese Registry. Rev Cardiovasc Med. 2021;22(1):239-45. DOI:10.31083/j.rcm.2021.01.103.
8. Fladseth K, Wilsgaard T, Lindekleiv H, et al. Outcomes after coronary angiography for unstable angina compared to stable angina, myocardial infarction and an asymptomatic general population. Int J Cardiol Hear Vasc. 2022;42:101099. DOI:10.1016/j.ijcha.2022.101099.
9. Бернс С.А., Шмидт Е.А., Нагирняк О.А. и др. Оценка исходов и тактики лечения пациентов с острым коронарным синдромом без подъема сегмента ST по данным 5летнего наблюдения. Кардиология. 2018;58(7):32-40. DOI:10.18087/cardio.2018.7.10141.
10. Марцевич С. Ю., Лукина Ю. В., Кутишенко Н. П. и др. Медицинские регистры. Роль в доказательной медицине. Рекомендации по созданию. Методические рекомендации. М.: ООО «Силицея- Полиграф”. 2023. ISBN: 9785-6049087-8-5. DOI:10.15829/ROPNIZ-m1-2023.
11. Аверков О.В., Арутюнян Г.К., Дупляков Д.В. и др. Острый коронарный синдром без подъема сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025;30(5):6319. DOI:10.15829/1560-4071-2025-6319. EDN: CXJUIB.
12. Budzianowski J, Faron W, Rzeźniczak J, et al. Predictors of Revascularization in Patients with Unstable Angina. J Clin Med. 2024;13(4):1096. DOI:10.3390/jcm13041096.
13. Case BC, Weintraub WS. Non-ST-Segment-Elevation Myocardial Infarction: When Is Rapid Revascularization Critical? J Am Heart Assoc. 2021;10(19):e023645. DOI:10.1161/JAHA.121.023645.
14. Wijeysundera HC, Sidhu MS, Bennell MC, et al. Predictors of Initial Revascularization Versus Medical Therapy Alone in Patients With NonST-Segment-Elevation Acute Coronary Syndrome Undergoing an Invasive Strategy. Circ Cardiovasc Interv. 2016;9(7):e003592. DOI:10.1161/CIRCINTERVENTIONS.115.003592.
Об авторах
С. Ю. МарцевичРоссия
Марцевич Сергей Юрьевич
Москва
Е. П. Калайджян
Россия
Калайджян Елена Петровна
Москва
А. В. Загребельный
Россия
Загребельный Александр Васильевич
Москва
А. Н. Бородин
Россия
Бородин Антон Николаевич
Сергиев Посад
Н. П. Кутишенко
Россия
Кутишенко Наталья Петровна
Москва
О. М. Драпкина
Россия
Драпкина Оксана Михайловна
Москва
Рецензия
Для цитирования:
Марцевич С.Ю., Калайджян Е.П., Загребельный А.В., Бородин А.Н., Кутишенко Н.П., Драпкина О.М. Практика применения чрескожных коронарных вмешательств при остром коронарном синдроме без подъема сегмента ST (по данным регистра CONTRAST). Рациональная Фармакотерапия в Кардиологии. 2025;21(3):226-233. https://doi.org/10.20996/1819-6446-2025-3196. EDN: MUCPZC
For citation:
Martsevich S.Yu., Кalaydzhyan E.P., Zagrebelnyi A.V., Borodin A.N., Kutishenko N.P., Drapkina O.M. Practice of percutaneous coronary interventions in non-ST-elevation acute coronary syndrome (based on the CONTRAST registry data). Rational Pharmacotherapy in Cardiology. 2025;21(3):226-233. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3196. EDN: MUCPZC

















































