ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Цель. Оценить и сравнить диагностическую эффективность модели предтестовой вероятности (ПТВ) Европейского общества кардиологов (ЕОК) 2019 г. с вариантами базовой и клинической модели консорциума Coronary Artery Disease (CAD) в предсказании обструктивной ишемической болезни сердца (ИБС).
Материал и методы. В одномоментное исследование включены 366 пациентов (средний возраст — 64,8 года, мужчин — 62,6%) с подозрением на стабильную стенокардию, которым была выполнена компьютерная томографическая ангиография коронарных артерий сердца. Обструктивная ИБС определялась при наличии стеноза ≥50% в сегментах эпикардиальных коронарных артерий диаметром ≥2,5 мм. Оценивали клинические характеристики и сердечно-сосудистые факторы риска. Значения ПТВ вычисляли для каждой из трех моделей, а их диагностическую эффективность оценивали с использованием площади под ROC-кривой (AUC, area under the curve) и теста Хосмера—Лемешоу для калибровки. Также проанализированы чувствительность, специфичность и прогностическая ценность.
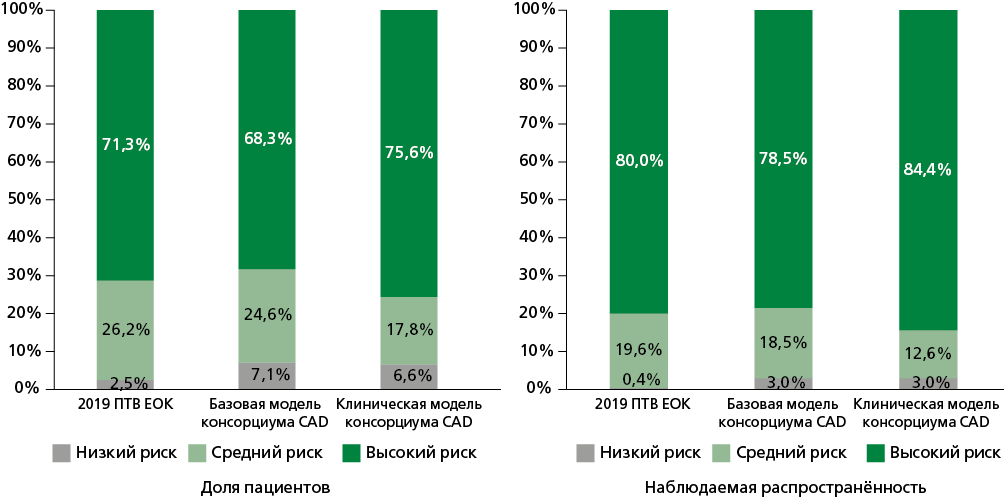
Результаты. Обструктивная ИБС выявлена у 270 (73,8%) пациентов, среди которых мужской пол, артериальная гипертензия, дислипидемия, курение, типичная и атипичная стенокардия встречались статистически значимо чаще (все p<0,05). Клиническая модель консорциума CAD обеспечила наиболее точную оценку распространённости обструктивной ИБС у пациентов высокого риска (76,6% ожидаемых vs 84,4% подтверждённых случаев), в то время как модель 2019 ПТВ ЕОК была более точна в группе низкого риска (2,5% ожидаемых vs 0,4% подтверждённых случаев). Клиническая модель консорциума CAD продемонстрировала лучшую предсказательную диагностическую ценность с AUC 0,760 и хорошей калибровкой (тест Хосмера—Лемешоу, p=0,823). Базовая модель консорциума CAD (AUC=0,755) заняла промежуточное место, а модель 2019 ПТВ ЕОК продемонстрировала наименьшую предсказательную ценность (AUC=0,701, плохая калибровка, p=0,001). Клиническая модель консорциума CAD с пороговым значением >33% имела чувствительность 66,7%, специфичность — 79,2%, положительная прогностическая ценность — 90% и отрицательная прогностическая ценность — 45,8% для предсказания обструктивной ИБС.
Заключение. Клиническая модель консорциума CAD продемонстрировала наиболее высокую точность в предсказании обструктивной ИБС у пациентов со стабильной стенокардией, особенно в группе высокого риска, по сравнению с моделью 2019 ПТВ ЕОК и базовой моделью консорциума CAD. Высокая диагностическая ценность и надежная калибровка делают её наиболее предпочтительным инструментом для оценки риска обструктивной ИБС.
Цель. Провести анализ индивидуальной зависимости распространённости, осведомлённости, лечения и контроля артериальной гипертонии (АГ) от региональных характеристик в рамках национального эпидемиологического исследования ЭССЕ-РФ в 2012-2022 гг. с оценкой влияния пандемии новой коронавирусной инфекции (COronaVIrus Disease 2019, COVID-19).
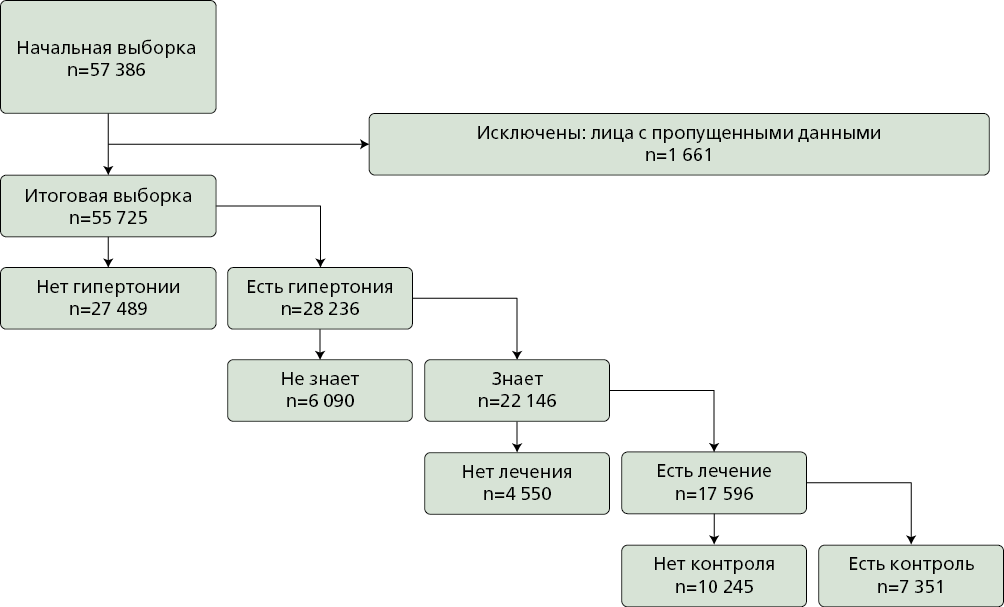
Материал и методы. Для анализа использовали объединённые данные исследования ЭССЕ-РФ в три временных периода: ЭССЕ-РФ-1 в 2012-2014 гг., ЭССЕ-РФ-2 в 2017-2018 гг., ЭССЕ-РФ-3 в 2020-2022 гг. Итоговая аналитическая выборка за все три временных среза составила 55 725 мужчин и женщин в возрасте 25-74 лет. В качестве исследуемых индивидуальных исходов рассматривали наличие, осведомлённость, лечение и контроль АГ. Региональные условия проживания оценивали с помощью "Экономического", "Демографического", "Промышленного" и "Социального" индексов по данным "НМИЦ терапии и профилактической медицины". Статистический анализ проведён с использованием обобщённых оценочных уравнений (логистические регрессионные модели) с расчётом отношений шансов (ОШ) и 95% доверительных интервалов (ДИ). Для оценки влияния пандемии COVID-19 на ассоциации региональных условий проживания с распространённостью, осведомлённостью, лечением и контролем АГ, проведён раздельный анализ в выборках ЭССЕ-РФ-1 2012-2014 гг. и ЭССЕ-РФ-3 2020-2022 гг.
Результаты. Улучшение социальных условий проживания сопровождается снижением вероятности АГ (ОШ=0,90; 95% ДИ 0,85-0,95), увеличением лечения (ОШ=1,13; 95% ДИ 1,02-1,25) и контроля (ОШ=1,11; 95% ДИ 1,01-1,22) АГ. Смещение демографической структуры регионов в сторону более молодого возраста ассоциируется со снижением вероятности АГ (ОШ=0,83; 95% ДИ 0,76-0,91). При росте промышленной развитости регионов снижается лечение АГ (ОШ=0,87; 95% 0,80-0,96). По сравнению с полом, возрастом и ожирением, региональные индексы вносят значительно меньший вклад в изучаемые исходы. Тем не менее вклад региональных условий проживания сопоставим с такими индивидуальными предикторами, как уровень образования и дохода, городское/сельское проживание. Наблюдаются существенные различия по ассоциациям региональных индексов с лечением и контролем АГ в выборках допандемийного (наличие множественных ассоциаций) и пандемийного (ассоциации практически отсутствуют) периодов исследования.
Заключение. Подтверждена ассоциация распространённости, лечения и контроля АГ с региональными условиями проживания. Снижение силы или даже инверсия ассоциаций региональных характеристик с лечением и контролем АГ в период COVID-19 подтверждает значимость пандемии как мощного фактора изменений в индивидуальном и популяционном поведении человека в отношении своего здоровья.
Цель. Оценить эффективность и безопасность применения кавутилида у пациентов с безуспешным опытом купирования текущего эпизода фибрилляции предсердий персистирующего и пароксизмального течения.
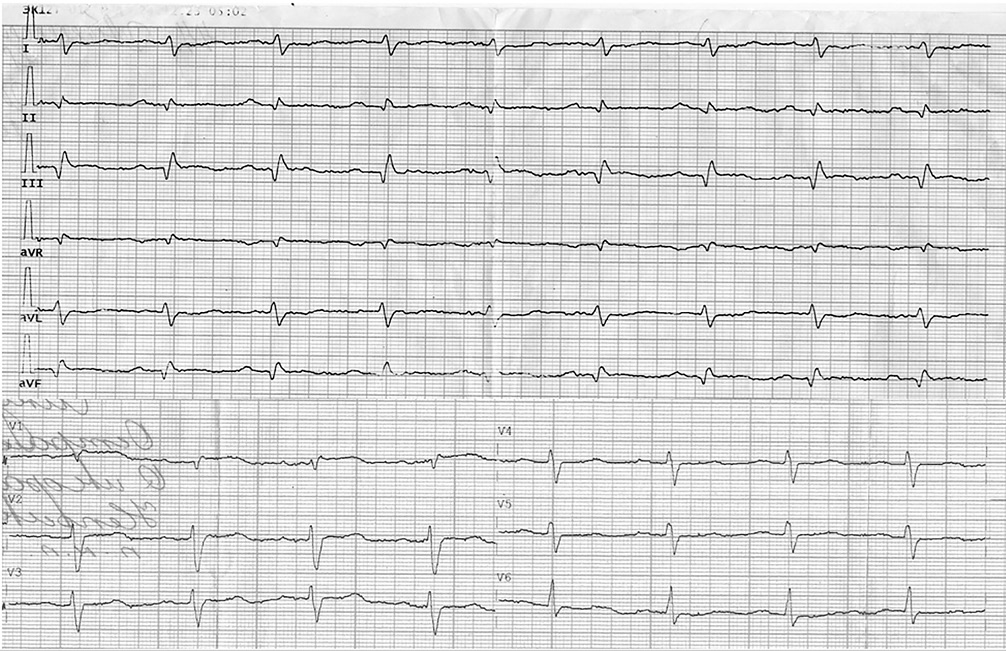
Материал и методы. В ретроспективное исследование включены 55 пациентов (средний возраст 60±8 лет, соотношение мужчин и женщин — 37 и 18 соответственно) с пароксизмальной (n=15) и персистирующей (n=40) формами фибрилляции предсердий, имеющие безуспешный опыт купирования текущего эпизода аритмии путем электроимпульсной терапии (ЭИТ). Всем пациентам в условиях блока интенсивной терапии вводился кавутилид по схеме: 5 мкг/кг-5 мкг/кг-10 мкг/кг-10 мкг/кг. После введения каждого болюса и перед введением последующего проводилась оценка параметров электрокардиограммы (ритм, интервал QT) и общего состояния, интервал между введениями составлял 15 мин. Дальнейшее введение прекращалось на любом из этапов в случае: восстановления синусового ритма (СР); снижения частоты сердечных сокращений менее 50 уд./мин; удлинения интервала QTс >500 мс; развития аритмогенного действия препарата. В течение 24 ч пациент находился под телеметрическим наблюдением для оценки эффективности и безопасности терапии.
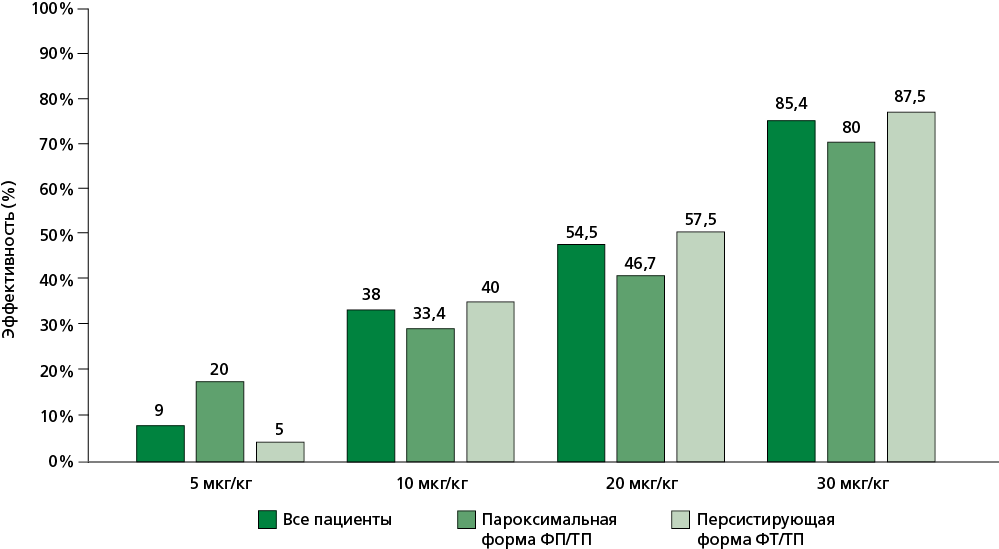
Результаты. У 47 (85,4%) пациентов из 55 отмечено восстановление СР после введения кавутилида. Медиана времени достижения СР составила 40 [15240] мин. У 5 (9%) из 47 пациентов восстановление СР произошло после введения кавутилида в начальной дозе 5 мкг/кг. После введения кавутилида в дозе 10 мкг/кг СР восстановился ещё у 16 пациентов. Суммарная эффективность кавутилида в дозе 10 мкг/кг составила 38%. Оставшиеся пациенты получили кавутилид в дозе 20 мкг/кг — СР восстановился ещё у 9 больных (эффективность дозы 20 мкг/кг — 54,5%). Остальным больным потребовалось введение кавутилида в максимальной дозе 30 мкг/кг. У 12 (15%) больных отмечалось удлинение интервала QTc >500 мс, но ни в одном из случаев это не сопровождалось устойчивым желудочковым аритмогенным действием. У 4 (7,2%) из 55 пациентов в момент купирования аритмии наблюдалось кратковременное урежение частоты сердечных сокращений <50 уд./мин.
Заключение. Кавутилид обладает высокой эффективностью и безопасностью восстановления СР у пациентов с безуспешным опытом применения ЭИТ. Представленный опыт эффективного и безопасного использования кавутилида указывает на целесообразность рассмотрения возможности медикаментозной кардиоверсии данным лекарственным препаратом у пациентов после неэффективной попытки ЭИТ.
Цель. Изучить влияние статинотерапии разной интенсивности на андрогенный статус и эректильную функцию (ЭФ) у мужчин в возрасте 40-65 лет с высоким и очень высоким сердечно-сосудистым риском, а также оценить связь между уровнем половых гормонов, показателями ЭФ и традиционными факторами риска сердечно-сосудистых заболеваний, жёсткостью артерий и эндотелиальной функцией у этой категории пациентов.
Материал и методы. Планируется проведение проспективного рандомизированного контролируемого исследования с включением 150 пациентов мужского пола 40-65 лет, проходивших плановые профилактические осмотры в Медицинском научно-образовательном институте Московского государственного университета им. М. В. Ломоносова и имеющих высокий и очень высокий риск сердечно-сосудистых заболеваний. В I группе (n=75) пациенты будут получать питавастатин в стартовой дозе 1 мг/сут., во II группе (n=75) — розувастатин 20 мг/сут. Через 3 мес. запланирован контроль биохимических параметров, при необходимости титрация дозы питавастатина до 2-4 мг/сут. и/или розувастатина до 40 мг/сут. Набор в исследование будет проходить в течение 9 мес. в одном исследовательском центре. Наблюдение пациентов с объективной оценкой параметров ЭФ, анализа крови (в том числе андрогенного статуса), жёсткости магистральных сосудов, эндотелиальной функции будет проводиться в течение 6 мес. с момента включения. Контрольные визиты предусмотрены через 1, 3 и 6 мес.
Результаты. Предполагаемый результат проверки исследовательской гипотезы — статинотерапия не будет оказывать негативного влияния на андрогенный статус и ЭФ у мужчин. Интенсивная статинотерапия будет оказывать большее положительное влияние на эндотелиальную функцию, что может привести к улучшению ЭФ мужчин.
Заключение. Исследование планировалось с предположением, что статинотерапия не будет оказывать негативного влияния на андрогенный статус и ЭФ у мужчин в возрасте 40-65 лет. Также предполагается, что положительное влияние статинов на эндотелиальную функцию и жёсткость сосудов может привести к улучшению ЭФ мужчин с высоким и очень высоким сердечно-сосудистым риском. В случае подтверждения гипотезы полученные результаты будут способствовать улучшению приверженности лечению статинами пациентов мужского пола и, как следствие, повышению эффективности профилактики сердечно-сосудистых событий.
Цель. Изучить взаимосвязь между уровнями липопротеина(а) (Лп(а)), фактора роста эндотелия сосудов (VEGF), трансформирующего фактора роста β (TGF-β) в плазме крови, и возникновением рестеноза стента после чрескожного коронарного вмешательства у пациентов с ишемической болезнью сердца (ИБС), а также достижением целевого уровня холестерина липопротеинов низкой плотности (ХС ЛНП) на фоне гиполипидемической терапии.
Материал и методы. В проспективное наблюдение включены 92 пациента (средний возраст составил 64,0 года, 79,5% мужчины, 20,5% женщины) с диагнозом острого коронарного синдрома (ОКС), которым установили стенты в клинически значимую или инфаркт-связанную коронарную артерию. Одновременно визуально в процессе селективной коронарографии определяли кровоток в остальных коронарных артериях. При гемодинамически значимом стенозе коронарной артерии, не связанной с ОКС, на 70-90% больного приглашали на консультацию к кардиологу через 1 мес. с целью решения вопроса о реваскуляризации миокарда через нагрузочное тестирование с учётом клинического статуса пациента (жалоб). В случае необходимости повторной селективной коронарографии с лечебной целью через 1-2 мес. у пациентов визуализировали формирование неоинтимы, уточняли степень рестеноза внутри стента, ранее установленного в инфаркт-связанной артерии в сочетании с определением в плазме крови Лп(а), VEGF, TGF-β. Оценивали достижение целевого уровня ХС ЛНП на фоне гиполипидемической терапии. Пациенты были разделены на 2 группы: с выявленным рестенозом или неоинтимой (n=49) и без рестеноза (n=43). В группах сравнивали полученные клинико-лабораторные и ангиографические данные.
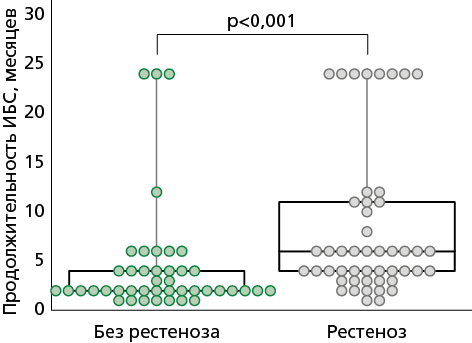
Результаты. Развитие рестеноза связано с продолжительным течением ИБС на протяжении 6,0 (4,0; 11,0) мес. (p<0,001), стабильной ИБС в 42,86% случаев (p=0,01), хронической болезнью почек 3А — 32,65% (p=0,02) и применением стента BMS (bare-metal stent) — 79,59% (n=39) (p<0,001), уровнем Лп(а) >30 мг/дл — 36,73% (p=0,01). При исследовании сочетаний двух комбинаций TGF-β + Лп(а) и Лп(а) + VEGF выявлено, что нахождение в границах нормативных значений обоих указанных показателей одновременно является протективным фактором относительно развития рестеноза — отношение шансов=0,2 [95% доверительный интервал 0,07-0,56] и отношение шансов=0,33 [95% доверительный интервал 0,14-0,82], соответственно.
Заключение. У пациентов с ИБС через 1-2 мес. после чрескожного коронарного вмешательства на фоне ОКС развитие рестеноза ассоциировано с продолжительным течением ИБС, хронической болезнью почек 3А и типом стента BMS, повышенным уровнем Лп(а) >30 мг/дл, независимо от достижения целевого уровня ХС ЛПН <1,4 ммоль/л. Увеличение значений исходного Лп(а) в комбинации с показателями VEGF и TGF-β в плазме крови указывает на высокий риск рестеноза стента, что может быть новыми биомаркерами для прогнозирования прогрессирования ИБС. Эти результаты подтверждают необходимость разработки практических рекомендаций по динамическому наблюдению данной группы пациентов.
СТРАНИЦЫ НАЦИОНАЛЬНОГО ОБЩЕСТВА ДОКАЗАТЕЛЬНОЙ ФАРМАКОТЕРАПИИ
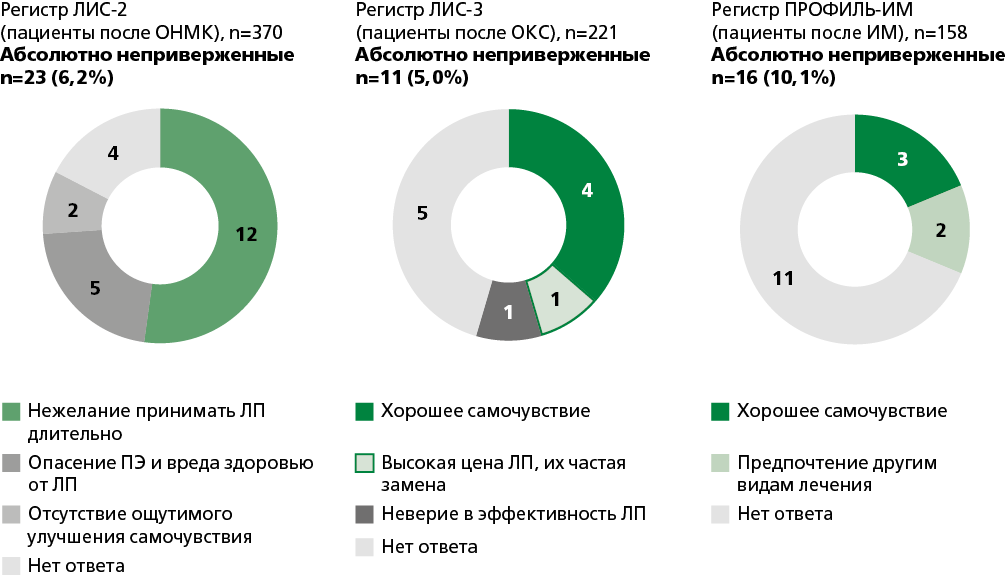
В статье рассматриваются проблемы отказа от медикаментозного лечения. Приводятся немногочисленные данные литературы, касающиеся клинической значимости отказа от лечения больных с заболеваниями внутренних органов. Зарубежные оригинальные исследования, посвящённые проблемам отказа от лечения у больных с хроническими неинфекционными заболеваниями, в частности у пациентов с сердечно-сосудистыми болезнями, единичны. В большинстве этих исследований изучается не только отказ от приёма лекарственных препаратов (ЛП), но и отказ от конкретных лечебных процедур, а также причины этого отказа. Проводится анализ российских проспективных клинических регистров сердечно-сосудистых заболеваний, в которых оказалось возможным зафиксировать факт полного отказа от медикаментозной терапии или феномен абсолютной неприверженности. Частота полного отказа от лечения колебалась от 1 до 10,1%. Ведущими причинами полного отказа от приёма ЛП были хорошее самочувствие, нежелание длительно принимать лекарства, высокая стоимость лечения. Продемонстрировано, что полный отказ от терапии может отрицательно повлиять на исходы болезни. Таким образом, определённая часть больных с сердечно-сосудистыми заболеваниями полностью отказывается от лечения, несмотря на рекомендации. Частично это может объясняться хорошим самочувствием больных. Также характерную роль, по-видимому, играет и плохая информированность больных об эффективности назначенных ЛП. Следовательно, перспективным способом профилактики феномена абсолютной неприверженности у пациентов с хроническими неинфекционными заболеваниями является их регулярное наблюдение и информирование, что назначенная терапия способна не только устранять симптомы заболевания, но и улучшать его прогноз, снижать риск осложнений.
АКТУАЛЬНЫЕ ВОПРОСЫ КЛИНИЧЕСКОЙ ФАРМАКОЛОГИИ
Цель. Оценить особенности приема антикоагулянтной терапии (АКТ) у пациентов с кардиоэмболическим (КЭ) подтипом ишемического инсульта (ИИ) и фибрилляцией предсердий (ФП), госпитализированных в сосудистый центр.
Материал и методы. Проведено одномоментное исследование на базе сосудистого центра ГБУЗ "ММНКЦ им. С. П. Боткина" г. Москвы с апреля 2022 г. по апрель 2023 г. В исследование включены пациенты старше 18 лет с подтвержденным КЭ подтипом ИИ и ФП, поступившие в течение первых 12 ч от начала симптомов и принимавшие антикоагулянты более 1 мес. до госпитализации. Не включались пациенты с геморрагическим и другими, кроме КЭ, подтипами ИИ, отсутствием данных о приеме антикоагулянтов или отказавшиеся от участия в исследовании.
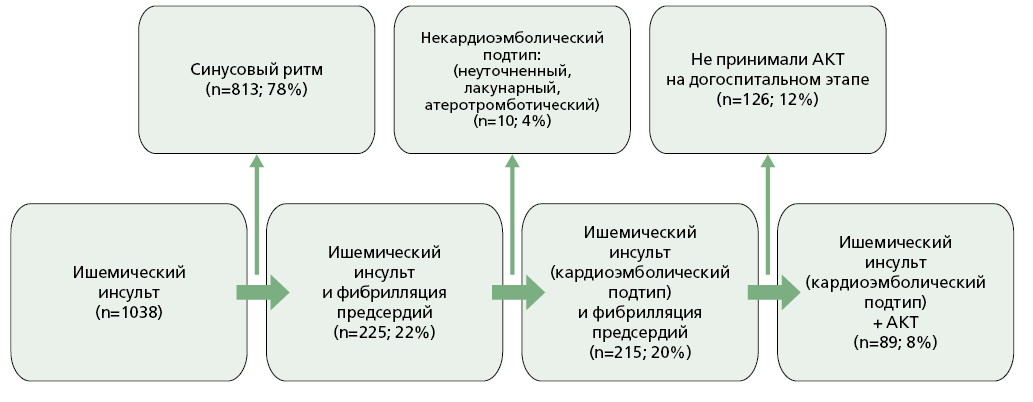
Результаты. Из 1038 пациентов с ИИ у 215 (20,7%) выявлен КЭ подтип на фоне ФП. Более половины из них (109 человек) не принимали АКТ на момент ИИ. В исследование включены 106 пациентов, принимавших антикоагулянты на амбулаторном этапе: ривароксабан (n=56), апиксабан (n=30), дабигатрана этексилат (n=11), варфарин (n=9). Средний возраст пациентов составил 77,8 лет, средний балл по шкале CHA2DS2-VASc — 6. У 33,9% больных дозы прямых пероральных антикоагулянтов не соответствовали клиническим рекомендациям (например, выявлено необоснованное снижение дозы ривароксабана и апиксабана). Средняя оценка тяжести инсульта по шкале NIHSS составила 7 баллов, госпитальная летальность достигла 30,2%. Высокая смертность связана с тяжёлым течением инсульта (у половины пациентов >8 баллов по NIHSS) и высокой частотой коморбидных состояний: гипертоническая болезнь — 95,2% случаев, хроническая сердечная недостаточность — 60,4%, сахарный диабет 2 типа — 30,1%, перенесённый инфаркт миокарда — 37,7%.
Заключение. Высокая частота ИИ на фоне проводимой АКТ подчёркивает необходимость рутинного мониторинга концентрации прямых пероральных антикоагулянтов в крови, регулярной оценки приверженности лечению и систематического информирования пациентов и их родственников о важности соблюдения режима приёма препаратов.
Цель. На основе оценки физико-химических свойств комплексных соединений магния и экспериментов с изолированными предсердными кардиомиоцитами крысы выявить наиболее перспективный состав лекарственного препарата, влияющий на восполнение внутриклеточного дефицита магния.
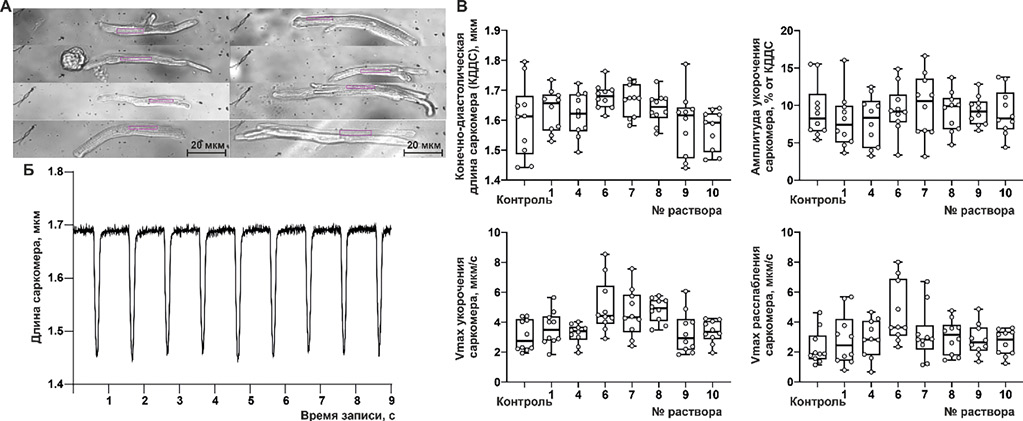
Материалы и методы. Проводились оценка осмоляльности растворов, содержащих комплексные соединения магния, их экстракция в органические растворители разной полярности (хлороформ и бутанол), а также определение диффузии через модель клеточной мембраны (бумажный фильтр, модифицированный лецитином). В экспериментах на изолированных предсердных кардиомиоцитах крысы проведено тестирование составов на восполнение внутриклеточного (цитозольного) дефицита магния с применением методов лазерной сканирующей (конфокальной) микроскопии.
Результаты. Исходя из экспериментальных данных, полученных в ходе физико-химического тестирования препаратов магния и опытов, проведённых на кардиомиоцитах лабораторных животных, наиболее перспективным в отношении восполнения внутриклеточного магния оказалась система на основе аспарагината магния, в которой соотношение ионов магния к аспарагиновой кислоте составляет 1 к 2,5. 30-мин инкубация кардиомиоцитов с данным препаратом приводила к повышению цитозольного [Mg2+]i на 115% относительно значений контрольного уровня. Удаление избытка ионов калия из системы аспарагината калия и магния смещает рН в сторону более физиологичного значения (от 6,8 до 7,3), при этом липофильные свойства (экстракция в органические растворители и диффузия через лецитиновый фильтр) усиливаются в два раза.
Заключение. В работе представлен методологический подход к анализу комплексных соединений магния для восполнения внутриклеточного дефицита, включающий тип комплексного соединения, его концентрацию, липофильность, а также осмоляльность исходной системы. Данные, полученные в ходе экспериментов, были подтверждены в трансляционном опыте с изолированными предсердными кардиомиоцитами, позволяющем выделить наиболее перспективный комплекс в отношении восполнения внутриклеточного дефицита магния.
КЛИНИЧЕСКИЙ СЛУЧАЙ
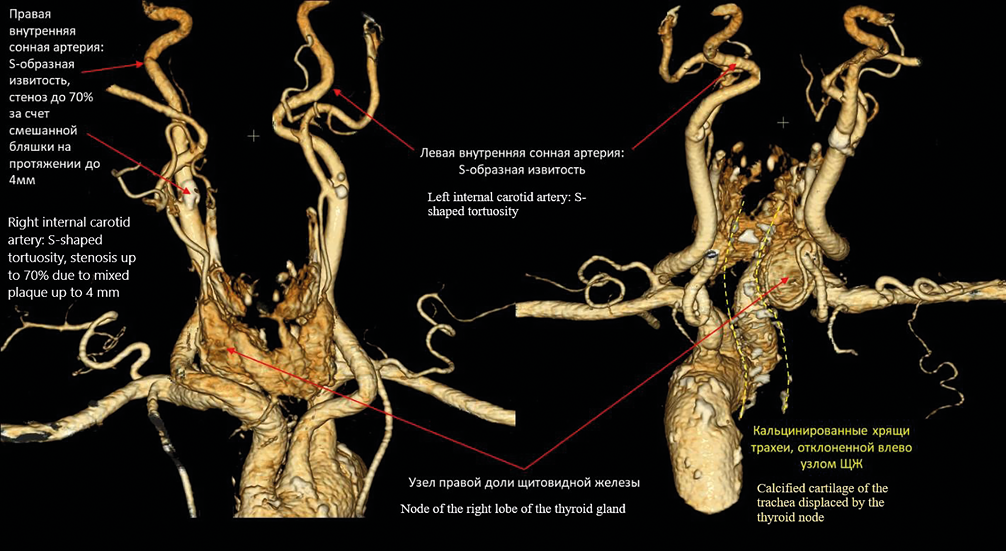
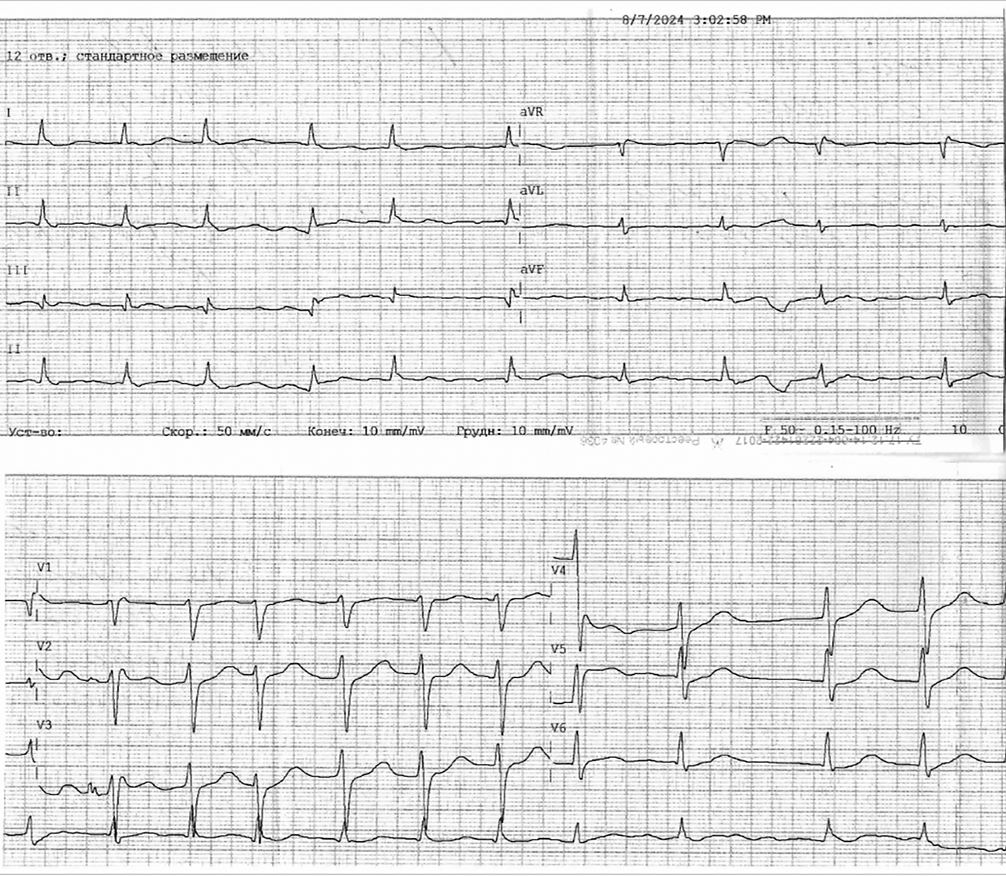
В статье описано клиническое наблюдение пациентки, 44 лет, с практически одновременным возникновением массивной тромбоэмболии лёгочной артерии с двухсторонним поражением на фоне тромбоза задней большеберцовой вены с признаками флотации тромба и эмболическим инфарктом миокарда вследствие парадоксальной эмболии и дефекта межпредсердной перегородки на фоне выраженной анемии неустановленной этиологии. При этом следует отметить выбранную тактику с первоначальным проведением первичного чрескожного коронарного вмешательства по поводу инфаркта миокарда 2 типа и тромботической окклюзии задней межжелудочковой артерии с установкой стента и последующей тромболитической терапией по поводу тромбоэмболии лёгочной артерии. В статье также обсуждаются сложные вопросы назначения и изменений в антитромботической терапии, проведённых на основании решений врачебного консилиума, что привело к значительному клиническому улучшению при выписке больной из стационара.
Механизмы лекарственно-индуцированных миопатий — прямая миотоксичность, иммуноопосредованное и непрямое повреждение мышц. Клинические проявления варьируют от бессимптомных или небольших миалгий и мышечной слабости до хронической миопатии с выраженной слабостью и в редких случаях рабдомиолиза с высвобождением продуктов клеточного распада в кровоток и межклеточное пространство. Мышечные симптомы, хотя и считаются наиболее частыми нежелательными явлениями при использовании статинов, в большинстве случаев не представляют реальной угрозы. Крайне редким осложнением терапии статинами становится рабдомиолиз. Представленный случай иллюстрирует сложности, которые возникли при дифференциальном диагнозе причин рабдомиолиза у пациентки, получавшей высокую дозу статина. Необходимость широкого применения высокоинтенсивной статинотерапии, нередко сопровождающейся одновременным использованием тикагрелора и ингибиторов протонной помпы, требует осторожности в отношении безопасности лечения, особенно у пожилых пациентов.
Из-за высокой частоты встречаемости аллергических и сердечно-сосудистых заболеваний необходимо помнить о возможности возникновения синдрома Коуниса (СК), который заключается в сочетании аллергической реакции и острого инфаркта миокарда (ОИМ). В статье описывается случай развития СК у пациента 62 лет, не имеющего атеросклеротического поражения коронарных артерий, во время инфузии плазмозамещающего раствора — декстрана — применяемого пациентом в ходе самолечения и приведшего к развитию анафилактического шока. Диагноз ОИМ подтвержден биомаркерами некроза миокарда, а также изменениями на электрои эхокардиограммах. Лечение пациента осуществлялось в соответствии с действующими нормативными документами по лечению ОИМ и аллергической реакции. Особенностью представленного клинического случая является развитие СК I типа на плазмозамещающий раствор — декстран, а также многокомпонентность ОИМ, обусловленного не только спазмом коронарной артерии, но и гипотензией, возникшей вследствие анафилактического шока. Этот случай демонстрирует важность знаний о СК, подтверждая необходимость ограничения самолечения и проведения профилактических консультаций о его последствиях.
ТОЧКА ЗРЕНИЯ
В статье рассматривается эволюция подходов к оценке риска тромбоэмболических осложнений (ТЭО) у пациентов с фибрилляцией предсердий с акцентом на роль гендерного фактора в шкале CHA2DS2-VASc, долгое время являющейся стандартом стратификации риска инсульта. Проведённый анализ исторических аспектов разных стратегий оценки риска ТЭО, начиная с рекомендаций 2001 г., когда не существовало единой оценки риска, до современных международных руководств 2024 г. доказывает, что целесообразно включение женского пола как независимого фактора риска инсульта. Современные данные свидетельствуют о нивелировании значимости гендерной принадлежности с течением времени в частоте возникновения инсультов среди пациентов с фибрилляцией предсердий и предлагают рассматривать женский пол лишь как модификатор риска инсульта, зависящий от возраста. Результаты исследований, проведённых в разных странах (Финляндия, Дания, Великобритания), подтверждают снижение влияния женского пола как самостоятельного фактора риска на частоту инсульта, определяя целесообразность перехода к упрощённой шкале CHA2DS2-VA (без учёта гендерной принадлежности). Авторы акцентируют внимание на важности индивидуальной эпизодической переоценки риска ТЭО, в особенности у пациентов с сопутствующей патологией, а также подчеркивают необходимость соблюдения настороженности при внедрении изменений в отечественную практику, учитывая специфику российской медицины и имеющиеся различия с системами здравоохранения других стран.
ЮБИЛЕЙ
В июне 2025 г. отмечает 95-летний юбилей известный российский кардиолог и терапевт, почетный кардиолог России, лауреат премии им. Д. Д. Плетнева доктор медицинских наук профессор Сыркин Абрам Львович.
ISSN 2225-3653 (Online)