Перейти к:
Синдром Коуниса I типа, развившийся при введении плазмозамещающего раствора (клинический случай)
https://doi.org/10.20996/1819-6446-2025-3164
EDN: RLRVKG
Аннотация
Из-за высокой частоты встречаемости аллергических и сердечно-сосудистых заболеваний необходимо помнить о возможности возникновения синдрома Коуниса (СК), который заключается в сочетании аллергической реакции и острого инфаркта миокарда (ОИМ). В статье описывается случай развития СК у пациента 62 лет, не имеющего атеросклеротического поражения коронарных артерий, во время инфузии плазмозамещающего раствора — декстрана — применяемого пациентом в ходе самолечения и приведшего к развитию анафилактического шока. Диагноз ОИМ подтвержден биомаркерами некроза миокарда, а также изменениями на электрои эхокардиограммах. Лечение пациента осуществлялось в соответствии с действующими нормативными документами по лечению ОИМ и аллергической реакции. Особенностью представленного клинического случая является развитие СК I типа на плазмозамещающий раствор — декстран, а также многокомпонентность ОИМ, обусловленного не только спазмом коронарной артерии, но и гипотензией, возникшей вследствие анафилактического шока. Этот случай демонстрирует важность знаний о СК, подтверждая необходимость ограничения самолечения и проведения профилактических консультаций о его последствиях.
Ключевые слова
Для цитирования:
Кожевникова Е.В., Переверзева К.Г., Гурбанова А.А., Якушин С.С. Синдром Коуниса I типа, развившийся при введении плазмозамещающего раствора (клинический случай). Рациональная Фармакотерапия в Кардиологии. 2025;21(2):182-187. https://doi.org/10.20996/1819-6446-2025-3164. EDN: RLRVKG
For citation:
Kozhevnikova E.V., Pereverzeva K.G., Gurbanova A.A., Yakushin S.S. Type I Kounis syndrome developing following administration of a plasma substitute (a clinical case). Rational Pharmacotherapy in Cardiology. 2025;21(2):182-187. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3164. EDN: RLRVKG
Введение
Синдром Коуниса (СК) — это сочетание острого коронарного синдрома (ОКС) (включая коронарный спазм, острый инфаркт миокарда (ОИМ) и тромбоз стента) с состояниями, связанными с активацией тучных клеток и тромбоцитов, на фоне аллергических, гиперчувствительных, анафилактических или анафилактоидных реакций [1][2].
Существует три типа СК:
- I тип представляет собой проявление эндотелиальной дисфункции или микрососудистой стенокардии у пациентов с неизменёнными коронарными артериями (КА) в виде их спазма, который может прогрессировать до ОИМ;
- II тип развивается у пациентов с ранее существовавшим атеросклеротическим заболеванием сердца без клинических проявлений, у которых возникает либо изолированный спазм КА, либо сочетание спазма КА с эрозией или разрывом бляшки, приводящими к ОИМ;
- III тип СК диагностируется у пациентов с тромбозом (подтип IIIa) или рестенозом стента КА (подтип IIIb) в случае наличия эозинофилов и тучных клеток в ткани тромба [3]. К данному типу СК также относятся случаи внезапной смерти пациентов после стентирования КА, при которых выявляется инфильтрация эозинофилами и тучными клетками тканей, прилегающих к стенту [3].
Аутопсийные исследования показали, что дегрануляция тучных клеток становится причиной до 13% случаев внезапной смерти [4].
Наиболее часто СК встречается на фоне применения антибактериальных и нестероидных противовоспалительных препаратов, а также контрастных веществ [5]. В зарубежной литературе зафиксированы единичные случаи возникновения данного синдрома при введении плазмозамещающих препаратов [2]. В демонстрируемом клиническом случае СК развился на введение плазмозамещающего раствора — декстрана.
Описание клинического случая
Больной К., 62 года, поступил в кардиологический стационар 07.08.2024 в 13:20 с предварительным диагнозом: ишемическая болезнь сердца: ОКС с подъёмом сегмента ST от 07.08.2024.
Из анамнеза известно, что пациент длительное время являлся донором крови и её компонентов. В связи с диагностированной эритремией в донорстве крови и её компонентов в 2024 г. пациенту отказано и 06.08.2024 с лечебной целью пациент самостоятельно произвел кровопускание и удалил ~500 мл крови (пациент — медицинский работник). Процедуру перенёс удовлетворительно. Однако утром 07.08.2024 почувствовал слабость и недомогание, в связи с чем начал инфузию декстрана. Сразу же после начала инфузии препарата почувствовал головокружение, учащённое сердцебиение, слабость, потемнение в глазах, появилась пена изо рта. Во время приступа снятие электрокардиограммы (ЭКГ) не проводилось. Коллегами пациенту внутривенно введено 8 мг дексаметазона, вызвана бригада скорой медицинской помощи, на зарегистрированной ЭКГ отмечен подъём сегмента ST в II, III, aVF отведениях (рис. 1). Введены 1,0 мл 1% морфина гидрохлорида внутривенно струйно, 5000 ЕД гепарина натрия внутривенно струйно, 400,0 мл 0,9% раствора натрия хлорида внутривенно капельно, а также 1 мл 0,1% адреналина гидрохлорида внутривенно струйно. Пациент доставлен в кардиологический стационар.
Из анамнеза известно, что в течение длительного времени страдает гипертонической болезнью (ГБ), а также поллинозом, для лечения которого использует суспензию для инъекций, содержащую бетаметазона дипропионат и бетаметазона натрия фосфат; с 36 лет — наджелудочковая экстрасистолия. В 1998 г. на введение противостолбнячной сыворотки развивалась сывороточная болезнь.
При поступлении общее состояние тяжёлое, рост 178 см, вес 85 кг, индекс массы тела — 26,8 кг/м2. В лёгких дыхание везикулярное, единичные влажные мелкопузырчатые хрипы в нижних отделах с обеих сторон, частота дыхательных движений — 16 в минуту, ритм неправильный, частота сердечных сокращений (ЧСС) — 140 уд./мин, артериальное давление (АД) — 70/40 мм рт.ст., на ЭКГ — сегмент ST в II, III, aVF отведениях на изолинии, фибрилляция предсердий (ФП) (рис. 2). В приёмном отделении даны: клопидогрел 600 мл внутрь, ацетилсалициловая кислота 250 мг внутрь. Транспортирован в рентгеноперационную, во время транспортировки произошло спонтанное восстановление синусового ритма.
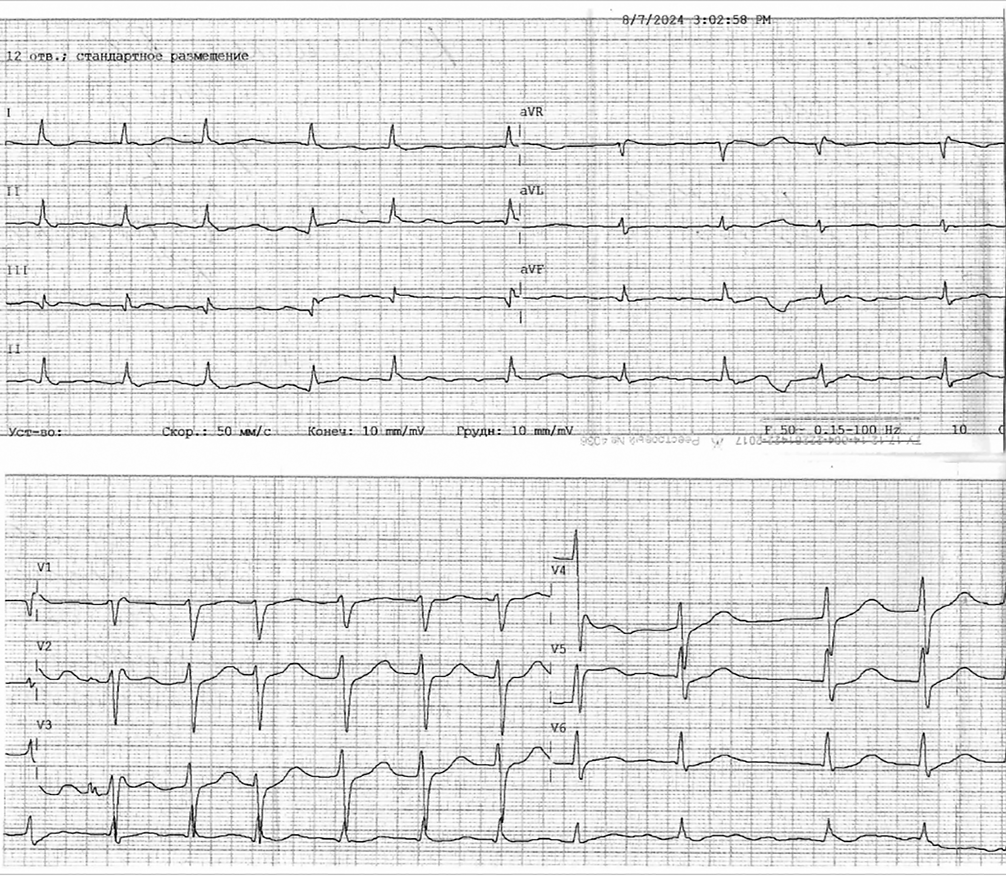
Рисунок 1. ЭКГ, зарегистрированная бригадой скорой медицинской помощи — подъём сегмента ST во II, III, aVF отведениях.
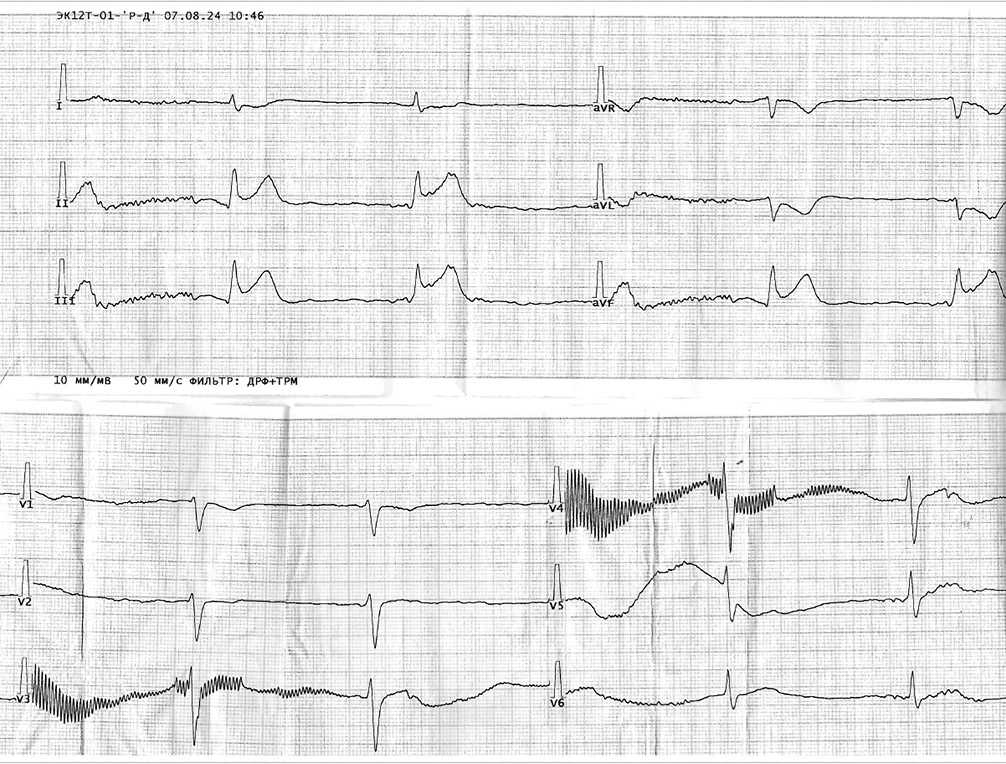
Рисунок 2. ЭКГ, зарегистрированная в приёмном отделении кардиологического стационара — фибрилляция предсердий, сегмент ST во II, III, aVF отведениях на изолинии.
07.08.2024 в 13:30 проведена коронароангиография, на которой все КА без атеросклеротического поражения.
По результатам эхокардиографии 08.08.2024 выявлена гипокинезия верхней трети нижней стенки миокарда левого желудочка (ЛЖ), дилатация полостей левого (4,6 см) и правого предсердий (4,3×5,9 см), правого желудочка (передне-задний размер — 3,1 см). Толщина задней стенки ЛЖ — 0,9 см, толщина межжелудочковой перегородки — 1,0 см. Недостаточность митрального и трикуспидального клапанов с регургитацией 2 степени. Нарушение диастолической функции ЛЖ I типа. Атеросклероз аорты. Фракция выброса ЛЖ — 63%.
В общем анализе крови 07.08.2024 и 14.08.2024 уровни лейкоцитов 29,53×109/л и 13,54×109/л, скорость оседания эритроцитов — 5 и 21 мм/час, уровни эозинофилов — 1,0 и 1,7% соответственно. В биохимическом анализе крови 08.08.2024 общий холестерин — 4,03 ммоль/л, липопротеиды низкой плотности — 2,28 ммоль/л, липопротеиды высокой плотности — 1,47 ммоль/л, триглицериды — 0,6 ммоль/л.
Динамика высокочувствительного тропонина I (07.08.2024 — 39,5 нг/л, 08.08.2024 — 200 нг/л) подтверждает диагноз ОИМ. Определение уровней гистамина и триптазы не проводилось.
По результатам холтеровского мониторирования ЭКГ 15.08.2024: синусовый ритм, эпизоды миграции суправентрикулярного водителя ритма, эктопического предсердного ритма, в т.ч. ускоренного с ЧСС от 57 до 98 уд./мин. Одиночная желудочковая экстрасистола в паре с наджелудочковой экстрасистолой, 5681 одиночных политопных наджелудочковых экстрасистол, в т.ч. с аберрантным проведением по типу блокады левой ножки пучка Гиса, эпизоды би- и тригеминии, 536 парных наджелудочковых экстрасистол, в т.ч. с аберрантным проведением по типу блокады левой ножки пучка Гиса, 23 пробежки предсердной тахикардии (максимальное количество комплексов — 9).
На фоне лечения в стационаре (хлоропирамин (блокатор гистаминовых Н1-рецепторов) с 07.08.2024 по 12.08.2024 40 мг 2 раза в сут. внутривенно струйно, дексаметазон 4 мг внутривенно струйно 07.08.2024 и по 8 мг в 250 мл 0,9% натрия хлорида с 08.08.2024 по 12.08.2024, а также терапия ОИМ в сочетании с ФП и другими наджелудочковыми нарушениями ритма — клопидогрел, аторвастатин, лизиноприл, амиодарон, ривароксабан, пантопразол) наблюдалось улучшение состояния, ангинозная боль не рецидивировала. АД стабилизировалось на уровне 130/80 мм рт.ст., ЧСС 60-65 уд./мин, однако появились папулы на медиальных поверхностях плеч и голеней. Пациент был направлен на консультацию дерматовенеролога. 14.08.2024 дерматовенерологом поставлен диагноз: лекарственная токсикодермия на декстран, стадия регресса. Рекомендовано: гипоаллергенная диета, фексофенадин (антигистаминное средство системного действия) 180 мг № 10, мазь клобетазол 2 раза в сут. В дальнейшем токсикодермия регрессировала.
Пациент выписан на 9 сутки ОИМ.
Основное заболевание: ишемическая болезнь сердца: не-Q-образующий нижне-боковой ИМ II типа 07.08.2024 (СК I типа).
Конкурирующее заболевание: аллергическая реакция по типу анафилактического шока 07.08.2024 на внутривенное введение декстрана. Лекарственная токсикодермия на декстран, стадия регресса.
Фоновое: ГБ 3 стадии. Целевой уровень АД достигнут. Риск 4. Избыточная масса тела.
Осложнения: Killip II. Пароксизм ФП со спонтанным восстановлением синусового ритма 07.08.2024 г. EHRA IIb. Эпизоды миграции суправентрикулярного ритма. Редкая одиночная желудочковая экстрасистолия. Редкая одиночная и парная политопная наджелудочковая с абберантным проведением, с эпизодами би- и тригеминии экстрасистолия. Пробежки предсердной тахикардии.
Сопутствующий диагноз: эритремия. Цереброваскулярная болезнь: хроническая ишемия головного мозга 1 стадии.
Обсуждение
Особенность данного клинического случая — развитие СК I типа на плазмозамещающий раствор — декстран, а также многокомпонентность развития ОИМ, обусловленного не только эндотелиальной дисфункцией с возможным спазмом КА, что подтверждается динамическими изменениями на ЭКГ, но и гипотензией, возникшей вследствие анафилактического шока.
Отсутствие чётких рекомендаций по диагностике и лечению СК определяет сложность ведения таких пациентов, что требует сочетания лечения острой аллергической реакции и ОИМ.
Так как адреналин способен вызвать/усилить спазм КА и вторично способствовать активации тромбоцитов посредством симпатической стимуляции, применять его стоит с осторожностью, преимущественно при отёке гортани и анафилактическом шоке [5]. Адреналин усугубляет ишемию, удлиняет интервал QT и может спровоцировать аритмию. β-блокаторы могут вызвать/усилить спазм КА из-за отсутствия антагонизма α-адренергических рецепторов. В связи с этим их также применять следует с осторожностью, отдавая предпочтение антагонистам медленных кальциевых каналов. При этом необходимо помнить, что последние могут спровоцировать или усугубить имеющуюся у пациента гипотензию. Противоаллергические препараты также должны применяться с осторожностью, т.к. могут вызвать дегрануляцию тучных клеток и привести к повторной аллергической реакции [6][7].
В представленном случае лечение пациента проводилось в соответствии с клиническими рекомендациям "ОИМ с подъёмом сегмента ST электрокардиограммы" [8] с применением внутривенного раствора адреналина гидрохлорида (обосновано введён бригадой скорой медицинской помощи), дексаметазона и хлоропирамина для лечения анафилактического шока, фексофенадина, а также клобетазола пропионата для лечения лекарственной токсикодермии. При этом в связи с имеющимися нарушениями ритма сердца, способностью β-адреноблокаторов вызывать спазм КА и невысокими показателями АД пациенту планово назначены амиодарон и ривароксабан в сочетании с клопидогрелом, а от тройной антитромботической терапии решено воздержаться, т.к. стентирование КА не проводилось.
Необходимо отметить, что в клинических рекомендациях "ОИМ с подъёмом сегмента ST электрокардиограммы" [8] рекомендации по назначению антиагрегантной терапии даны в целом для пациентов с ИМ, без уточнения типа ИМ, в связи с этим в нашей клинике пациентам с ИМ 2 типа антиагрегантная терапия назначается в полном объёме.
Назначение ривароксабана при наличии единственного пароксизма в остром периоде ИМ обусловлено тем, что ещё в клинических рекомендациях 2016 г. Европейского общества кардиологов по лечению пациентов с ФП впервые сделан акцент на целесообразность антикоагулянтной терапии у пациентов с единственным пароксизмом ФП при ОИМ [9]. В связи с тем, что в 2016 г. в Российской Федерации отсутствовали отечественные клинические рекомендации, деятельность врачей осуществлялась в соответствии с клиническими рекомендациями Европейского общества кардиологов и с 2016 г. пациентам с ФП и ОИМ при наличии единственного пароксизма ФП назначалась пероральная антикоагулянтная терапия. Необходимо отметить, что более детализированные и конкретные рекомендации в отношении этой группы пациентов были даны только в российских клинических рекомендациях 2024 г. "ОИМ с подъёмом сегмента ST электрокардиограммы", в которых указано, что "у пациентов с ИМ с подъёмом сегмента ST ЭКГ и впервые возникшей в острой фазе заболевания ФП рекомендуется рассмотреть вопрос о назначении оральных антикоагулянтов на неопределённо долгий срок, с переоценкой всей антитромботической терапии в зависимости от риска развития тромбоэмболических осложнений по шкале CHA2DS2-VASc и риска кровотечений по шкале HAS-BLED" [10]. В связи с тем, что пациент — мужчина, который имеет 2 балла по шкале CHA2DS2-VASc (ГБ и ИМ), есть все показания для назначения длительной терапии пероральными антикоагулянтами. Более того, наличие частой наджелудочковой экстрасистолии позволяет предположить, что у пациента уже имеется субклиническая ФП.
Наличие ГБ и ИМ также определило очень высокий риск сердечно-сосудистых осложнений в дальнейшем и назначение статина с целью снижения уровня холестерина липопротеидов низкой плотности <1,4 ммоль/л или >50% от исходного уровня [11].
Дискусcионным является применение амиодарона. Данный препарат был назначен исходя из того, что у пациента имелись пароксизм ФП и симптомная экстрасистолия. Назначение других антиаритмических препаратов ограничено тем, что антиаритмики IC класса пациенту противопоказаны в связи с наличием структурной патологии сердца — ИМ. Применение антиаритмиков II класса (β-блокаторов) не рекомендовано из-за предполагаемого вазоспазма и невысокого АД, от назначения антиаритмиков IV класса также отказались по причине ОИМ (рутинно не рекомендуются + невысокое АД). Антиаритмик III класса соталол также не мог быть назначен пациенту с ОИМ.
Необходимо отметить, что так как СК в основном описывается в виде отчётов о клинических случаях, показатели смертности существенно различаются — от 0 до 50% [12]. В одном ретроспективном исследовании, включавшем данные 235 420 пациентов, госпитализированных по поводу аллергии, гиперчувствительности, анафилаксии или анафилактических реакций в период с 2007 г. по 2014 г. уровень смертности составил 7% [12][13]. В работе С. С. Якушина и cоавт. показано, что летальность при СК составляет ~5,5% [5].
На прогноз СК влияют разные факторы, в т.ч. сопутствующие заболевания, чувствительность, место реакции антител с антигенами, способ попадания аллергена в организм, концентрация аллергена, количество аллергенов, воздействию которых подвергается пациент и сила первоначальной аллергической реакции [14].
Данный клинический случай подчеркивает важность развития концепции "ответственного самолечения" [15] и недопустимость привычного "самолечения", которое, по данным А. Н. Покида и соавт., широко распространено среди населения [16]. Так, в анализируемой авторами выборке из 1500 человек в возрасте 18 лет и старше установлено, что "в случае возникновения какого-либо недомогания или болезни каждый второй взрослый респондент старше 18 лет предпочитает лечиться самостоятельно, используя разные лекарства или народные средства". Похожие данные получены и рядом других исследователей, что описано в цитируемой статье [16].
Интересным является факт, что самолечение распространено и среди врачей. Например, в Швейцарии только каждый пятый врач наблюдается у врача общей практики [17], а распространённость самолечения среди медицинских работников, согласно источникам литературы, превосходит 50% [18]. В Эфиопии этот показатель составляет 67,5% [19]. Данные российских исследований неоднозначны: в них частота самолечения врачей колеблется от 11,5 [20] до 86% [21].
Заключение
В представленном клиническом случае реакция гиперчувствительности, которая привела к аллергическому ОИМ, или СК 1 типа, вызвана плазмозамещающим раствором декстраном, применяемым пациентом в ходе самолечения. Данное клиническое наблюдение показывает необходимость знаний об аллергическом ОИМ, являющимся опасным для жизни состоянием, независимо от причины аллергической реакции и типа СК. Следует помнить о возможности развития СК практически на любой лекарственный препарат, а также избегать самолечения и проводить профилактические консультации о последствиях самолечения.
Список литературы
1. Pejcic AV, Milosavljevic MN, Jankovic S, et al. Kounis syndrome associated with the use of diclofenac. Tex Heart Inst J. 2023;50(1):e217802. DOI:10.14503/THIJ21-7802.
2. Kounis NG. Kounis syndrome: an update on epidemiology, pathogenesis, diagnosis and therapeutic management. Clin Chem Lab Med. 2016;54(10):1545- 59. DOI:10.1515/cclm-2016-0010.
3. Kounis NG, Koniari I, Roumeliotis A, et al. Thrombotic responses to coronary stents, bioresorbable scaffolds and the Kounis hypersensitivity-associated acute thrombotic syndrome. J Thorac Dis. 2017;9(4):1155-64. DOI:10.21037/jtd.2017.03.134.
4. Beck SC, Wilding T, Buka RJ, et al. Biomarkers in human anaphylaxis: a critical appraisal of current evidence and perspectives. Front Immunol. 2019;10:494. DOI:10.3389/fimmu.2019.00494.
5. Yakushin S, Gurbanova A, Pereverzeva K. Kounis Syndrome: Review of Clinical Cases. Cardiovasc Hematol Disord Drug Targets. 2024;24(2):83-97. DOI:10.2174/011871529x305833240708051508.
6. Amino M, Fukushima T, Uehata A, et al. Should beta-blockers be continued as a treatment for myocardial infarction in the case of Kounis syndrome? Ann Noninvasive Electrocardiol. 2021;26(4):e12837. DOI:10.1111/anec.12837.
7. Kurosawa Y, Nirengi S, Homma T, et al. A single-dose of oral nattokinase potentiates thrombolysis and anti-coagulation profiles. Sci Rep. 2015;5:11601. DOI:10.1038/srep11601.
8. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2020. Российское кардиологическое общество, Ассоциация сердечно-сосудистых хирургов России. Российский кардиологический журнал. 2020;25(11):4103. DOI:10.15829/29/1560-4071-2020-4103.
9. Kirchhof P., Benussi S., Kotecha D. и др. Рекомендации ESC по лечению пациентов с фибрилляцией предсердий, разработанные совместно с EACTS. Российский кардиологический журнал. 2017;(7):7-86. DOI:10.15829/1560-4071-2017-7-7-86.
10. Аверков О.В., Арутюнян Г.К., Дупляков Д.В. и др. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025;30(3):6306. DOI:10.15829/1560-4071-2025-6306.
11. Ежов М.В., Кухарчук В.В., Сергиенко И.В. и др. Нарушения липидного обмена. Клинические рекомендации 2023. Российский кардиологический журнал. 2023;28(5):5471. DOI:10.15829/1560-4071-2023-5471.
12. Akbaş T, Kaya A, Altun G, et al. Cases of allergic coronary syndrome (Kounis syndrome): what we should know. Nagoya J Med Sci. 2022;84(3):664-72. DOI:10.18999/nagjms.84.3.664.
13. Desai R, Parekh T, Patel U, et al. Epidemiology of acute coronary syndrome coexistent with allergy/hypersensitivity/anaphylactic reactions (Kounis syndrome) in the United States: a nationwide inpatients analysis. Int J Cardiol. 2019;292: 35-8. DOI:10.1016/j.ijcard.2019.06.002.
14. Wang C, Fang W, Song L, et al. Analysis of Clinical Features of Non-steroidal Anti-inflammatory Drugs Induced Kounis Syndrome. Front Cardiovasc Med. 2022;9:901522. DOI:10.3389/fcvm.2022.901522.
15. Толпыгина С.Н., Марцевич С.Ю., Концевая А.В. и др. Ответственное самолечение — основополагающие принципы и место в современной системе здравоохранения. Рациональная фармакотерапия в кардиологии. 2018;14(1):101-10. DOI:10.20996/1819-6446-2018-14-1-101-11.
16. Покида А.Н., Зыбуновская Н.В. Практика самолечения российского населения в современных условиях. Здоровье населения и среда обитания. 2023;31(2):15-26. DOI:10.35627/2219-5238/2023-31-2-15-26.
17. Schulz S, Einsle F, Schneider N, et al. Illness behavior of general practitioners — a cross-sectional survey. Occup Med (Lond). 2017;67(1):33-7. DOI:10.1093/occmed/kqw135.
18. Кобякова О.С., Куликов Е.С., Деев Е.А. и др. Распространенность факторов риска хронических неинфекционных заболеваний среди медицинских работников. Кардиоваскулярная терапия и профилактика. 2018;17(3):96-104. DOI:10.15829/1728-8800-2018-3-96-104.
19. Sado E, Kassahun E, Bayisa G, et al. Epidemiology of self-medication with modern medicines among health care professionals in Nekemte town, western Ethiopia. BMC Res Notes. 2017;10(1):533. DOI:10.1186/s13104-017-2865-5.
20. Светличная Т. Г., Смирнова Е.А. Здоровье и образ жизни медицинских работников психиатрических учреждений. Социальная и клиническая психиатрия. 2015;25(2):106-11.
21. Гурьянов М.С., Камаев И.А., Коптева Л.Н. Самооценка здоровья и медицинская активность работников здравоохранения. Альманах современной науки и образования. 2008;(11):55-6.
Об авторах
Е. В. КожевниковаРоссия
Кожевникова Екатерина Владимировна, студентка 6 курса лечебного факультета
Рязань
К. Г. Переверзева
Россия
Переверзева Кристина Геннадьевна, д.м.н., профессор кафедры госпитальной терапии с курсом медико-социальной экспертизы
Рязань
А. А. Гурбанова
Россия
Гурбанова Арзу Арифовна, клинический ординатор кафедры госпитальной терапии с курсом медико-социальной экспертизы
Рязань
С. С. Якушин
Россия
Якушин Сергей Степанович, д.м.н., профессор, заведующий кафедрой госпитальной терапии с курсом медико-социальной экспертизы
Рязань
Дополнительные файлы
Рецензия
Для цитирования:
Кожевникова Е.В., Переверзева К.Г., Гурбанова А.А., Якушин С.С. Синдром Коуниса I типа, развившийся при введении плазмозамещающего раствора (клинический случай). Рациональная Фармакотерапия в Кардиологии. 2025;21(2):182-187. https://doi.org/10.20996/1819-6446-2025-3164. EDN: RLRVKG
For citation:
Kozhevnikova E.V., Pereverzeva K.G., Gurbanova A.A., Yakushin S.S. Type I Kounis syndrome developing following administration of a plasma substitute (a clinical case). Rational Pharmacotherapy in Cardiology. 2025;21(2):182-187. (In Russ.) https://doi.org/10.20996/1819-6446-2025-3164. EDN: RLRVKG

















































